水煤气是一种较清洁的气体燃料,由碳粉和水蒸气反应制得。某研究性学习小组同学为探究水煤气的成分,对此进行如下探究:
探究一:制备水煤气时利用木炭的化学性质是什么?
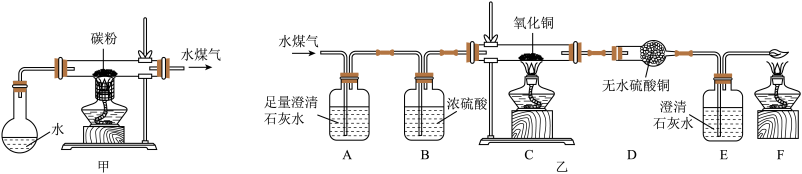
(1)小组设计如图甲所示装置进行实验(左边加热装置未标出),酒精灯上加网罩,其作用是_______ ,水煤气用碳粉和水蒸气发生反应制得,反应过程中碳粉夺取水中的氧,使水发生了还原反应,说明碳粉具有_______ 性(填“氧化”或“还原”)。
探究二:水煤气的成分是什么?
【猜想与假设】小米说:水煤气中可能是CO2、H2、O2、CO。
(2)小联说:不可能含有CO2,由于_________ 。
(3)小想说:也不可能含有O2,从安全性角度考虑,是由于________ ;于是,该小组同学认为:该气体可能是含有H2和CO。
【查阅资料】可用足量的澄清石灰水来检验和吸收二氧化碳气体;无水硫酸铜遇水由白色变成蓝色。
【进行实验】将制得的水煤气依次通过图乙装置中,观察到的现象如下:
【得出结论】
(4)水煤气的成分中含有_________ ;若D装置与E装置位置颠倒,造成的不良后果是__________ 。

探究一:制备水煤气时利用木炭的化学性质是什么?
(1)小组设计如图甲所示装置进行实验(左边加热装置未标出),酒精灯上加网罩,其作用是
探究二:水煤气的成分是什么?
【猜想与假设】小米说:水煤气中可能是CO2、H2、O2、CO。
(2)小联说:不可能含有CO2,由于
(3)小想说:也不可能含有O2,从安全性角度考虑,是由于
【查阅资料】可用足量的澄清石灰水来检验和吸收二氧化碳气体;无水硫酸铜遇水由白色变成蓝色。
【进行实验】将制得的水煤气依次通过图乙装置中,观察到的现象如下:
| 实验装置 | 实验操作的目的 | 实验现象 |
| A、B | 净化水煤气 | |
| C | 利用水煤气还原氧化铜 | 黑色粉末变红 |
| D和E | 检验反应后的产物 | D中变蓝,E中变浑浊 |
| F | 燃烧处理尾气 | 产生蓝色火焰 |
(4)水煤气的成分中含有
更新时间:2023-01-07 01:22:21
|
相似题推荐
科学探究题
|
适中
(0.65)
解题方法
【推荐1】为探究碳及其氧化物的某些性质,用以下装置进行实验(B、D装置内药品均足量)。
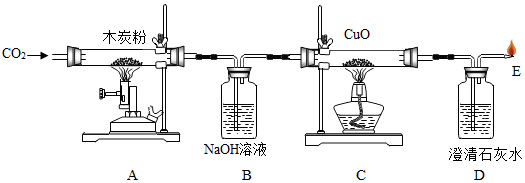
①实验过程中,A中玻璃管内发生反应的化学方程式是_____ ;C中玻璃管内的现象为_____ ,D瓶中的现象为_____ ;
②B装置的作用是_____ ;C中发生反应的化学方程式是:_____ 。
③实验过程中,_____ (从A至E中选填)处发生的反应体现了一氧化碳的化学性质。
④E处能点燃,下列说法正确的是_____ (选填编号)
A 装置A处玻璃管中反应没有完全
B 装置B处反应没有完全
C 装置C处玻璃管中反应没有完全
D 装置D处反应没有完全

①实验过程中,A中玻璃管内发生反应的化学方程式是
②B装置的作用是
③实验过程中,
④E处能点燃,下列说法正确的是
A 装置A处玻璃管中反应没有完全
B 装置B处反应没有完全
C 装置C处玻璃管中反应没有完全
D 装置D处反应没有完全
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
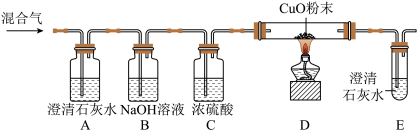
【推荐2】天然气作为燃料已进入千家万户,其主要成分是CH4。如果它不完全燃烧会生成什么物质呢?某研究性学习小组对此展开探究。
资料:1.NaOH溶液会与CO2反应,可用于吸收CO2;
2.浓硫酸能吸收空气中的水分。
【提出猜想】
(1)甲烷燃烧后的生成物中一定有_____ (填化学式),可能有CO2和CO。
【实验探究】该小组同学将生成的混合气体,依次通过如图所示的装置,验证猜想。
【现象与结论】
(2)观察到A中_______ 证明混合气体中含有CO2。
(3)观察到D中粉末由______ ,证明混合气中含有CO,D处反应的化学方程式为_______ 。
【交流讨论】
(4)有同学提出:从环保的角度看,此装置有一个不足之处,你认为是______ 。

资料:1.NaOH溶液会与CO2反应,可用于吸收CO2;
2.浓硫酸能吸收空气中的水分。
【提出猜想】
(1)甲烷燃烧后的生成物中一定有
【实验探究】该小组同学将生成的混合气体,依次通过如图所示的装置,验证猜想。
【现象与结论】
(2)观察到A中
(3)观察到D中粉末由
【交流讨论】
(4)有同学提出:从环保的角度看,此装置有一个不足之处,你认为是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】为了探究木炭在高温条件下还原氧化铜所生成的气体产物是什么,课外兴趣小组进行了如下实验探究:
(提出问题)生成的气体产物是什么?
(1)①(实验猜想)猜想1:只有CO2
猜想2:只有______ (填化学式);
猜想3:含有CO和CO2。
若猜想1成立,木炭与氧化铜反应的化学方程式为________ 。
②(实验探究)基于猜想3,根据CO和CO2的性质,兴趣小组同学设计了下图装置进行探究。(提示:NaOH溶液能吸收CO2)
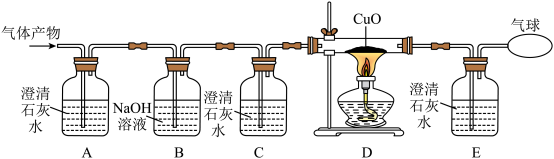
(2)观察到A装置中的澄清石灰水变浑浊,证明气体产物中有_______ (填化学式),写出澄清石灰水变浑浊的化学方程式________ 。
(3)有两种实验现象都能分别证明气体产物中含有CO。
现象1:C装置中_________ ,E装置中出现浑浊。
现象2:D装置中__________ 。
(4)C装置的作用是__________ 。
(5)图中气球的作用是_________ 。
(实验结论)通过实验探究,_______ 成立。
(提出问题)生成的气体产物是什么?
(1)①(实验猜想)猜想1:只有CO2
猜想2:只有
猜想3:含有CO和CO2。
若猜想1成立,木炭与氧化铜反应的化学方程式为
②(实验探究)基于猜想3,根据CO和CO2的性质,兴趣小组同学设计了下图装置进行探究。(提示:NaOH溶液能吸收CO2)

(2)观察到A装置中的澄清石灰水变浑浊,证明气体产物中有
(3)有两种实验现象都能分别证明气体产物中含有CO。
现象1:C装置中
现象2:D装置中
(4)C装置的作用是
(5)图中气球的作用是
(实验结论)通过实验探究,
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某学习小组将一根Zn条插入浓H2SO4中,发现Zn表面有大量气泡产生,还闻到了刺激性的气味,于是同学们提出对该产生的气体成分进行探究。
【提出问题】
该气体的成分是什么?
【查阅资料】
(1)大多数的金属与浓硫酸反应产生SO2,而活泼金属与稀硫酸反应产生H2。
(2)SO2能使品红溶液褪色。
【猜想假设】
猜想一:只有SO2; 猜想二:SO2和H2; 猜想三:______ 。
【设计实验】
如图装置进行实验(部分夹持仪器省略)
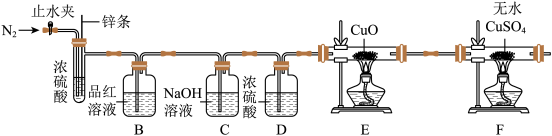
【结论与反思】
(1)通过上述实验现象及结论,可以得出猜想______ 成立。
(2)在实验步骤①中,通入N2的目的是:______ 。
(3)写出E装置中发生反应的化学方程式______ 。
【延伸与拓展】
SO2与CO2有相似的化学性质,SO2与水反应生成亚硫酸,请写出亚硫酸的化学式______ 。
实验室常用NaOH溶液处理SO2尾气,写出SO2与NaOH反应的化学方程式______ 。
【提出问题】
该气体的成分是什么?
【查阅资料】
(1)大多数的金属与浓硫酸反应产生SO2,而活泼金属与稀硫酸反应产生H2。
(2)SO2能使品红溶液褪色。
【猜想假设】
猜想一:只有SO2; 猜想二:SO2和H2; 猜想三:
【设计实验】
如图装置进行实验(部分夹持仪器省略)

| 实验步骤 | 主要现象 | 结论 |
| ①打开止水夹,先通入一段时间N2 | ||
| ②关闭止水夹,将足量Zn条下放,浸入浓硫酸中 | B装置处品红溶液褪色 | 说明气体中有 |
| ③点燃E装置处酒精灯 | E装置处固体 F装置固体变蓝色 | 说明气体中有H2 |
(1)通过上述实验现象及结论,可以得出猜想
(2)在实验步骤①中,通入N2的目的是:
(3)写出E装置中发生反应的化学方程式
【延伸与拓展】
SO2与CO2有相似的化学性质,SO2与水反应生成亚硫酸,请写出亚硫酸的化学式
实验室常用NaOH溶液处理SO2尾气,写出SO2与NaOH反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐2】某研究性学习小组的同学用电解水的方法测定水的组成后,提出问题:“测定水的组成还有其他的方法吗?”经过讨论后,得到了肯定的答案,邀请你一起对此展开探究。
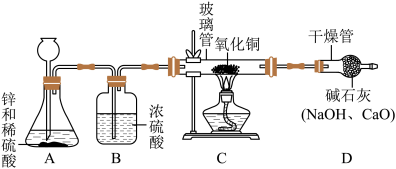
[设计方案]甲同学利用氢气还原氧化铜的原理和下图装置及药品进行实验(操作规范)。装置A中发生反应的化学方程式为______ ,洗气瓶B中浓硫酸的作用为___
[实验探究]当玻璃管中固体由黑色转变为红色时,实验测得:①装置C的玻璃管和其中固体的总质量在反应后减少了1.6g;②装置D的干燥管和其中物质的总质量在反应后增加了1.82g,用此数据算得水中H、O元素的质量比为_____ ,而由水的化学式算得H、O元素的质量比为_________ 。
[分析交流]针对上述结果与理论值有偏差,乙同学认为:该装置存在缺陷,此观点得到了大家的认同,你对此改进的方法是____ (假设生成的水完全被D中碱石灰吸收,装置内空气中的水蒸气、CO2忽略不计)。小组同学用改进后的装置重新实验得到了正确结果。
[意外发现]丙同学不小心将反应后的少量红色固体a洒落到多量稀硫酸中了,发现除了有红色固体b以外,溶液的颜色由无色变为蓝色。
[提出问题]铜与稀硫酸是不反应的,这里溶液的颜色为什么会变蓝呢?
[查阅资料]①CuO被还原的过程中会有Cu2O生成,Cu2O也能被还原在Cu;
②Cu2O固体是红色的,它一稀硫酸的反应为:
Cu2O+H2SO4=CuSO4+Cu+H2O.
[得出结论]红色固体a中含有Cu2O。
[分析交流]红色固体a中含有Cu2O是否会影响水组成的测定结果____ (填“影响”或“不影响”)。
[提出猜想]针对红色固体a的成分,小组同学提出猜想①是:Cu2O和Cu;猜想②是:___________ 。
[拓展探究]丁同学利用改进后的装置及药品重新实验,通过测量反应前后固体质量的方法去确定哪种猜想成立,他已称得:①玻璃管的质量;②反应前红色固体a和玻璃管的总质量,完全反应后,你认为他还需要称量_________ 的质量。
[教师点拨]称取一定质量的红色固体a与足量的稀硫酸充分反应后,经过滤、洗涤、干燥后再称量红色固体b的质量,也可以确定哪种猜想成立。
[定量分析]小组同学再次实验,他们开始称取质量为3.6g的红色固体a,与足量的稀硫酸完全反应后得到红色固体b为2g 。假如3.6g红色固体a都是Cu2O,请你计算出生成铜的质量(利用Cu2O+H2SO4=CuSO4+Cu+H2O.进行计算,写出计算过程);然后,通过与实际得到的固体2g进行比较,判断猜想______ 成立(填①或②)。

[设计方案]甲同学利用氢气还原氧化铜的原理和下图装置及药品进行实验(操作规范)。装置A中发生反应的化学方程式为
[实验探究]当玻璃管中固体由黑色转变为红色时,实验测得:①装置C的玻璃管和其中固体的总质量在反应后减少了1.6g;②装置D的干燥管和其中物质的总质量在反应后增加了1.82g,用此数据算得水中H、O元素的质量比为
[分析交流]针对上述结果与理论值有偏差,乙同学认为:该装置存在缺陷,此观点得到了大家的认同,你对此改进的方法是
[意外发现]丙同学不小心将反应后的少量红色固体a洒落到多量稀硫酸中了,发现除了有红色固体b以外,溶液的颜色由无色变为蓝色。
[提出问题]铜与稀硫酸是不反应的,这里溶液的颜色为什么会变蓝呢?
[查阅资料]①CuO被还原的过程中会有Cu2O生成,Cu2O也能被还原在Cu;
②Cu2O固体是红色的,它一稀硫酸的反应为:
Cu2O+H2SO4=CuSO4+Cu+H2O.
[得出结论]红色固体a中含有Cu2O。
[分析交流]红色固体a中含有Cu2O是否会影响水组成的测定结果
[提出猜想]针对红色固体a的成分,小组同学提出猜想①是:Cu2O和Cu;猜想②是:
[拓展探究]丁同学利用改进后的装置及药品重新实验,通过测量反应前后固体质量的方法去确定哪种猜想成立,他已称得:①玻璃管的质量;②反应前红色固体a和玻璃管的总质量,完全反应后,你认为他还需要称量
[教师点拨]称取一定质量的红色固体a与足量的稀硫酸充分反应后,经过滤、洗涤、干燥后再称量红色固体b的质量,也可以确定哪种猜想成立。
[定量分析]小组同学再次实验,他们开始称取质量为3.6g的红色固体a,与足量的稀硫酸完全反应后得到红色固体b为2g 。假如3.6g红色固体a都是Cu2O,请你计算出生成铜的质量(利用Cu2O+H2SO4=CuSO4+Cu+H2O.进行计算,写出计算过程);然后,通过与实际得到的固体2g进行比较,判断猜想
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
【推荐3】定性和定量结合既是化学的重要思想,也是研究物质组成的重要方法。某研究性学习小组为检测实验室用H2还原CuO所得红色固体Cu中是否含有Cu2O(红色),进行了认真的研究。请你一起踏上探究之路,回答下列问题。
【查阅资料】①无水CuSO4遇水变蓝 ②高温灼烧CuO生成Cu2O和O2③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象为_______ ,结论为红色固体中含有Cu2O.
方案2 装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O.
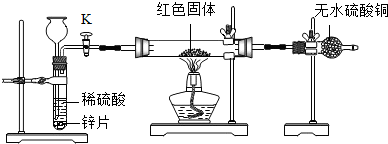
(1)为确保探究的科学、合理、安全.实验中还应采取的措施有_____ ;(填序号)
①加热前先排尽装置中的空气
②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶
(2)由方案2实验后得出结论:红色固体中含有Cu2O.写出红色固体Cu2O与H2反应的化学方程式_______________
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg.
(1)该实验方案最少得进行_____ 次称量;
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为_____ .
【查阅资料】①无水CuSO4遇水变蓝 ②高温灼烧CuO生成Cu2O和O2③Cu2O与稀H2SO4反应:Cu2O+H2SO4=Cu+CuSO4+H2O
【设计实验方案】
方案1 取该红色固体加入适量稀H2SO4,实验现象为
方案2 装置如图所示,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O.

(1)为确保探究的科学、合理、安全.实验中还应采取的措施有
①加热前先排尽装置中的空气
②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在盛有CuSO4的干燥管后再连接一个装有浓H2SO4的洗气瓶
(2)由方案2实验后得出结论:红色固体中含有Cu2O.写出红色固体Cu2O与H2反应的化学方程式
方案3 称得干燥坩埚(常用于固体加热的容器)的质量为ag,取红色固体置于坩埚中称得总质量为bg,在空气中高温灼烧至质量恒定,称得最后坩埚与固体总质量为cg.
(1)该实验方案最少得进行
(2)若确认红色固体中含有Cu2O,则c与a,b应符合的数学关系式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】小华同学欲通过实验探究“用酒精灯给物质加热时,应该用哪一层火焰”,请你帮助他完成实验探究过程的设计,并根据实验数据得出结论,还要回答实验过程中的有关问题。
【提出问题】用酒精灯给物质加热时,应该用哪一层火焰?
【做出猜测】你的猜测是_____ 。
【活动过程和记录】取三支试管,各加入5mL水。
①将其中一支试管的底部放在酒精灯火焰上方约3cm处加热;
②将另一支试管的底部放在内焰部分加热;
③将第三支试管的底部放在外焰部分加热。
记录上述三种情况下将水加热至沸腾所需时间(假设以上情况下试管不会破裂):
【问题和讨论】
①上述实验三支试管中,各加入5mL水,即要求所取水的量相同,若不相同,行吗?为什么?_____ 。
②若不用以上探究方法,你认为还可以有其他方法吗?若有,请简要叙述操作过程、现象及结论。_____
【提出问题】用酒精灯给物质加热时,应该用哪一层火焰?
【做出猜测】你的猜测是
【活动过程和记录】取三支试管,各加入5mL水。
①将其中一支试管的底部放在酒精灯火焰上方约3cm处加热;
②将另一支试管的底部放在内焰部分加热;
③将第三支试管的底部放在外焰部分加热。
记录上述三种情况下将水加热至沸腾所需时间(假设以上情况下试管不会破裂):
| 第①种情况 | 第②种情况 | 第③种情况 | |
| 所需时间/s | 87 | 54 | 25 |
【问题和讨论】
①上述实验三支试管中,各加入5mL水,即要求所取水的量相同,若不相同,行吗?为什么?
②若不用以上探究方法,你认为还可以有其他方法吗?若有,请简要叙述操作过程、现象及结论。
您最近一年使用:0次
【推荐2】萧红中学八年级“爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如下实验,请回答下列问题:
(1)为了使酒精灯火焰集中,提高温度达到高温的条件,可以在酒精灯上加______ 。
(2)请写出C与CuO反应的化学方程式_________ 。
(3)实验结束时,应_________ (填序号)。
①先撒出导管,再熄灭酒精灯 ②先熄灭酒精灯,再撤出导管
【猜想与假设】试管冷却后,同学们将试管中的固体取出,试管内的固体可能是什么?
小L的猜想:固体物质是碳和铜
小P的猜想:固体物质是氧化铜和铜
小G的猜想:固体物质是氧化铜、碳和铜
(4)你的猜想:固体物质还可能________ 。
【制定计划】
(5)同学们一致认为试管中的固体一定有铜,原因是:小L说:Cu是_____ 固体,而碳和氧化铜都是黑色固体,通过观察能够发现;小P说:固体中一定有铜还因为_____ ,所以铜一定存在。
【实验结论】
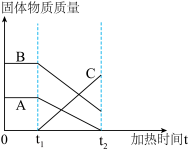
(6)最后经过实验证明小P的猜想正确,小P同学绘制了试管中某固体物质的质量变化趋势图,其中表示CuO的是______ 。(填“A”或“B”或“C”)
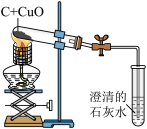
(1)为了使酒精灯火焰集中,提高温度达到高温的条件,可以在酒精灯上加
(2)请写出C与CuO反应的化学方程式
(3)实验结束时,应
①先撒出导管,再熄灭酒精灯 ②先熄灭酒精灯,再撤出导管
【猜想与假设】试管冷却后,同学们将试管中的固体取出,试管内的固体可能是什么?
小L的猜想:固体物质是碳和铜
小P的猜想:固体物质是氧化铜和铜
小G的猜想:固体物质是氧化铜、碳和铜
(4)你的猜想:固体物质还可能
【制定计划】
(5)同学们一致认为试管中的固体一定有铜,原因是:小L说:Cu是
【实验结论】
(6)最后经过实验证明小P的猜想正确,小P同学绘制了试管中某固体物质的质量变化趋势图,其中表示CuO的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究。
(1)贝贝取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。
结论:石蜡的密度比水_____ ,溶解性_____ ,硬度_____ 。
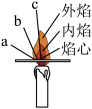
(2)芳芳点燃蜡烛,观察到火焰分为_____ 、_____ 、_____ 三层。为探究火焰三层的温度,她取用一根火柴梗,_____ ,如图所示。取出火柴梗后看到_____ (填“a”“b”或“c”)处最先炭化。
结论:蜡烛火焰的温度最高。
兴趣小组随后提出对酒精灯的火焰温度进行如下探究。
【提出问题】酒精灯火焰哪部分温度最高?
【做出猜想】猜想一:酒精灯火焰外焰温度最高;
猜想二:酒精灯火焰内焰温度最高;
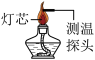
【实验探究】该小组同学用特殊的测温仪器装置进行实验(如图),测得酒精灯各层火焰温度和平均温度如下表(探头位置是指测温探头离灯芯的垂直高度):
(3)根据上表数据,用酒精灯加热仪器或药品时用_____ 加热最好。
(4)实验中,若燃着的酒精灯中酒精不足,现要添加酒精,采取的操作是:先_____ ,再向酒精灯中添加酒精。添加的酒精量不超过酒精灯容积的_____ (填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(5)用酒精灯给试管里的液体加热,加热时试管与灯芯接触的不良后果是_____ 。
【交流反思】不仅酒精灯的各层火焰温度不同,而且相同火焰层在不同位置,温度也有差异。
(6)该小组在测量酒精灯的相同火焰层,所测试温度有差异,经小组讨论分析除了与测温探头距离灯芯的垂直距离有关,你认为还可能的原因有哪些?(写出一点即可)_____ 。
(1)贝贝取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛浮在水面上。
结论:石蜡的密度比水
(2)芳芳点燃蜡烛,观察到火焰分为
结论:蜡烛火焰的温度最高。

兴趣小组随后提出对酒精灯的火焰温度进行如下探究。
【提出问题】酒精灯火焰哪部分温度最高?
【做出猜想】猜想一:酒精灯火焰外焰温度最高;
猜想二:酒精灯火焰内焰温度最高;
【实验探究】该小组同学用特殊的测温仪器装置进行实验(如图),测得酒精灯各层火焰温度和平均温度如下表(探头位置是指测温探头离灯芯的垂直高度):

| 火焰层 | 焰心 | 内焰 | 外焰 | |||
| 探头位置(cm) | 0.5 | 1.5 | 2.5 | 3.0 | 4.0 | 4.5 |
| 火焰温度(℃) | 537 | 670 | 775 | 806 | 750 | 667 |
| 平均温度(℃) | 603 | 791 | 708 | |||
(4)实验中,若燃着的酒精灯中酒精不足,现要添加酒精,采取的操作是:先
 ”、“
”、“ ”或“
”或“ ”)。
”)。(5)用酒精灯给试管里的液体加热,加热时试管与灯芯接触的不良后果是
【交流反思】不仅酒精灯的各层火焰温度不同,而且相同火焰层在不同位置,温度也有差异。
(6)该小组在测量酒精灯的相同火焰层,所测试温度有差异,经小组讨论分析除了与测温探头距离灯芯的垂直距离有关,你认为还可能的原因有哪些?(写出一点即可)
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
【推荐1】月饼包装袋内常有一包食品脱氧剂。某化学兴趣小组想要探究食品脱氧剂的成分,剪开新鲜月饼包装袋,经精细分拣后发现脱氧剂大部分为黑色固体,还有少量白色粉末。
【提出问题】黑色粉末的成分是什么?
【猜想与假设】小组同学议论纷纷:
猜想1:可能有铁粉;猜想2:可能有炭粉;猜想3:可能有铜粉。
(1)小组同学根据观察到的现象一致认为猜想3不成立,其理由是_______ 。
【探究1】
(2)小组同学根据另两种猜想设计了如下实验方案,请完成下表:
【反思与评价】
(3)该同学取少量黑色粉末,加入稀盐酸,产生现象_______ 。该现象能进一步确认有铁粉存在,与步骤1所得结论一致。
(4)步骤2中涉及的一个反应化学方程式为_______ 。
(5)经查阅资料,对照实验结论,大家认识到了脱氧剂的脱氧原理是利用了铁与_______ 发生生锈反应的性质从而延长食品的保质期。
【探究2】
同学们经查阅资料,明确了脱氧剂中的白色粉末是硅藻土。硅藻土是一种填充剂,不溶于水,其作用在于吸附水分,为脱氧反应提供水分,同时疏松配料,使氧气易于接触铁粉。
(6)硅藻土疏松多孔,具有吸附性,与实验室常见的_______ (填物质名称)相似。
(7)如图是每克脱氧剂中硅藻土用量与脱氧时间的关系图,可知:硅藻土的最佳用量比例是_____ %。(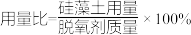 )
)
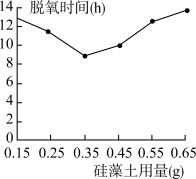
(8)硅藻土含量通常控制在最佳用量比,高于或低于最佳量时,脱氧速度均会减慢。请分别分析可能的原因,硅藻土用量过多时,_______ ;硅藻士用量过少时,_______ 。
(9)脱氧剂的脱氧速度还有可能受哪些因素影响?请写出一条并说明理由:_______ 。
【提出问题】黑色粉末的成分是什么?
【猜想与假设】小组同学议论纷纷:
猜想1:可能有铁粉;猜想2:可能有炭粉;猜想3:可能有铜粉。
(1)小组同学根据观察到的现象一致认为猜想3不成立,其理由是
【探究1】
(2)小组同学根据另两种猜想设计了如下实验方案,请完成下表:
| 实验步骤 | 实验原理 | 操作及实验现象(假设每步操作均完全) | 实验结论 |
| 步骤1 | 物理方法 | 猜想1成立 | |
| 步骤2 | 化学方法 | 取步骤1剩余黑色粉末样品充分灼烧,产生气体通入澄清石灰水,观察到澄清石灰水 | 猜想2成立 |
【反思与评价】
(3)该同学取少量黑色粉末,加入稀盐酸,产生现象
(4)步骤2中涉及的一个反应化学方程式为
(5)经查阅资料,对照实验结论,大家认识到了脱氧剂的脱氧原理是利用了铁与
【探究2】
同学们经查阅资料,明确了脱氧剂中的白色粉末是硅藻土。硅藻土是一种填充剂,不溶于水,其作用在于吸附水分,为脱氧反应提供水分,同时疏松配料,使氧气易于接触铁粉。
(6)硅藻土疏松多孔,具有吸附性,与实验室常见的
(7)如图是每克脱氧剂中硅藻土用量与脱氧时间的关系图,可知:硅藻土的最佳用量比例是
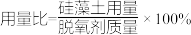 )
)
(8)硅藻土含量通常控制在最佳用量比,高于或低于最佳量时,脱氧速度均会减慢。请分别分析可能的原因,硅藻土用量过多时,
(9)脱氧剂的脱氧速度还有可能受哪些因素影响?请写出一条并说明理由:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】小乔、小渝和小江三位同学进行下图两个实验
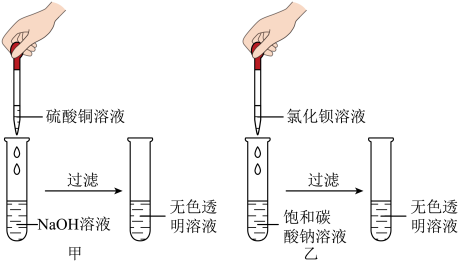
(1)甲实验中反应化学方程式为_________
(2)实验结束后,三位同学把实验后的三支试管的溶液倒入同一个烧杯中,烧杯中没有明显现象,他们决定对溶液溶质成分进行探究
【提出问题】烧杯中溶质成分是什么?
小乔和小渝两位同学讨论后一致认为溶液中一定含有________ ,溶质中还可能含有什么?
【进行猜想】小乔认为溶液中溶质可能有Na2CO3;小渝认为溶液中溶质可能有_________ ;小江认为溶液中溶质可能NaOH和Na2CO3都有
【验证猜想】小江为了验证自己的猜想,设计了如下实验
【结论分析】小乔认为实验操作②的结论不严谨,因为_________ ;若要确定小江猜想是否成立,应另取少量烧杯中的溶液于试管中,滴加足量的________
【拓展与思考】如果实验①中测得PH=7,烧杯中溶液的溶质成分是_______

(1)甲实验中反应化学方程式为
(2)实验结束后,三位同学把实验后的三支试管的溶液倒入同一个烧杯中,烧杯中没有明显现象,他们决定对溶液溶质成分进行探究
【提出问题】烧杯中溶质成分是什么?
小乔和小渝两位同学讨论后一致认为溶液中一定含有
【进行猜想】小乔认为溶液中溶质可能有Na2CO3;小渝认为溶液中溶质可能有
【验证猜想】小江为了验证自己的猜想,设计了如下实验
| 实验操作 | 现象 | 结论 |
| ①取少量烧杯中的溶液于试管中,测定pH | pH>7 | 溶液呈碱性 |
| ②另取少量烧杯中的溶液于试管中,滴加足量BaCl2,静置,在滴加无色酚酞 | 溶液由无色变为红色 | 小江的猜想成立 |
【拓展与思考】如果实验①中测得PH=7,烧杯中溶液的溶质成分是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】下图是灭火器原理模拟示意图。
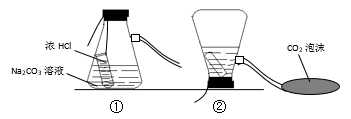
(1)上述装置②发生反应的化学方程式是_______________________ 。
(2)CO2灭火的原理是_______________________ 。
(3)某同学对装置②反应后的溶液中溶质的成分进行探究。
【查阅资料】氯化银不溶于酸
【提出猜想】装置②反应后的溶液中溶质为:
I.________ ;II.HCl和NaCl;III.Na2CO3和NaCl。
【进行实验】
【拓展与思考】如果猜想II成立,产生此结果的原因是实验时____________________ 。反应后溶液溶质不可能出现的组合是NaCl、Na2CO3、HCl,原因是__________ 。

(1)上述装置②发生反应的化学方程式是
(2)CO2灭火的原理是
(3)某同学对装置②反应后的溶液中溶质的成分进行探究。
【查阅资料】氯化银不溶于酸
【提出猜想】装置②反应后的溶液中溶质为:
I.
【进行实验】
| 实验装置及操作 | 实验现象与结论 |
| a.取装置②反应后的溶液于试管中,加入足量稀HNO3。 b.继续向a的溶液中滴加 | c.有气体产生;猜想1、猜想II不成立。 d. |
【拓展与思考】如果猜想II成立,产生此结果的原因是实验时
您最近一年使用:0次



