名校
解题方法
1 . 性质决定用途。下列物质的性质与用途具有对应关系的是
| A.N2是无色气体,可用作保护气 |
| B.盐酸具有酸性,可用于除铁锈 |
| C.氢气具有可燃性,可用于填充探空气球 |
| D.浓硫酸具有腐蚀性,可作干燥剂 |
您最近一年使用:0次
2 . 在O2、H2、CO、CO2、CH4五种气体中,常用来灭火的是_______ ,有还原性而无毒的是_______ ,在空气中能燃烧生成使澄清石灰水变浑浊的气体是_______ ,能与血红蛋白结合使人中毒的是_______ 。
您最近一年使用:0次
解题方法
3 . 下列有关物质的性质和用途对应关系正确的是
| A.活性炭有吸附性,可用作除味剂 | B.铜有导热性,可用于制电线 |
| C.氢气具有还原性,可用作燃料 | D.盐酸有挥发性,可用于除铁锈 |
您最近一年使用:0次
解题方法
4 . 下列物质的用途中,利用其化学性质的是
| A.干冰用于人工降雨 | B.焦炭用于炼铁工业 | C.氢气用于填充气球 | D.金用于制作金箔 |
您最近一年使用:0次
解题方法
5 . 今年我国已有多款家用型“氢能自行车”投放市场,“氢能进万家”战略进一步落实。氢能自行车配套有“微型太阳能制充氢一体机”、氢燃料电池、储氢燃料棒。______ (答1条)。
(2)氢能自行车轮胎由合成橡胶制成,合成橡胶属于以下哪种材料______(填序号)。
(3)氢能自行车的车把、轴承、挡泥板等都是钢材制成的,请任选一个部件写出一种合理的防锈方法______ 。
(4)在氢燃料电池中,氢气与外界进来的氧气在催化剂作用下化合生成水,同时为自行车提供电力,这一过程中的能量转化形式是______ 能转化为电能。
(5)微型太阳能制充氢一体机可以连接太阳能电池板或家用电源,能将一杯水电解出200L氢气,并将氢气充入储氢燃料棒中,该制氢反应的化学方程式是______ ,氢气在连接电源的______ 极产生。
(6)氢能源的优点是______ (答1条)。

(2)氢能自行车轮胎由合成橡胶制成,合成橡胶属于以下哪种材料______(填序号)。
| A.有机高分子材料 | B.金属材料 | C.复合材料 |
(3)氢能自行车的车把、轴承、挡泥板等都是钢材制成的,请任选一个部件写出一种合理的防锈方法
(4)在氢燃料电池中,氢气与外界进来的氧气在催化剂作用下化合生成水,同时为自行车提供电力,这一过程中的能量转化形式是
(5)微型太阳能制充氢一体机可以连接太阳能电池板或家用电源,能将一杯水电解出200L氢气,并将氢气充入储氢燃料棒中,该制氢反应的化学方程式是
(6)氢能源的优点是
您最近一年使用:0次
解题方法
6 . 小华用如图所示的实验装置进行电解水的实验。一段时间后停止通电,在玻璃管b中收集到0.16g气体。___________ (答一点即可)。
(2)请计算该实验过程中,消耗的水的质量。

(2)请计算该实验过程中,消耗的水的质量。
您最近一年使用:0次
解题方法
7 . 我国力争2060年前实现“碳中和”,捕集、封存CO2是实现“碳中和”的一种途径。对于化石燃料产生的CO2捕集技术主要有两种:燃烧前捕集技术和燃烧后捕集技术。
(1)燃烧前捕集技术:将化石燃料与水蒸气在一定条件下反应生成的水煤气(CO和H2)加以利用,再将CO2分离出来。以煤为例,流程图如图:______ 。
②利用膜分离法可从CO2与H2混合气体中捕集CO2,这一过程属于_______ (选填“物理变化”或“化学变化”)。分离出的H2的用途有_______ (写一种)。
(2)燃烧后捕集技术:捕获化石燃料燃烧后烟气中的CO2,实现CO2的富集。
①常用的CO2分离方法是化学吸收法,如热钾碱法吸收CO2,其原理是利用碳酸钾溶液吸收CO2生成碳酸氢钾(称为富液);再加热富液,释放CO2,实现CO2的富集。写出生成富液的化学方程式:_______ 。
②富氧燃烧技术是采用纯氧代替空气供化石燃料燃烧,这一捕获CO2技术的优点是______ 。
(1)燃烧前捕集技术:将化石燃料与水蒸气在一定条件下反应生成的水煤气(CO和H2)加以利用,再将CO2分离出来。以煤为例,流程图如图:

②利用膜分离法可从CO2与H2混合气体中捕集CO2,这一过程属于
(2)燃烧后捕集技术:捕获化石燃料燃烧后烟气中的CO2,实现CO2的富集。
①常用的CO2分离方法是化学吸收法,如热钾碱法吸收CO2,其原理是利用碳酸钾溶液吸收CO2生成碳酸氢钾(称为富液);再加热富液,释放CO2,实现CO2的富集。写出生成富液的化学方程式:
②富氧燃烧技术是采用纯氧代替空气供化石燃料燃烧,这一捕获CO2技术的优点是
您最近一年使用:0次
解题方法
8 . 二氧化碳和甲烷在一定条件下发生反应,其分子种类变化的微观示意图如下,利用该反应可实现二氧化碳的资源化利用。
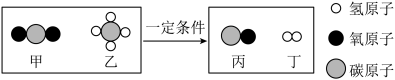
| A.四种物质中属于氧化物的只有丙 |
| B.丁可以做气体燃料 |
| C.丁中的氢元素全部来自乙 |
| D.参加反应的甲和乙的分子个数比为1:1 |
您最近一年使用:0次
9 . 食盐是生活必需品,也是重要的化工原料。
(1)电解饱和食盐水可以得到多种化工产品,主要过程如下:______ 。
②碱B的化学式为______ ,判断的依据是______ 。
(2)某食盐中添加了碘酸钾 和亚铁氰化钾(
和亚铁氰化钾(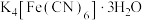 ,相对分子质量为422)。其中亚铁氰化钾可防止食盐结块,但人们总是担心其会分解产生剧毒的氰化钾
,相对分子质量为422)。其中亚铁氰化钾可防止食盐结块,但人们总是担心其会分解产生剧毒的氰化钾 。某同学对亚铁氰化钾受热分解进行了探究,其热重分析数据如图:
。某同学对亚铁氰化钾受热分解进行了探究,其热重分析数据如图:
回答下列问题:
①该食盐中至少含有______ 种金属元素(填一数字)。
②写出70℃~100℃反应的化学方程式______ ;当温度达到400℃时,会产生剧毒的 ,同时还会产生一种单质气体X,则X的化学式是
,同时还会产生一种单质气体X,则X的化学式是______ 。
③食用含亚铁氰化钾作抗结剂的食盐是否安全?其理由是______ 。
(1)电解饱和食盐水可以得到多种化工产品,主要过程如下:
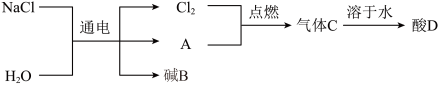
②碱B的化学式为
(2)某食盐中添加了碘酸钾
 和亚铁氰化钾(
和亚铁氰化钾(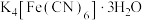 ,相对分子质量为422)。其中亚铁氰化钾可防止食盐结块,但人们总是担心其会分解产生剧毒的氰化钾
,相对分子质量为422)。其中亚铁氰化钾可防止食盐结块,但人们总是担心其会分解产生剧毒的氰化钾 。某同学对亚铁氰化钾受热分解进行了探究,其热重分析数据如图:
。某同学对亚铁氰化钾受热分解进行了探究,其热重分析数据如图: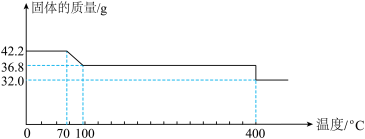
回答下列问题:
①该食盐中至少含有
②写出70℃~100℃反应的化学方程式
 ,同时还会产生一种单质气体X,则X的化学式是
,同时还会产生一种单质气体X,则X的化学式是③食用含亚铁氰化钾作抗结剂的食盐是否安全?其理由是
您最近一年使用:0次
10 . 阅读下面的科普短文,回答相关问题。
氨(NH3)是一种重要的化学物质,可用于制造硝酸和氮肥。氨主要来自于人工合成。1909年,弗里茨•哈伯成功地利用氮气、氢气合成出氨。为了找到合成氨反应合适的催化剂,人们做了6500多次实验,发现铁触媒效果较好。1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)工业上合成氨的原料是氢气和_______ 。
(2)科学家研究合成氨反应催化剂的目的是_______ 。
(3)氨可用于制造氮肥,下列肥料属于氮肥的是______。
氨(NH3)是一种重要的化学物质,可用于制造硝酸和氮肥。氨主要来自于人工合成。1909年,弗里茨•哈伯成功地利用氮气、氢气合成出氨。为了找到合成氨反应合适的催化剂,人们做了6500多次实验,发现铁触媒效果较好。1913年第一座合成氨工厂建立。如今全球合成氨年产量超千万吨,其中大约85%的氨用于生产氮肥,缓解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)工业上合成氨的原料是氢气和
(2)科学家研究合成氨反应催化剂的目的是
(3)氨可用于制造氮肥,下列肥料属于氮肥的是______。
| A.NH4NO3 | B.KCl | C.NaNO3 | D.Ca3(PO4)2 |
您最近一年使用:0次



