学习了金属的化学性质后,小月对Zn、Fe、Cu的活泼程度进行了如下实验验证。
实验一:利用金属与金属化合物溶液反应来验证金属活动性,设计了如图实验方案。
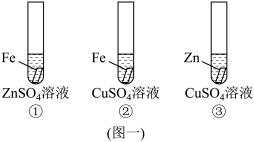
(1)实验一中,试管②里发生的反应现象为______ 。
(2)验证金属活动性:Zn>Fe>Cu
上述实验中,没有必要做的是______ (填试管序号)。
实验二:能否利用金属与酸反应的速率验证金属活动性强弱?
【查阅资料】影响化学反应速率的因素除了物质本身的化学性质外,还有温度、反应物浓度、接触面积等因素。
【实验验证】如图二,取大小相同的金属片,分别加入到相同的三份稀盐酸中,并用温度传感器测定一段时间反应过程中温度变化。所得温度变化曲线如图三所示。
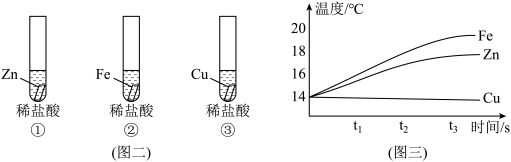
(3)实验二中,有明显现象的是试管______ (填试管序号)。
(4)实验二中,试管里②发生化学反应方程式为______ 。
(5)根据图三分析,金属与酸反应属于______ (填“吸热”或“放热”)反应。
【反思交流】根据上述金属与酸反应的实验,能否验证得出金属活动性:
Zn>Fe>Cu?请做出判断并说明理由______ 。
【拓展延伸】为得到活动性:Zn>Fe>Cu的结论,小月提出,可在原实验二方案基础上,再直接利用一种药品完成实验即可,该药品可能是______ 。
A.CuSO4 B.FeSO4 C.MgSO4
实验一:利用金属与金属化合物溶液反应来验证金属活动性,设计了如图实验方案。

(1)实验一中,试管②里发生的反应现象为
(2)验证金属活动性:Zn>Fe>Cu
上述实验中,没有必要做的是
实验二:能否利用金属与酸反应的速率验证金属活动性强弱?
【查阅资料】影响化学反应速率的因素除了物质本身的化学性质外,还有温度、反应物浓度、接触面积等因素。
【实验验证】如图二,取大小相同的金属片,分别加入到相同的三份稀盐酸中,并用温度传感器测定一段时间反应过程中温度变化。所得温度变化曲线如图三所示。

(3)实验二中,有明显现象的是试管
(4)实验二中,试管里②发生化学反应方程式为
(5)根据图三分析,金属与酸反应属于
【反思交流】根据上述金属与酸反应的实验,能否验证得出金属活动性:
Zn>Fe>Cu?请做出判断并说明理由
【拓展延伸】为得到活动性:Zn>Fe>Cu的结论,小月提出,可在原实验二方案基础上,再直接利用一种药品完成实验即可,该药品可能是
A.CuSO4 B.FeSO4 C.MgSO4
更新时间:2023/02/17 22:32:38
|
相似题推荐
科学探究题
|
适中
(0.65)
名校
解题方法
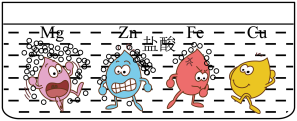
【推荐1】已知某金属材料中含有镁、锌、铁、铜中的两种,小明在老师的指导下对该金属材料的成分进行探究。
【查阅资料】金属与盐酸反应的比较,如图所示。得出这四种金属的活动性由强到弱的顺序是______ 。
【进行实验】
实验一:
实验二:
步骤1:另取金属材料,用砂纸打磨,称量其质量为20g;
步骤2:将打磨过的金属材料没入过量的硫酸锌溶液中,过一会儿取出,洗净,在一定条件下烘干,称量其质量大于20g;
【得出结论】该金属材料中除铁外,还含有_________ 。步骤2中反应的化学方程式为_________ 。
【拓展提升】将该金属材料加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤液和滤渣,将所得滤渣放入稀盐酸中,有气泡产生。则滤液里一定含有_________ (填写化学式,下同),滤渣中一定含有_________ 。
【查阅资料】金属与盐酸反应的比较,如图所示。得出这四种金属的活动性由强到弱的顺序是

【进行实验】
实验一:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量打磨过的金属材料于试管中,加入 | 固体全部溶解, | 金属材料中一定有铁,一定没有 |
步骤1:另取金属材料,用砂纸打磨,称量其质量为20g;
步骤2:将打磨过的金属材料没入过量的硫酸锌溶液中,过一会儿取出,洗净,在一定条件下烘干,称量其质量大于20g;
【得出结论】该金属材料中除铁外,还含有
【拓展提升】将该金属材料加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤液和滤渣,将所得滤渣放入稀盐酸中,有气泡产生。则滤液里一定含有
您最近一年使用:0次
【推荐2】在学习金属的化学性质时,老师在课堂上给学生们演示了如图实验:
(1)(知识回放)金属活动性顺序:K Ca Na Mg_______ Zn Fe Sn Pb(H)Fe Hg Ag Pt Au,请你在上面横线上填写对应金属的元素符号。
(2)(给出资料)M是一种金属,MSO4溶液是无色液体。
(实验目的)探究M 与铜、铝的活动性顺序。
(猜想与假设)猜想Ⅰ:Al>Cu>M;猜想Ⅱ:Al>M>Cu;猜想Ⅲ:_______ 。
(3)(进行实验)
第一步:老师取出M 丝、铜丝、铝丝用砂纸进行打磨,目的是_______ 。
第二步:老师按照如图进行实验操作,要求同学们填写如下表格:
第三步:根据表格,可判断猜想Ⅱ正确。
(4)(交流表达)
老师要求同学们写出试管丙中反应的化学方程式_______ 。
然后经同学们讨论后大家认为该实验可以优化,去掉试管_______ (填试管编号)中的实验,也可以得出正确的结论。
(1)(知识回放)金属活动性顺序:K Ca Na Mg
(2)(给出资料)M是一种金属,MSO4溶液是无色液体。
(实验目的)探究M 与铜、铝的活动性顺序。
(猜想与假设)猜想Ⅰ:Al>Cu>M;猜想Ⅱ:Al>M>Cu;猜想Ⅲ:
(3)(进行实验)
第一步:老师取出M 丝、铜丝、铝丝用砂纸进行打磨,目的是
第二步:老师按照如图进行实验操作,要求同学们填写如下表格:
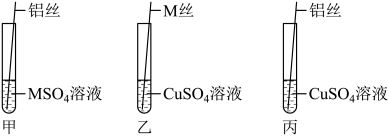
| 实验操作 | 实验现象 | 实验结论 |
| 铝丝插入装有MSO4溶液的试管中(图甲) | 铝丝表面出现一层黑色物质 | |
| M丝插入装有CuSO4溶液的试管中(图乙) | M丝表面出现一层红色物质,溶液的颜色 | M>Cu |
| 铝丝插入装有CuSO4溶液的试管中(图丙) | 铝丝表面出现一层红色物质,颜色由蓝色变为无色 | Al>Cu |
(4)(交流表达)
老师要求同学们写出试管丙中反应的化学方程式
然后经同学们讨论后大家认为该实验可以优化,去掉试管
您最近一年使用:0次
【推荐3】某化学兴趣小组的学生,发现金属R不在初中学到的金属活动性顺序表中,该小组为了了解R与常见金属铝、铜的金属活动性顺序,进行如下探究活动:
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R; 猜想二:____________ ; 猜想三:R>Al>Cu,
【查阅资料】 R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色。
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究。
【交流反思】究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误。于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色______________ ,进而确认猜想三不成立,猜想二成立。
【作出猜想】他们考虑到铝的活动性比铜强,对三种金属的活动性顺序作出如下猜想:
猜想一:Al>Cu>R; 猜想二:
【查阅资料】 R是一种银白色的金属,在R的盐溶液中只有+2价R的盐溶液呈蓝色,常温下铝的表面会形成一层致密的氧化膜;硫酸铝、氯化铝、硝酸铝的溶液均为无色。
【实验探究】为了探究哪一种猜想成立,甲、乙、丙三位同学分别针对猜想一、猜想二、猜想三设计实验方案并展开实验探究。
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一 |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立。R与稀硫酸反应的化学方程式可表示为 |
| 猜想三 | 无明显现象 | 猜想三成立 |
【交流反思】究竟哪种猜想成立?三位同学经讨论交流,发现丙同学在实验前没有打磨铝丝,这可能会导致实验结论错误。于是他们先打磨铝丝,再将其插入到丙同学做实验用过的溶液中,一段时间后,溶液的颜色
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
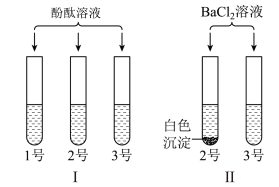
【推荐1】化学实验课上,同学们利用如图装置和步骤鉴别稀硫酸、稀盐酸和碳酸钠三种无色溶液。
步骤Ⅰ:把标有序号1、2、3的三种溶液分别滴入标有对应序号的三支试管中,分别滴加几滴无色酚酞溶液,鉴别出了1号溶液。
步骤Ⅱ:再向另两支试管中分别滴加几滴BaCl2溶液,鉴别出了2号和3号溶液。
(1)步骤Ⅰ中,1号试管中溶液变为红色,可知1号为___________ 溶液(填化学式)。
(2)步骤Ⅱ中,产生白色沉淀的化学方程式是___________ 。
【提出问题】将反应后2号试管内溶液过滤,滤液中的溶质除酚酞外还有什么?
【做出猜想】
(3)猜想一:只有HCl 猜想二:只有BaCl2
猜想三:HCl和BaCl2 猜想四:___________
【讨论交流】
(4)有同学指出猜想___________ 不合理,理由是___________ 。
【设计实验】
(5)以下是部分同学设计的实验方案,最终一定能得出猜想三成立的是___________(填字母)
【反思拓展】
(6)有同学指出,可将上述方案中的一种改进后,也可得出猜想三成立的结论。实验过程中一定能观察到的现象是___________ (填序号)。
①产生气泡 ②实验后溶液变为红色 ③产生白色沉淀
步骤Ⅰ:把标有序号1、2、3的三种溶液分别滴入标有对应序号的三支试管中,分别滴加几滴无色酚酞溶液,鉴别出了1号溶液。
步骤Ⅱ:再向另两支试管中分别滴加几滴BaCl2溶液,鉴别出了2号和3号溶液。
(1)步骤Ⅰ中,1号试管中溶液变为红色,可知1号为
(2)步骤Ⅱ中,产生白色沉淀的化学方程式是
【提出问题】将反应后2号试管内溶液过滤,滤液中的溶质除酚酞外还有什么?
【做出猜想】
(3)猜想一:只有HCl 猜想二:只有BaCl2
猜想三:HCl和BaCl2 猜想四:
【讨论交流】
(4)有同学指出猜想
【设计实验】
(5)以下是部分同学设计的实验方案,最终一定能得出猜想三成立的是___________(填字母)
| A.向滤液中加入少量镁粉 | B.向滤液中加入少量Na2SO4溶液 |
| C.向滤液中加入少量AgNO3溶液 | D.向滤液中加入少量Na2CO3溶液 |
【反思拓展】
(6)有同学指出,可将上述方案中的一种改进后,也可得出猜想三成立的结论。实验过程中一定能观察到的现象是
①产生气泡 ②实验后溶液变为红色 ③产生白色沉淀
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】小红同学在学习“金属的化学性质”实验操作时,发现几支试管中产生气泡的速率有的快有的慢。于是,她与小芳同学一起合作进行如下探究。
【提出问题】金属与酸反应的快慢受哪些因素影响?
【猜想与假设】猜想1:可能与酸的浓度有关 猜想2:可能与金属的种类有关
猜想3:可能与金属的形状有关。
【设计并实验】为了验证猜想,小红和小芳设计如图1所示的装置进行如下实验:
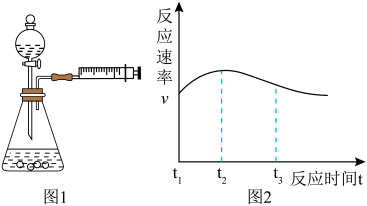
(1)小红和小芳检查图1装置气密性的方法是______ 。
(2)实验时须将镁片和铁片进行打磨,其目的是______ 。
(3)写出镁与稀硫酸反应的化学方程式:______ 。
【收集证据】(4)要比较金属的形状对反应快慢的影响,应选择的实验编号是______ 。
【得出结论】(5)从上述实验数据可得出的结论是______ 。
【评价与反思】(6)测得实验①反应中产生气体的速率(v)与时间(t)的关系如图2所示,t1~t2时间段内反应速率逐渐加快的原因是______ ;t2~t3时间段内反应速率逐渐减慢的主要原因是______ 。
(7)铁与硫酸反应的快慢还受到温度的影响。请你设计实验验证:______ (不要求写出现象和结论)。
【提出问题】金属与酸反应的快慢受哪些因素影响?
【猜想与假设】猜想1:可能与酸的浓度有关 猜想2:可能与金属的种类有关
猜想3:可能与金属的形状有关。
【设计并实验】为了验证猜想,小红和小芳设计如图1所示的装置进行如下实验:

(1)小红和小芳检查图1装置气密性的方法是
(2)实验时须将镁片和铁片进行打磨,其目的是
(3)写出镁与稀硫酸反应的化学方程式:
| 实验编号 | 硫酸的浓度 (均取20mL) | 金属 (均取2g) | 金属的形状 | 收集50mLH2 所需时间/s |
| ① | 10% | 镁 | 粉末状 | 60 |
| ② | 10% | 铁 | 片状 | 120 |
| ③ | 10% | 镁 | 片状 | 102 |
| ④ | 20% | 铁 | 片状 | 110 |
【得出结论】(5)从上述实验数据可得出的结论是
【评价与反思】(6)测得实验①反应中产生气体的速率(v)与时间(t)的关系如图2所示,t1~t2时间段内反应速率逐渐加快的原因是
(7)铁与硫酸反应的快慢还受到温度的影响。请你设计实验验证:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】化学社团的同学在探究金属化学性质时,进行了图1所示的实验。_______ ,铜片表面无明显变化。
实验过程中小强意外发现:当两种金属发生触碰时(如图2),铜片表面产生了气泡。
【提出问题】
图2中铜是否发生了化学反应?产生的气体是什么?
【作出猜想】
(2)同学们对产生的气体进行了以下猜想:
小德猜想是二氧化硫;
小强猜想是氧气;
小美猜想是氢气。
他们作出猜想的理论依据是化学反应前后______ 不变;
【查阅资料】
①将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面产生气体。该反应过程中金属失去的电子通过导线发生了转移。
②二氧化硫能使品红溶液褪色。
【设计并进行实验】
(3)他们设计了图3装置进行实验将产生的气体分别通过导管与图4中的装置连接来验证自己的猜想。
【教师释疑】
图1实验中,锌与稀硫酸反应,锌失去电子,酸溶液中氢离子在锌片表面获得电子生成氢气
【学生感悟】
图3实验中,酸溶液中的氢离子从铜片表面获得锌失去的电子生成了氢气。
【得出结论】
(4)图2中两种金属触碰后铜____ (填“有”或“没有”)发生化学反应。
【延伸应用】
(5)制造钢制船闸门时,为防止铁被腐蚀,常在钢闸门表面安装比铁更活泼的金属。这种金属可以是_______(填字母序号)。
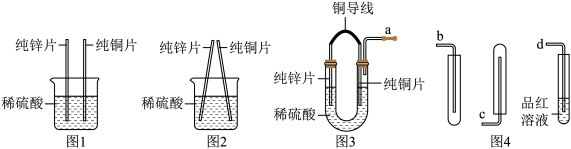
实验过程中小强意外发现:当两种金属发生触碰时(如图2),铜片表面产生了气泡。
【提出问题】
图2中铜是否发生了化学反应?产生的气体是什么?
【作出猜想】
(2)同学们对产生的气体进行了以下猜想:
小德猜想是二氧化硫;
小强猜想是氧气;
小美猜想是氢气。
他们作出猜想的理论依据是化学反应前后
【查阅资料】
①将锌片、铜片用导线连接后平行插入稀硫酸中,铜片表面产生气体。该反应过程中金属失去的电子通过导线发生了转移。
②二氧化硫能使品红溶液褪色。
【设计并进行实验】
(3)他们设计了图3装置进行实验将产生的气体分别通过导管与图4中的装置连接来验证自己的猜想。
| 实验操作 | 实验现象 | 实验结论 | |
| 小德 | 连接导管a与导管d,向品红溶液中通入气体一段时间 | 小美的猜想正确 | |
| 小强 | 选用正确方法收集气体一段时间后,向试管内伸入带火星的木条 | 木条不复燃 | |
| 小美 | 连接导管a与导管 | 气体燃烧,听到轻微的“噗”声 |
【教师释疑】
图1实验中,锌与稀硫酸反应,锌失去电子,酸溶液中氢离子在锌片表面获得电子生成氢气
【学生感悟】
图3实验中,酸溶液中的氢离子从铜片表面获得锌失去的电子生成了氢气。
【得出结论】
(4)图2中两种金属触碰后铜
【延伸应用】
(5)制造钢制船闸门时,为防止铁被腐蚀,常在钢闸门表面安装比铁更活泼的金属。这种金属可以是_______(填字母序号)。
| A.铜 | B.锌 | C.银 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】据统计,我国每年报废的手机超过 1 亿部,若不进行有效回收利用, 会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。

【提出问题】从废旧手机中可以回收到哪些有价值的金属?如何回收?
【查阅资料】
ⅰ.手机电路板中的金属及其价格如下表所示:
说明:Fe、Cu、Al、Ni 的含量用质量分数(%)表示,Au、Ag、Pd 的含量的单位为“g/t”。
ⅱ.Ni的金属活动性位于氢前,Pd的金属活动性位于氢后,NiCl2溶液为绿色。
ⅲ.2Cu+O2+2H2SO4 CuSO4+2H2O
CuSO4+2H2O
【实验方案】
第一步:选择值得回收的金属。
依据资料ⅰ中的数据,废旧手机中有回收价值的金属有 Au、Ag、Cu 、Pd,原因是:①它 们市场价格较高;②_______________ 。
第二步:设计实验分离、回收部分金属。
【问题讨论】
(1)由步骤Ⅰ中的现象,可推知焊锡的物理性质是________ 。
(2)步骤Ⅱ对应的实验现象是____________ 。
(3)步骤Ⅱ所得的溶液中,一定含有的金属元素是________ 。
(4)步骤Ⅴ的操作是__________ 。
【反思交流】
为了确认步骤Ⅳ中滤纸上的金属成分,应进一步查阅的资料为___________________ 。

【提出问题】从废旧手机中可以回收到哪些有价值的金属?如何回收?
【查阅资料】
ⅰ.手机电路板中的金属及其价格如下表所示:
| 种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
| 市场价格($/t ) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
| 矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
| 手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
ⅱ.Ni的金属活动性位于氢前,Pd的金属活动性位于氢后,NiCl2溶液为绿色。
ⅲ.2Cu+O2+2H2SO4
 CuSO4+2H2O
CuSO4+2H2O【实验方案】
第一步:选择值得回收的金属。
依据资料ⅰ中的数据,废旧手机中有回收价值的金属有 Au、Ag、Cu 、Pd,原因是:①它 们市场价格较高;②
第二步:设计实验分离、回收部分金属。
| 序号 | 实验步骤 | 实验现象 |
| I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
| II | 将金属电路放入烧杯中,加入足量稀盐酸浸泡 | _____________ |
| III | 取II中未溶解的电路,用蒸馏水洗净后,放入如右图所示的装置中,进行实验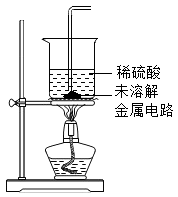 | 溶液逐渐变为蓝色,仍有微量金属固体未溶解 |
| IV | 取III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
| V | _______________ | 得到红色固体 |
(1)由步骤Ⅰ中的现象,可推知焊锡的物理性质是
(2)步骤Ⅱ对应的实验现象是
(3)步骤Ⅱ所得的溶液中,一定含有的金属元素是
(4)步骤Ⅴ的操作是
【反思交流】
为了确认步骤Ⅳ中滤纸上的金属成分,应进一步查阅的资料为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】实验探究是化学学习的重要手段。
(1)兴趣小组1的学生向1~5号小试管中分别滴加少量稀盐酸。
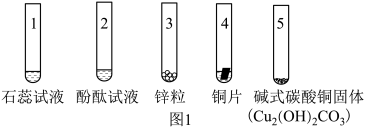
①______ 中溶液变为红色(填“试管1”或“试管2”)。
②试管3中产生气泡,试管4中无明显现象,由此推断金属活动性Cu比Zn______ (填“强”或“弱”)。
③试管5中生成一种盐和两种氧化物,该反应的化学方程式为______ 。
④【小组拓展】
某锌粉含有铜、镁中的一种杂质,取该样品6.5g与足量稀盐酸充分反应,生成氢气0.21g,该锌粉中含有的杂质是______ 。
另取一定量该样品放入硫酸铜溶液中,充分反应后过滤,得到滤渣和滤液。将滤渣洗净,滴入稀硫酸,有气泡产生,则滤液中一定含有的溶质是______
(2)兴趣小组:2的同学们借助传感器对稀NaOH溶液与稀盐酸的中和反应进行研究,实验装置如图2,三颈烧瓶中盛放溶液X
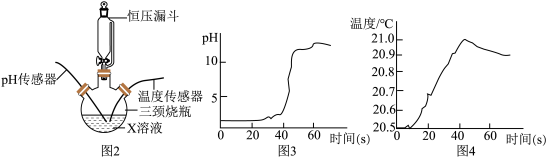
①甲同学用pH传感器测得三颈烧瓶内溶液pH的变化如图3,判断溶液X是______ ,实验进行到60s时溶液中的溶质为______ (填化学式)。
②乙同学用温度传感器测得三颈烧瓶内温度变化如图4(实验过程中热量散失忽略不计),据此可得出反应过程中______ 能量的结论(填“吸收”或“释放”)。
③丙同学提出,通过监测三颈烧瓶内压强变化,也可以推导出乙同学的实验结论,其理由是______
(1)兴趣小组1的学生向1~5号小试管中分别滴加少量稀盐酸。

①
②试管3中产生气泡,试管4中无明显现象,由此推断金属活动性Cu比Zn
③试管5中生成一种盐和两种氧化物,该反应的化学方程式为
④【小组拓展】
某锌粉含有铜、镁中的一种杂质,取该样品6.5g与足量稀盐酸充分反应,生成氢气0.21g,该锌粉中含有的杂质是
另取一定量该样品放入硫酸铜溶液中,充分反应后过滤,得到滤渣和滤液。将滤渣洗净,滴入稀硫酸,有气泡产生,则滤液中一定含有的溶质是
(2)兴趣小组:2的同学们借助传感器对稀NaOH溶液与稀盐酸的中和反应进行研究,实验装置如图2,三颈烧瓶中盛放溶液X

①甲同学用pH传感器测得三颈烧瓶内溶液pH的变化如图3,判断溶液X是
②乙同学用温度传感器测得三颈烧瓶内温度变化如图4(实验过程中热量散失忽略不计),据此可得出反应过程中
③丙同学提出,通过监测三颈烧瓶内压强变化,也可以推导出乙同学的实验结论,其理由是
您最近一年使用:0次
【推荐3】某化学兴趣小组的同学,为了比较金属R与铁、铜的金属活动性强弱,进行如下探究活动
(1)【进行猜想】对三种金属的活动性顺序做出如下猜想:
猜想一:R>Fe>Cu;猜想二_____ ;猜想三:Fe>Cu>R
(2)【收集证据】同学们根据实验仪器和药品,分别用下列两种方案展开实验探究。
(3)【表达与交流】写出铁丝与稀盐酸反应的化学方程式_____ 。
(4)【探究结论】两种实验方案都得出猜想一正确。
【归纳总结】他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与_____ 是否反应。
(3)金属与酸溶液是否反应或反应的剧烈程度。
(5)【拓展应用】利用以下五组试剂验证锌、铜、银三种金属的活动性顺序,从原理上分析可以达到实验目的的有_____ 。
①Cu、ZnSO4溶液、Ag
②稀硫酸、Zn、Cu、AgNO3溶液
③Ag、Zn、CuSO4溶液
④Ag、Zn、Cu、稀硫酸
⑤ZnSO4溶液、 Cu、AgNO3溶液
(1)【进行猜想】对三种金属的活动性顺序做出如下猜想:
猜想一:R>Fe>Cu;猜想二
(2)【收集证据】同学们根据实验仪器和药品,分别用下列两种方案展开实验探究。
| 主要操作 | 主要现象 | 实验结论 | |
| 甲 | (1)将粗细相同打磨好的R丝、铁丝,分别在空气中点燃 | R丝在空气中剧烈燃烧,铁丝在空气中不燃烧 | 金属活动性 |
| (2)将 | 有明显的实验现象出现 | 金属活动性:Fe> Cu | |
| 乙 | 将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中 | R丝产生 | 金属活动性:R>Fe>Cu |
(4)【探究结论】两种实验方案都得出猜想一正确。
【归纳总结】他们总结得出比较金属活动性强弱的常见方法有:
(1)金属与氧气反应的难易和剧烈程度;
(2)金属与
(3)金属与酸溶液是否反应或反应的剧烈程度。
(5)【拓展应用】利用以下五组试剂验证锌、铜、银三种金属的活动性顺序,从原理上分析可以达到实验目的的有
①Cu、ZnSO4溶液、Ag
②稀硫酸、Zn、Cu、AgNO3溶液
③Ag、Zn、CuSO4溶液
④Ag、Zn、Cu、稀硫酸
⑤ZnSO4溶液、 Cu、AgNO3溶液
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐1】金属材料的应用推动了社会发展,人类的生产和生活都离不开金属。
被誉为“中国天眼”的 FAST 是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰(Mn),现探究三种金属的活动性强弱。
【猜想】猜想1:Mn>Fe>Cu 猜想2:Fe>Cu>Mn 猜想3:_______ 。
【实验】
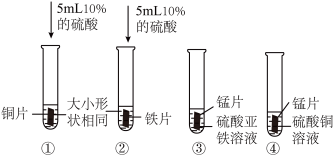
【分析】
(1)请写出实验②中的现象是_______ 。
(2)实验过程中发现只有实验①无明显现象,由此可得出猜想_______ (填“1”“2”或“3”)成立,请写出实验③反应的化学方程式_______ 。(反应后锰元素显+2价)
(3)通过实验现象及分析发现,不需要进行实验____ (填“①”“②”“③”或“④”)就能够得出结论。
被誉为“中国天眼”的 FAST 是目前世界上最大口径、最灵敏的射电望远镜,支撑它的角钢塔架中含有铁、铜、锰(Mn),现探究三种金属的活动性强弱。
【猜想】猜想1:Mn>Fe>Cu 猜想2:Fe>Cu>Mn 猜想3:
【实验】

【分析】
(1)请写出实验②中的现象是
(2)实验过程中发现只有实验①无明显现象,由此可得出猜想
(3)通过实验现象及分析发现,不需要进行实验
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】在实验探究课上,老师给了同学们一包红色粉末,该粉末是铜粉和氧化铁粉中的一种或两种。同学们为了确定该粉末的成分,进行如下探究。请你参与他们的探究并回答问题。
【提出问题】
(1)假设1:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是_________ 。
【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置图如下)。
【进行实验】通过实验及分析,确认假设3成立。
【反思与评价】
(3)①实验过程中,硬质玻璃管内发生的化学反应方程式是___________ 。
②实验时通入一氧化碳片刻后再加热的原因是___________ 。
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是_________ 。
【拓展】
(4)①为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的___________ (填序号)。
A.硝酸铜溶液 B.稀盐酸 C.氯化锌溶液
②请你用另一种反应原理证明猜想3成立,实验方案是___________ 。
【提出问题】
(1)假设1:红色粉末是铜粉;假设2:红色粉末是氧化铁粉;假设3:红色粉末是
【设计实验方案】同学们对实验作了如下设想和分析:取少量红色粉末放入硬质玻璃管中,通入一氧化碳片刻后加热至充分反应(实验装置图如下)。
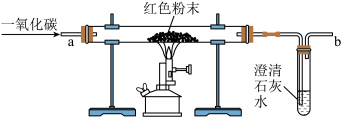
| 实验中可能出现的现象 | 结论 |
| ① | 假设1成立 |
| ②红色粉末全部变黑色,石灰水变浑浊 | 假设2成立 |
| ③ | 假设3成立 |
【进行实验】通过实验及分析,确认假设3成立。
【反思与评价】
(3)①实验过程中,硬质玻璃管内发生的化学反应方程式是
②实验时通入一氧化碳片刻后再加热的原因是
③从环保角度看,上面的实验装置有不足之处,请你对该装置进行改进,具体措施是
【拓展】
(4)①为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的
A.硝酸铜溶液 B.稀盐酸 C.氯化锌溶液
②请你用另一种反应原理证明猜想3成立,实验方案是
您最近一年使用:0次
【推荐3】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;
你的猜想是_______ 。
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因,该原因是_______ 。
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
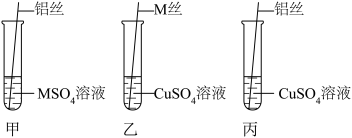
试管乙中观察到的现象是_______ 。
试管丙中反应的化学方程式为_______ 。
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管_______ (填试管编号)中的实验,也可以得出Al>M>Cu的结论。
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;
你的猜想是
【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸);
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:

试管乙中观察到的现象是
试管丙中反应的化学方程式为
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
您最近一年使用:0次



