下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图。
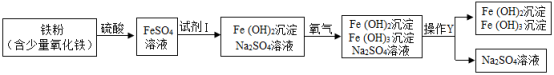
(1)试剂I和操作Y的名称分别为________________ 、___________________ 。
(2)硫酸与氧化铁的反应为__________________________________ 。
(3)往铁粉(含少量氧化铁)中加入硫酸,除铁、氧化铁与硫酸发生反应外,一定还发生其它反应。作出这种判断的依据是_______________________________ 。
(4)某铁矿主要成分为Fe3O4,利用CO将该物质中铁还原出来的方程式为___________ 。

(1)试剂I和操作Y的名称分别为
(2)硫酸与氧化铁的反应为
(3)往铁粉(含少量氧化铁)中加入硫酸,除铁、氧化铁与硫酸发生反应外,一定还发生其它反应。作出这种判断的依据是
(4)某铁矿主要成分为Fe3O4,利用CO将该物质中铁还原出来的方程式为
更新时间:2016-11-27 16:33:14
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】由废铁屑(主要成分为Fe和Fe2O3)制取磁性材料四氧化三铁的主要流程如下:
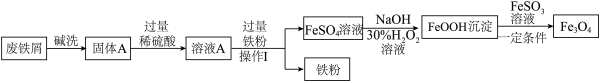
已知:①废铁屑表面含有油污,
②铁与硫酸铁溶液反应的化学方程式为 。
。
(1)碱洗的作用是______ ,操作I的名称是:______ 。
(2)固体A中加入过量稀硫酸发生反应的化学方程式有______ 。
(3)溶液A中加入过量的铁粉,其目的是______ ,涉及的反应类型有______ 种。流程中不选用铁片,而选用铁粉的优点是______ 。
(4)FeOOH与FeSO3溶液在一定条件下反应的化学方程式为: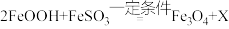 ,则X为
,则X为______ 。

已知:①废铁屑表面含有油污,
②铁与硫酸铁溶液反应的化学方程式为
 。
。(1)碱洗的作用是
(2)固体A中加入过量稀硫酸发生反应的化学方程式有
(3)溶液A中加入过量的铁粉,其目的是
(4)FeOOH与FeSO3溶液在一定条件下反应的化学方程式为:
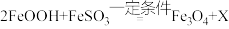 ,则X为
,则X为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐2】人类的生产生活离不开金属。
(1)日常生活用品大多用到了金属材料,现在年产量最高的金属是________ 。
(2)铝制品具有较好的抗腐蚀性能是因为________ (用化学方程式表示)。
(3)现有镁、铁、银的混合物若干放入硫酸铜溶液中,充分反应后过滤,向滤渣中加入稀盐酸,观察到有气泡冒出,则滤渣中一定含有________ 。
(4)现有一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。
①若所加硫酸铜溶液不足,则滤液中一定含有的溶质为________ (填化学式)。
②若所加硫酸铜溶液过量,则该镀锌铁片中铁与锌的质量最简比为________ 。
(1)日常生活用品大多用到了金属材料,现在年产量最高的金属是
(2)铝制品具有较好的抗腐蚀性能是因为
(3)现有镁、铁、银的混合物若干放入硫酸铜溶液中,充分反应后过滤,向滤渣中加入稀盐酸,观察到有气泡冒出,则滤渣中一定含有
(4)现有一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。
①若所加硫酸铜溶液不足,则滤液中一定含有的溶质为
②若所加硫酸铜溶液过量,则该镀锌铁片中铁与锌的质量最简比为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐3】回答下列与金属有关的问题。
(1)在自然条件下,能以单质的形式存在的金属是_________ (填序号);
A.Na B.Fe C.Cu D.Ag E.Au
(2)一定量Fe粉加入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,向滤渣中滴加稀盐酸无明显现象,则下列说法正确的是_________ (填序号):
A.滤渣中一定有Ag,滤液中一定没有AgNO3
B.滤渣中一定有Ag,滤液中一定有Fe(NO3)2
C.滤渣中一定有Ag、Cu,滤液中只有Fe(NO3)2
D.滤渣中一定有Ag、Cu,滤液中一定没有AgNO3和Cu(NO3)2
(3)小明同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬(Cr),好奇的小明想探究Cr、Cu、Fe三种金属的活动性顺序。
【查阅资料】
铬与稀硫酸反应,生成蓝色硫酸亚铬(CrSO4)溶液: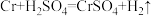 。
。
【设计并完成实验】
①Cr片放入FeSO4溶液中,溶液由浅绿色变成蓝色;
②Cu片放入CrSO4溶液中,无明显现象;
③Fe片放入稀H2SO4中,产生气泡溶液变成浅绿色。
不需要做的实验是_________ (填序号)。
【实验结论】
Cr、Cu、Fe三种金属的活动性,由强到弱的顺序为_________ 。
【知识运用】
将Cr片放入AgNO3溶液中,如果能发生反应,写出反应方程式,如果不能发生反应,说明理由_____ 。
(1)在自然条件下,能以单质的形式存在的金属是
A.Na B.Fe C.Cu D.Ag E.Au
(2)一定量Fe粉加入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,向滤渣中滴加稀盐酸无明显现象,则下列说法正确的是
A.滤渣中一定有Ag,滤液中一定没有AgNO3
B.滤渣中一定有Ag,滤液中一定有Fe(NO3)2
C.滤渣中一定有Ag、Cu,滤液中只有Fe(NO3)2
D.滤渣中一定有Ag、Cu,滤液中一定没有AgNO3和Cu(NO3)2
(3)小明同学家新换了水龙头,从说明书上了解到该水龙头是铜质镀铬(Cr),好奇的小明想探究Cr、Cu、Fe三种金属的活动性顺序。
【查阅资料】
铬与稀硫酸反应,生成蓝色硫酸亚铬(CrSO4)溶液:
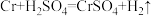 。
。【设计并完成实验】
①Cr片放入FeSO4溶液中,溶液由浅绿色变成蓝色;
②Cu片放入CrSO4溶液中,无明显现象;
③Fe片放入稀H2SO4中,产生气泡溶液变成浅绿色。
不需要做的实验是
【实验结论】
Cr、Cu、Fe三种金属的活动性,由强到弱的顺序为
【知识运用】
将Cr片放入AgNO3溶液中,如果能发生反应,写出反应方程式,如果不能发生反应,说明理由
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐1】有人用经过粉碎的含有较多有机物杂质的粗铜,通过下列步骤制取硫酸铜晶体
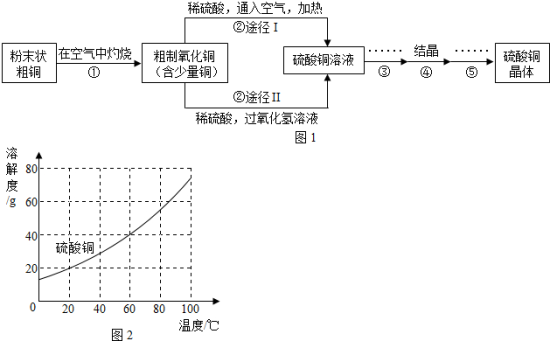
(1)若步骤①中灼烧温度过高会产生副产物氧化亚铜(铜的化合价为+1价),其化学式为_____ 。
(2)写出步骤②中氧化铜与稀硫酸反应的化学方程式:_____ 。
(3)步骤②中,铜和稀硫酸不能直接发生置换反应的原因是______ 。
(4)反应途径Ⅰ和Ⅱ,分别发生如下反应:
途径Ⅰ:2Cu+O2+2H2SO4 2CuSO4+2H2O
2CuSO4+2H2O
途径Ⅱ:Cu+H2O2+ H2SO4=CuSO4+2H2O
请选择你认为更适合于实际应用的途径,并说明理由:_____ 。
(5)根据图2,步骤④的结晶方法为_______ 。
(6)若800kg粗制氧化铜(其中单质铜的质量分数为4%),通过途径Ⅱ转化为硫酸铜,计算参加反应的过氧化氢的质量____ 。写出计算过程。

(1)若步骤①中灼烧温度过高会产生副产物氧化亚铜(铜的化合价为+1价),其化学式为
(2)写出步骤②中氧化铜与稀硫酸反应的化学方程式:
(3)步骤②中,铜和稀硫酸不能直接发生置换反应的原因是
(4)反应途径Ⅰ和Ⅱ,分别发生如下反应:
途径Ⅰ:2Cu+O2+2H2SO4
 2CuSO4+2H2O
2CuSO4+2H2O途径Ⅱ:Cu+H2O2+ H2SO4=CuSO4+2H2O
请选择你认为更适合于实际应用的途径,并说明理由:
(5)根据图2,步骤④的结晶方法为
(6)若800kg粗制氧化铜(其中单质铜的质量分数为4%),通过途径Ⅱ转化为硫酸铜,计算参加反应的过氧化氢的质量
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
名校
解题方法
【推荐2】你玩过塔积木的游戏吗?小明用六块积木A-F,分别对应碳酸钠、铁、硫酸、二氧化碳、氢氧化钙、氯化钡。按照“物质能反应,积木就能叠靠在一起,不反应积木就不接触”的原则搭成如图所示形状。
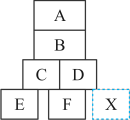
已知E的物质类别与其他五种不同。请回答下列问题:
(1)写出物质的化学式:A_____ ;E_____ 。
(2)B与C反应的化学方程式为:_____ 。
(3)B-F的叠放组合中,能反应的复分解反应共有_____ 个。
(4)小美认为加一块积木X可以更稳定,X的名称是_____ (不能重复A-F中的物质)。

已知E的物质类别与其他五种不同。请回答下列问题:
(1)写出物质的化学式:A
(2)B与C反应的化学方程式为:
(3)B-F的叠放组合中,能反应的复分解反应共有
(4)小美认为加一块积木X可以更稳定,X的名称是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】氯化钡是一种可溶性重金属盐,广泛应用于化工领域。工业上以重晶石(主要成分BaSO4,杂质为Fe2O3)为原料,通过下列流程生成氯化钡晶体(BaCl2·xH2O)。
已知:①
②CaO、BaO都能与水反应生成碱
③钡离子是重金属离子,有毒
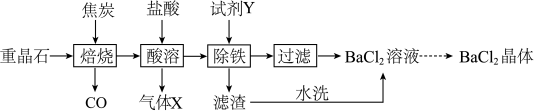
(1)焙烧时,焦炭与杂质Fe2O3发生反应的化学方程式为____________ ;
(2)气体X的成分除H2S和少量挥发出的HCl、水蒸气外,还含有____________ 。
(3)除铁反应中,试剂Y可以是___________ (填字母)
a NaOH溶液 b 氨水 c 生石灰 d BaO固体
证明铁已除尽的方法是:取上层清液于试管中,____________ 。
(4)对滤渣进行水洗的目的是提高晶体产率和____________ 。
已知:①

②CaO、BaO都能与水反应生成碱
③钡离子是重金属离子,有毒

(1)焙烧时,焦炭与杂质Fe2O3发生反应的化学方程式为
(2)气体X的成分除H2S和少量挥发出的HCl、水蒸气外,还含有
(3)除铁反应中,试剂Y可以是
a NaOH溶液 b 氨水 c 生石灰 d BaO固体
证明铁已除尽的方法是:取上层清液于试管中,
(4)对滤渣进行水洗的目的是提高晶体产率和
您最近一年使用:0次
【推荐1】制盐在我国有着悠久的历史。某粗盐中主要含有NaCl、Na2SO4及少量MgSO4和CaSO4,为获取NaCl和Na2SO4,取样品溶于水得到溶液A,进行如图实验:______ g。_______ 。
(3)Ⅲ中加入过量稀盐酸的目的是_______ 。
(4)将“溶液D”在80℃时蒸发浓缩,有少量固体析出。
NaCl和Na2SO4在不同温度下的溶解度:
①经检验,少量固体是纯净的Na2SO4。分析NaCl不析出的原因是______ 。
②停止蒸发浓缩,降温至10℃并过滤,得到大量固体及母液。设计实验检验所得固体中是否含有NaCl:_______ 。从母液中获得NaCl固体的方法是_______ 。

(3)Ⅲ中加入过量稀盐酸的目的是
(4)将“溶液D”在80℃时蒸发浓缩,有少量固体析出。
NaCl和Na2SO4在不同温度下的溶解度:
| 温度/℃ | 10 | 40 | 80 | |
| 溶解度(g/100g水) | NaCl | 35.8 | 36.6 | 38.4 |
| Na2SO4 | 9.1 | 48.8 | 43.7 | |
②停止蒸发浓缩,降温至10℃并过滤,得到大量固体及母液。设计实验检验所得固体中是否含有NaCl:
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】有一包固体粉末样品M,可能含氧化铜、氧化铝、钢、铝、碳中的一种或几种。为探究样品M的组成,某化学兴趣小组进行了如下图所示实验(部分生成物已省略)。
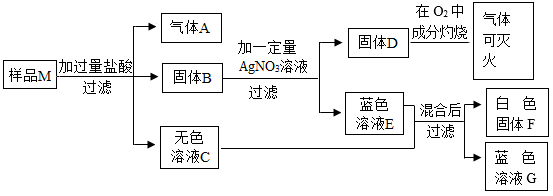
(1)气体是_____ 。
(2)向固体B中加入硝酸银溶液,发生反应的化学方程式为_____ 。
(3)样品M中可确定的物质为_____ (填化学式,下同)。
(4)蓝色溶液G中一定含有大量的阴离子为_____ 。

(1)气体是
(2)向固体B中加入硝酸银溶液,发生反应的化学方程式为
(3)样品M中可确定的物质为
(4)蓝色溶液G中一定含有大量的阴离子为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】氧化镁在医药等行业应用广泛。实验室以菱镁矿(主要成分为MgCO3,含少量FeCO3和SiO2等)为原料制备高纯氧化镁的实验流程如下:
查阅资料:①MgCO3、FeCO3的化学性质和CaCO3相似均能与酸发生类似反应
②SiO2不溶于水和酸
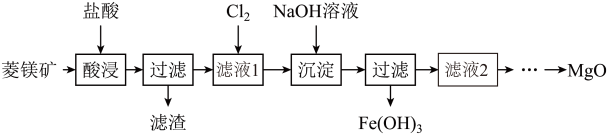
(1)酸浸过程中发生主要反应的化学方程式为________________ 。
(2)通入C12,将FeCl2转化为FeCl3,该反应属于基本反应类型中的______________ 反应。
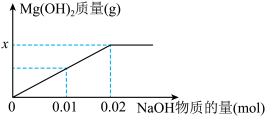
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是_______________ 。
(4)“滤液2”中的溶质主要是MgCl2和_______________ 。
查阅资料:①MgCO3、FeCO3的化学性质和CaCO3相似均能与酸发生类似反应
②SiO2不溶于水和酸

(1)酸浸过程中发生主要反应的化学方程式为
(2)通入C12,将FeCl2转化为FeCl3,该反应属于基本反应类型中的
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是
(4)“滤液2”中的溶质主要是MgCl2和
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】实验室中有两瓶失去标签的无色溶液,已知是氢氧化钠溶液和碳酸钠溶液中的各一种,小明和小刚想用化学方法鉴别两瓶溶液,进行了如下实验探究。
(1)①小明分别取少量两种待测溶液于A、B两支试管中,分别滴加适稀硝酸,振荡,观察到A试管中的现象是______ ,则A试管中的溶液为碳酸钠溶液。
②小刚从下列四种试剂中选取了一种试剂,也成功鉴别了上述两种无色溶液,则小刚所选的试剂是______ (选填字母序号之一)。
A.酚酞试液 B.Fe2O3粉末 C.CaCl2 溶液 D.NaCl溶液
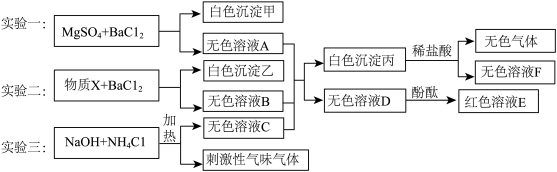
(2)某同学欲探究固体混合物A的成分,已知A中可能含有NH4Cl、NH4NO3、Cu(NO3)2、BaCO3中的两种或多种,按下图所示进行探究实验,出现的现象如图中所述。(设过程中所发生的反应都恰好完全反应)
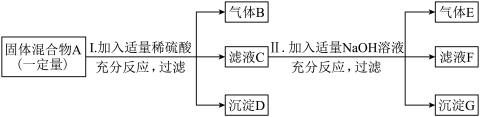
①气体E的化学式为______ ,沉淀D的化学式为______ 。
②在固体混合物A里,上述四种物质中肯定存在的物质是______ (填化学式)。
③写出步骤Ⅱ中生成沉淀G时,一定发生的化学反应方程式______ 。
④根据上述实验现象推断,在固体混合物A里,上述四种物质中,还不能确定存在的物质是______ (填化学式),为进一步确定其是否存在,可取少量滤液F再进行实验。请简要说明实验操作步骤、发生的现象及结论______ 。
(1)①小明分别取少量两种待测溶液于A、B两支试管中,分别滴加适稀硝酸,振荡,观察到A试管中的现象是
②小刚从下列四种试剂中选取了一种试剂,也成功鉴别了上述两种无色溶液,则小刚所选的试剂是
A.酚酞试液 B.Fe2O3粉末 C.CaCl2 溶液 D.NaCl溶液
(2)某同学欲探究固体混合物A的成分,已知A中可能含有NH4Cl、NH4NO3、Cu(NO3)2、BaCO3中的两种或多种,按下图所示进行探究实验,出现的现象如图中所述。(设过程中所发生的反应都恰好完全反应)

①气体E的化学式为
②在固体混合物A里,上述四种物质中肯定存在的物质是
③写出步骤Ⅱ中生成沉淀G时,一定发生的化学反应方程式
④根据上述实验现象推断,在固体混合物A里,上述四种物质中,还不能确定存在的物质是
您最近一年使用:0次
【推荐2】从天然盐井水中获取的粗盐中含有泥沙、氯化镁、硫酸钠和氯化钙等杂质。为得到精盐,某兴趣小组设计如下实验:【提示】杂质含量较少,不考虑微溶物形成沉淀。
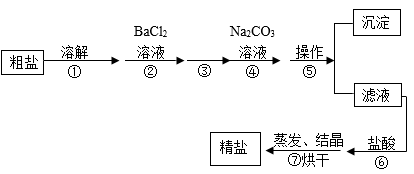
(1)步骤⑤操作的名称是___________ ,步骤③加入试剂一定不可能是___________ 。
a.氢氧化钙溶液 b.氢氧化钾溶液 c.氢氧化钡溶液
(2)请设计实验来验证滤液中含有氢氧化钠(写出实验步骤和现象)______

(1)步骤⑤操作的名称是
a.氢氧化钙溶液 b.氢氧化钾溶液 c.氢氧化钡溶液
(2)请设计实验来验证滤液中含有氢氧化钠(写出实验步骤和现象)
您最近一年使用:0次