某化学小组发现一袋包装破损的漂白粉,同学们对其漂白作用是否失效产生了疑问。
【查阅资料】漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应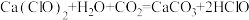 ,HClO能使有色物质如品红溶液褪色。HClO不稳定,易分解生成HCl和O2。
,HClO能使有色物质如品红溶液褪色。HClO不稳定,易分解生成HCl和O2。
【实验探究】
【继续探究】同学们对失效后的漂白粉的成分很感兴趣,并作进一步探究。在老师的帮助下,同学们对失效后的漂白粉成分进行猜想,猜想一:CaCl2和CaCO3;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和CaCO3和Ca(OH)2。
【查阅资料】漂白粉的主要成分是Ca(ClO)2、CaCl2和Ca(OH)2,其有效成分是Ca(ClO)2。Ca(ClO)2可溶于水,漂白原理是:它在空气中发生反应
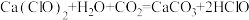 ,HClO能使有色物质如品红溶液褪色。HClO不稳定,易分解生成HCl和O2。
,HClO能使有色物质如品红溶液褪色。HClO不稳定,易分解生成HCl和O2。【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 把少量漂白粉样品加入水中,通入足量的CO2气体, | 漂白粉的漂白作用已失效。 |
【继续探究】同学们对失效后的漂白粉的成分很感兴趣,并作进一步探究。在老师的帮助下,同学们对失效后的漂白粉成分进行猜想,猜想一:CaCl2和CaCO3;猜想二:CaCl2和Ca(OH)2;猜想三:CaCl2和CaCO3和Ca(OH)2。
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:把样品加入水中,充分溶解后过滤, | 有气泡产生。 | 猜想一成立。 |
| 步骤二: |
2017九年级下·江苏·专题练习 查看更多[2]
更新时间:2016-11-27 16:33:15
|
相似题推荐
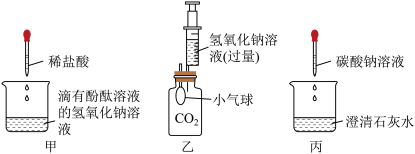
【推荐1】学习小组同学用如图所示实验探究完碱的化学性质后,将甲、乙、丙中的无色溶液倒入到一个洁净的废液缸,发现废液明显变浑浊且呈红色。同学们很好奇,于是接着进行了下列的拓展学习与探究。
【反思交流】
(1)小组同学做甲图所示实验时,当溶液恰好由红色变为无色,即停止了滴加稀盐酸,写出发生反应的化学方程式:____________________ 。做乙图所示实验时,看到的现象是____________________ 。
(2)废液呈红色,说明废液显__________ 性。废液变浑浊,是因为倾倒前丙中的溶液含有__________ (填化学式)。
【拓展问题】使废液变成红色的物质是什么?
【做出猜想】猜想一:只有NaCO3;
猜想二:只有NaOH;
猜想三:NaOH和Ca(OH)2;
猜想四:NaOH和Na2CO3;
(3)你认为以上猜想中,不合理的是猜想__________ 。
【查阅资料】CaCl2溶液呈中性。
【验证猜想】
(4)静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成,写出该反应的化学方程式____________________ 。静置后,发现试管中的上层清液仍为红色,由此证明了猜想__________ 成立。

【反思交流】
(1)小组同学做甲图所示实验时,当溶液恰好由红色变为无色,即停止了滴加稀盐酸,写出发生反应的化学方程式:
(2)废液呈红色,说明废液显
【拓展问题】使废液变成红色的物质是什么?
【做出猜想】猜想一:只有NaCO3;
猜想二:只有NaOH;
猜想三:NaOH和Ca(OH)2;
猜想四:NaOH和Na2CO3;
(3)你认为以上猜想中,不合理的是猜想
【查阅资料】CaCl2溶液呈中性。
【验证猜想】
(4)静置一段时间后,取少量废液缸中的上层红色清液于试管中,加入过量CaCl2溶液,有白色沉淀生成,写出该反应的化学方程式
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
【推荐2】某化学兴趣小组学习碱的性质后,到实验室做实验.小明将二氧化碳通入氢氧化钠溶液后无明显现象,然后向得到的溶液中滴加CaCl2溶液,产生白色沉淀;小杰做的实验和小明一样,但没有出现白色沉淀.他们为了查明原因,查阅资料:①CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CO2+H2O=2NaHCO3;②Ca(HCO3)2溶于水,溶液呈碱性;③CaCl2溶液呈中性:④Na2CO3、NaHCO3溶液都呈碱性,都能与酸反应;⑤铝、锌、铁、铜的盐溶液与NaHCO3溶液混合会产生沉淀.
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3; 猜想②NaHCO3;
猜想③Na2CO3、NaOH; 猜想④_____________________ .
【实验探究】
【继续探究】将4.0gNaOH固体溶解在100mL水中,然后通入4.0g二氧化碳气体,充分反应后,所得溶液的溶质是___________ .
他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3; 猜想②NaHCO3;
猜想③Na2CO3、NaOH; 猜想④
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| (1)取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡;再加入 | 无明显现象;有气泡产生. | 猜想②成立,反应的化学方程式 |
| (2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤,取滤液于另一支试管中,滴加 | 产生白色沉淀; | 猜想③成立 |
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】某同学参加实验操作考查的题目是:鉴别稀硫酸,稀盐酸和氢氧化钠三种无色溶液。该同学进行了如下操作:把标有序号1、2、3的三种溶液分别滴入标有对应序号的三支试管中,向三支试管中滴加酚酞试液,鉴别出1号溶液;再向另两支试管中滴加BaCl2溶液,观察到2号试管中有白色沉淀生成。
请回答:
(1)1号试管中是______ 溶液。
(2)2号试管发生化学反应的实质是BaCl2溶液中的Ba2+和2号溶液中的______ (填微粒符号)结合生成白色沉淀______ 。该反应的化学方程式为______ ,把该试管反应后的物质进行过滤,得到滤液。
【提出问题】除含有酚酞外,滤液中溶质的成分是什么?
【猜想假设】猜想一:HCl;猜想二:HCl和______ (填化学式);猜想三:HCl和BaCl2。
【进行实验】①取一定量的滤液于试管中,向试管中滴加Na2SO4溶液,有白色沉淀生成,猜想______ 正确。
②为了验证该滤液的酸碱性,将一片pH试纸放在干燥的玻璃片上,用______ 蘸取该滤液,滴到试纸上,立即将试纸显示的颜色与pH标准比色卡进行对照,读出pH=5。
【交流拓展】2号试管中滤液显酸性,要将该滤液调至中性,可向滤液中加入适量______ (填序号)。
A.铁粉 B.氯化钙溶液 C.石灰石
请回答:
(1)1号试管中是
(2)2号试管发生化学反应的实质是BaCl2溶液中的Ba2+和2号溶液中的
【提出问题】除含有酚酞外,滤液中溶质的成分是什么?
【猜想假设】猜想一:HCl;猜想二:HCl和
【进行实验】①取一定量的滤液于试管中,向试管中滴加Na2SO4溶液,有白色沉淀生成,猜想
②为了验证该滤液的酸碱性,将一片pH试纸放在干燥的玻璃片上,用
【交流拓展】2号试管中滤液显酸性,要将该滤液调至中性,可向滤液中加入适量
A.铁粉 B.氯化钙溶液 C.石灰石
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】碳酸钠、碳酸氢钠是我们初中化学中两种常见的碳酸盐,它们与酸反应的情形非常相似。两者与酸反应有区别吗?老师通过控制变量法设计几组探究实验,进行探究。
(1)【实验1】:同时将足量的稀盐酸倒入锥形瓶甲和锥形瓶乙中(如下图)。
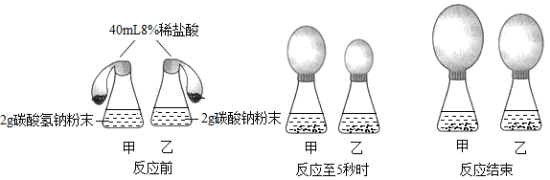
请写出碳酸氢钠和盐酸反应的化学方程式________ ;为探究其反应速率,可根据______ (选填“反应至5秒时”或“反应结束”)产生的二氧化碳的量来判断。
(2)【实验2】:在两个锥形瓶中分别加入2g碳酸钠粉末,然后向其中一个锥形瓶中倒入20mL的蒸馏水,向另一个锥形瓶中倒入20mL质量分数15%的稀盐酸(足量),利用温度传感器测定其温度变化(如图a)。另取2g碳酸氢钠粉末,重复上述实验(如图b)。

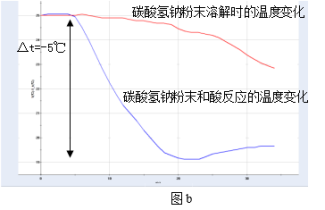
从温度曲线看,碳酸氢钠粉末溶于水及与酸反应过程中,___________ (选填“吸收”或“放出”)热量。
(3)两种粉末状固体溶于水及与酸反应过程的能量变化,对它们与酸的反应速率___________ (填“有”或“无”)较大影响。
(4)该实验中,与稀盐酸反应结束产生的二氧化碳的量:Na2CO3___________ NaHCO3(选填“>”、“<”或“=”)
(5)【实验3】:分别将极稀的盐酸逐滴滴入试管甲和试管乙中,边滴边振荡。
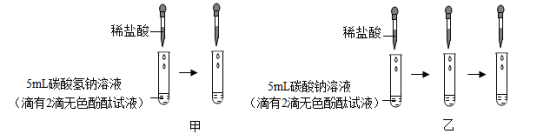
现象为:①试管甲中的溶液开始时显浅红色,逐滴滴入稀盐酸立即有气泡产生,浅红色逐渐消失。②试管乙中的溶液开始时显红色,滴入稀盐酸没有气泡产生,溶液颜色逐渐变为浅红色后,继续滴加稀盐酸有气泡产生,浅红色逐渐消失。

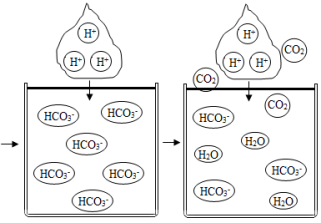
【反思】在【实验3】碳酸钠溶液中逐滴滴入稀盐酸,为何刚开始没有气泡产生?研究小组查阅资料,绘制出微观示意图。
①结合图示,用化学方程式解释刚开始没有气泡的原因___________ 。
②相同浓度的碳酸氢钠溶液和碳酸钠溶液的碱性:碳酸氢钠__ 碳酸钠(选填“>”、“<”或“=”)。
(1)【实验1】:同时将足量的稀盐酸倒入锥形瓶甲和锥形瓶乙中(如下图)。

请写出碳酸氢钠和盐酸反应的化学方程式
(2)【实验2】:在两个锥形瓶中分别加入2g碳酸钠粉末,然后向其中一个锥形瓶中倒入20mL的蒸馏水,向另一个锥形瓶中倒入20mL质量分数15%的稀盐酸(足量),利用温度传感器测定其温度变化(如图a)。另取2g碳酸氢钠粉末,重复上述实验(如图b)。


从温度曲线看,碳酸氢钠粉末溶于水及与酸反应过程中,
(3)两种粉末状固体溶于水及与酸反应过程的能量变化,对它们与酸的反应速率
(4)该实验中,与稀盐酸反应结束产生的二氧化碳的量:Na2CO3
(5)【实验3】:分别将极稀的盐酸逐滴滴入试管甲和试管乙中,边滴边振荡。

现象为:①试管甲中的溶液开始时显浅红色,逐滴滴入稀盐酸立即有气泡产生,浅红色逐渐消失。②试管乙中的溶液开始时显红色,滴入稀盐酸没有气泡产生,溶液颜色逐渐变为浅红色后,继续滴加稀盐酸有气泡产生,浅红色逐渐消失。


【反思】在【实验3】碳酸钠溶液中逐滴滴入稀盐酸,为何刚开始没有气泡产生?研究小组查阅资料,绘制出微观示意图。
①结合图示,用化学方程式解释刚开始没有气泡的原因
②相同浓度的碳酸氢钠溶液和碳酸钠溶液的碱性:碳酸氢钠
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究。
【查阅资料】白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3 ·yCaCO3。(杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一、定性探究:白云石粉的成分和性质
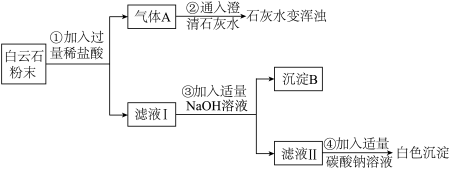
【实验分析】
(1)由步骤①②的现象可得出白云石粉中一定含有的离子是____________ (填离子符号)。
(2)步骤③生成氢氧化镁的化学方程式是________________________________ 。该反应属于 ______ (填写化学反应基本类型)。
(3)滤液Ⅱ中的溶质是_________________________ 。
【结 论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成。
【实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究。
二、定量探究:白云石的组成
【查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸镁与碳酸钙的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解。
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:
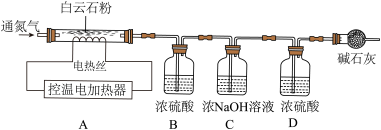
【实验步骤】①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量。
实验数据记录如下表:
【实验分析和数据处理】
(4)装置D的作用是______________ ;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是_______________ 。
(6)计算白云石中碳酸镁的质量分数。(写出计算过程):_______________ 。
(7)设计实验证明白云石粉已完全分解的实验方法是_____________________________ (写出实验方法、现象)
(8)白云石(xMgCO3 ·yCaCO3)中的 x:y=___________ (最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值 ________ (填偏大、偏小或不变)。
【查阅资料】白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3 ·yCaCO3。(杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一、定性探究:白云石粉的成分和性质

【实验分析】
(1)由步骤①②的现象可得出白云石粉中一定含有的离子是
(2)步骤③生成氢氧化镁的化学方程式是
(3)滤液Ⅱ中的溶质是
【结 论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成。
【实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究。
二、定量探究:白云石的组成
【查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸镁与碳酸钙的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解。
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量。
实验数据记录如下表:
| B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | |
| 反应前 | 50.0 | 100.0 | 50.0 |
| 700℃ | 50.0 | 102.1 | 50.1 |
| 1000℃ | 50.0 | 106.3 | 50.3 |
(4)装置D的作用是
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是
(6)计算白云石中碳酸镁的质量分数。(写出计算过程):
(7)设计实验证明白云石粉已完全分解的实验方法是
(8)白云石(xMgCO3 ·yCaCO3)中的 x:y=
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】小红同学用碳酸氢钠作为膨松剂蒸馒头时,发现蒸热后的馒头有气孔,但膨松效果一般;在妈妈的建议下,小红在使用碳酸氢钠的同时加入一定量的食醋,蒸熟后的馒头膨松效果就理想多了,小红对碳酸氢钠作为膨松剂的作用原理进行探究。
【提出问题】碳酸氢钠作为膨松剂的作用原理是什么?
【查阅资料】膨松剂是在食品加工过程中加入的,因产生气体,能使面胚发起形成多孔组织,从而使食品具有松软或酥脆特点的一类物质,化学膨松剂中通常含有碳酸氢钠。
【做出猜想】小红同学对用碳酸氢钠在两次制作馒头过程中的作用原理做出猜想:
猜想一:______ 。
猜想二:______ 。
【方案设计与实施】
小红同学分别对猜想一和猜想二设计了实验方案并实施验证。
试剂和用品:碳酸氢钠、稀盐酸、澄清石灰水 仪器和其他用品自选
仪器和其他用品自选
【解释与结论】①依据小红同学对碳酸氢钠作为膨松剂的作用原理的实验探究,获得碳酸氢钠的两个化学性质是______ 、______  用化学方程式表示
用化学方程式表示 。
。
②在有酸性物质存在时,碳酸氢钠作用效果会更好的原因是______ 。
【评价与反思】①小红妈妈制作馒头时,在面团发酵后,常加入少量纯碱来调节面团的酸度。小红提出:能不能单独使用纯碱做膨松剂?要解决该问题需要设计实验验证纯碱是否具有______ 的性质。
②市售膨松剂大多是复合膨松剂,一般由三类物质组成:碳酸氢钠、酸性物质、助剂 淀粉等
淀粉等 。结合上述探究,下列关于复合膨松剂的说法中,不正确的是
。结合上述探究,下列关于复合膨松剂的说法中,不正确的是______  填序号
填序号 。
。
a 复合膨松剂保存时要注意防潮
b 复合膨松剂在加水揉面与蒸馒头的过程中均起到发面的作用
c 使用复合膨松剂前必须先将面进行发酵
d 在蒸馒头时复合膨松剂中助剂的作用可能是调节气体产生的速率

【提出问题】碳酸氢钠作为膨松剂的作用原理是什么?
【查阅资料】膨松剂是在食品加工过程中加入的,因产生气体,能使面胚发起形成多孔组织,从而使食品具有松软或酥脆特点的一类物质,化学膨松剂中通常含有碳酸氢钠。
【做出猜想】小红同学对用碳酸氢钠在两次制作馒头过程中的作用原理做出猜想:
猜想一:
猜想二:
【方案设计与实施】
小红同学分别对猜想一和猜想二设计了实验方案并实施验证。
试剂和用品:碳酸氢钠、稀盐酸、澄清石灰水
 仪器和其他用品自选
仪器和其他用品自选
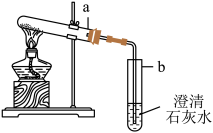
| 实验方案 | 实验现象 | 结论 | |
| 实验一 | 如图,取一定量碳酸氢钠于试管a中,加热,将产生的气体通入澄清石灰水中 | 试管a内壁有小液滴,导管口有气泡冒出,澄清石灰水变浑浊 | 猜想一正确 |
| 实验二 | 猜想二正确 |
【解释与结论】①依据小红同学对碳酸氢钠作为膨松剂的作用原理的实验探究,获得碳酸氢钠的两个化学性质是
 用化学方程式表示
用化学方程式表示 。
。②在有酸性物质存在时,碳酸氢钠作用效果会更好的原因是
【评价与反思】①小红妈妈制作馒头时,在面团发酵后,常加入少量纯碱来调节面团的酸度。小红提出:能不能单独使用纯碱做膨松剂?要解决该问题需要设计实验验证纯碱是否具有
②市售膨松剂大多是复合膨松剂,一般由三类物质组成:碳酸氢钠、酸性物质、助剂
 淀粉等
淀粉等 。结合上述探究,下列关于复合膨松剂的说法中,不正确的是
。结合上述探究,下列关于复合膨松剂的说法中,不正确的是 填序号
填序号 。
。a 复合膨松剂保存时要注意防潮
b 复合膨松剂在加水揉面与蒸馒头的过程中均起到发面的作用
c 使用复合膨松剂前必须先将面进行发酵
d 在蒸馒头时复合膨松剂中助剂的作用可能是调节气体产生的速率
您最近一年使用:0次
科学探究题
|
较难
(0.4)
真题
解题方法
【推荐1】在七十五届联合国大会上,中国提出努力争取2060年前实现“碳中和”,实现二氧化碳的“零排放”。化学兴趣小组认为实验室可用氢氧化钠溶液吸收多余的二氧化碳,从而实现实验室二氧化碳的“零排放”。小组同学对吸收后溶液中溶质的成分产生兴趣并进行探究。
【提出问题】 氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是什么?
【查阅资料】
(1)CO2与NaOH溶液反应会生成Na2CO3,当二氧化碳过量时,会继续反应生成NaHCO3。
(2)NaHCO3溶液呈弱碱性,一般不与CaCl2溶液反应,与稀盐酸反应产生气体。
(3)CaCl2溶液呈中性。
【作出猜想】
猜想①NaOH、Na2CO3 猜想②Na2CO3 猜想③Na2CO3、NaHCO3 猜想④NaHCO3
【实验与结论】
写出步骤一中反应的化学方程式___________ 。
【反思与交流】
反应物的量不同,可能导致生成物的种类不同。
【提出问题】 氢氧化钠溶液吸收二氧化碳气体后,溶液中溶质的成分是什么?
【查阅资料】
(1)CO2与NaOH溶液反应会生成Na2CO3,当二氧化碳过量时,会继续反应生成NaHCO3。
(2)NaHCO3溶液呈弱碱性,一般不与CaCl2溶液反应,与稀盐酸反应产生气体。
(3)CaCl2溶液呈中性。
【作出猜想】
猜想①NaOH、Na2CO3 猜想②Na2CO3 猜想③Na2CO3、NaHCO3 猜想④NaHCO3
【实验与结论】
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取少量待测液于试管中,加入CaCl2溶液 | 产生白色沉淀 | 猜想 |
| 步骤二:另取少量待测液于试管中,加入过量CaCl2溶液至不再产生沉淀,过滤,取少量滤液,向其中加入适量稀盐酸 | (填“有”或“无”) | 猜想③不成立 |
| 步骤三:另取步骤二的少量滤液,向其中滴入2~3滴无色酚酞试液 | 试液变红 | 猜想 |
【反思与交流】
反应物的量不同,可能导致生成物的种类不同。
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】在做酸碱中和反应的实验时,某同学向盛有NaOH溶液的烧杯中加入一定量的稀硫酸后没有明显现象。同学们产生疑问:反应后溶液中的溶质是什么呢?对此同学们展开了以下实验探究。
[假设猜想]同学们给出了以下的猜想:
①只有NaSO4;②有 Na2SO4和H2SO4;③有______________ ;④有Na2SO4、H2SO4和NaOH。
你认为以上猜想中肯定不成立的是______________ (填序号)。
[实验探究]为了探究其余的猜想,同学们做了如下的实验:
(1)李明同学取少量烧杯中的溶液于试管中,向其中滴加几滴无色酚酞溶液,没有明显变化,则原溶液中一定没有______________ 。
(2)张华也取少量样品溶液,向其中加入少量的碳酸钠溶液,发现立即有大量的气泡产生,产生气泡的化学反应方程式为______________ ,该现象可证明猜想②是正确的。
(3)李明又说,用Fe2O3固体同样也可以探究出猜想②是正确的,请你帮他写出具体的实验操作和现象:______________ 。
(4)受同学们的启发,小丽说用pH试纸也可以探究溶液成分,于是她用如图所示的方法测定该溶液的pH,结果小于7,也证明猜想②是正确的。但她的这种错误操作会产生的后果是______________ 。

(5)小刚说:“老师说过硫酸也可以和BaCl2溶液反应,生成硫酸钡白色沉淀,所以我们也可以用BaCl2溶液来探究。”于是他取少量样品溶液于试管中,向其中滴加几滴无色的BaCl2溶液,观察到产生白色沉淀,所以他证明猜想②是正确的。请问,小刚的结论是否正确,为什么?______________________________ 。
[得出结论]反应后的溶液中溶质是硫酸钠和硫酸。
[评价反思]在确定溶液中存在某物质时,要根据该物质性质来进行探究。我们已知物质的结构决定性质,之所以能选用以上步骤(2) 到步骤(4)方案进行验证,都与溶液中存在的微粒____________ (填符号)有关。
[假设猜想]同学们给出了以下的猜想:
①只有NaSO4;②有 Na2SO4和H2SO4;③有
你认为以上猜想中肯定不成立的是
[实验探究]为了探究其余的猜想,同学们做了如下的实验:
(1)李明同学取少量烧杯中的溶液于试管中,向其中滴加几滴无色酚酞溶液,没有明显变化,则原溶液中一定没有
(2)张华也取少量样品溶液,向其中加入少量的碳酸钠溶液,发现立即有大量的气泡产生,产生气泡的化学反应方程式为
(3)李明又说,用Fe2O3固体同样也可以探究出猜想②是正确的,请你帮他写出具体的实验操作和现象:
(4)受同学们的启发,小丽说用pH试纸也可以探究溶液成分,于是她用如图所示的方法测定该溶液的pH,结果小于7,也证明猜想②是正确的。但她的这种错误操作会产生的后果是

(5)小刚说:“老师说过硫酸也可以和BaCl2溶液反应,生成硫酸钡白色沉淀,所以我们也可以用BaCl2溶液来探究。”于是他取少量样品溶液于试管中,向其中滴加几滴无色的BaCl2溶液,观察到产生白色沉淀,所以他证明猜想②是正确的。请问,小刚的结论是否正确,为什么?
[得出结论]反应后的溶液中溶质是硫酸钠和硫酸。
[评价反思]在确定溶液中存在某物质时,要根据该物质性质来进行探究。我们已知物质的结构决定性质,之所以能选用以上步骤(2) 到步骤(4)方案进行验证,都与溶液中存在的微粒
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐3】某化学兴趣小组在实验室里用如图所示的电解器进行水的探究。(电解器的气密性非常好)
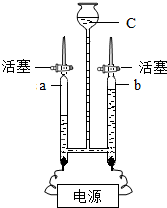
【提出问题】为什么水分子中氢、氧原子个数比为2∶1?
【探究课题】假设水的化学式为HxOy,测定x∶y的值。
【实验探究】
(1)电解水11分钟后赶出水中溶解的气体,同时测定电解过程中a、b管中气体在标准状况下的体积,相关数据记录在下表中:
(2)确定b管中气体成分。实验如下:
【实验分析】
(1)电解器玻璃管a中的电极连电源的______ 极(填“正”、“负”)。电解器中的液体为很稀的硫酸钠溶液,此处硫酸钠的作用为______ ,硫酸钠的化学式为______ 。
(2)写出电解时反应的化学方程式______ 。
(3)分析上表中的数据可知:电解开始阶段a管收集到的气体与b管收集到的气体体积比明显偏大,可能的原因是______ 。
【探究结论】
查阅资料可知:在标准状况下,氢气的密度是0.089 g/L,氧气的密度是1.429 g/L。利用有关数据及假设的化学式,列出x与y的关系式:______ (仅列式,不要求出结果)。求解可得出x ∶y的值约为2:1。

【提出问题】为什么水分子中氢、氧原子个数比为2∶1?
【探究课题】假设水的化学式为HxOy,测定x∶y的值。
【实验探究】
(1)电解水11分钟后赶出水中溶解的气体,同时测定电解过程中a、b管中气体在标准状况下的体积,相关数据记录在下表中:
| 时间/min(或操作) | 2 | 4 | 6 | 9 | 11 | 赶出水中溶解的气体 |
| a管中气体体积/mL | 12 | 29 | 49 | 79 | 99 | 100 |
| b管中气体体积/mL | 4 | 11 | 21 | 36 | 46 | 50 |
(2)确定b管中气体成分。实验如下:
| 实验操作 | 实验现象 | 结 论 |
【实验分析】
(1)电解器玻璃管a中的电极连电源的
(2)写出电解时反应的化学方程式
(3)分析上表中的数据可知:电解开始阶段a管收集到的气体与b管收集到的气体体积比明显偏大,可能的原因是
【探究结论】
查阅资料可知:在标准状况下,氢气的密度是0.089 g/L,氧气的密度是1.429 g/L。利用有关数据及假设的化学式,列出x与y的关系式:
您最近一年使用:0次



