(1)以下数据是白云区梓元岗中学2018届初三学生参加广州市“我与化学”的研究成果《不同干燥剂的吸水效果对比》。请同学们分析实验数据:
①计算含杂质20%的10g 生石灰能吸收水_____ g.(保留一位小数)
②生石灰在第4天后吸水效果_____ ,硅胶在第4天后吸水效果_____ 。
(2)为探究NaHCO3(固体50℃以上开始逐渐分解)析出的最佳条件,完成了几组实验:
①在反应时间相同情况下,35℃时NaHCO3产率比40℃时高的原因是_____ 。
②表格中X的数值可能为_____ 。
A85.8 B86.8 C92.1 D93.1
③由实验数据可知,能够得到最多NaHCO3的条件是_____ ℃和_____ min。
| 时间 干燥剂 | 第1天 | 第4天 | 第7天 | 第10天 |
| 生石灰质量g | 20.00 | 23.02 | 24.90 | 25.45 |
| 硅胶质量g | 20.00 | 24.17 | 24.69 | 24.72 |
①计算含杂质20%的10g 生石灰能吸收水
②生石灰在第4天后吸水效果
(2)为探究NaHCO3(固体50℃以上开始逐渐分解)析出的最佳条件,完成了几组实验:
| 实验序号 | 反应温度/℃ | 反应时间/min | NaHCO3产率/% |
| a | 30 | 60 | 86.8 |
| b | 30 | 120 | X |
| c | 35 | 60 | 89.4 |
| d | 35 | 120 | 92.5 |
| e | 40 | 60 | 85.3 |
| f | 40 | 120 | 85.6 |
①在反应时间相同情况下,35℃时NaHCO3产率比40℃时高的原因是
②表格中X的数值可能为
A85.8 B86.8 C92.1 D93.1
③由实验数据可知,能够得到最多NaHCO3的条件是
更新时间:2019-09-26 23:15:41
|
相似题推荐
实验题
|
较难
(0.4)
解题方法
【推荐1】以下是在实验室制取气体时常用的仪器,回答下列问题。

(1)标号为 E 的仪器名称是________________ ;
(2)用分解过氧化氢的方法制取 O2,并用排水法收集:
①组装制取装置时,需选择如图中的 A、D、H、L、M、N、O 和________________ (填序号);
②当________________ 时开始收集氧气才纯净;
(3)实验室制取二氧化碳:
①用向上排空气法收集二氧化碳,验满的方法是_______________ ;
②欲制得 6.6g CO2,可用稀盐酸与足量的_____________ 充分反应;设稀盐酸中 HCl 的质量为 x,根据化学方程式,列出 HCl 和 CO2质量关系的比例式_______________ ;
③通过②计算可分析,理论上需要用溶质质量分数为 10%的稀盐酸______________ g。

(1)标号为 E 的仪器名称是
(2)用分解过氧化氢的方法制取 O2,并用排水法收集:
①组装制取装置时,需选择如图中的 A、D、H、L、M、N、O 和
②当
(3)实验室制取二氧化碳:
①用向上排空气法收集二氧化碳,验满的方法是
②欲制得 6.6g CO2,可用稀盐酸与足量的
③通过②计算可分析,理论上需要用溶质质量分数为 10%的稀盐酸
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐2】氧化铜与氢气在加热的条件下可反应生成铜和水。实验室采用氢气还原氧化铜的方法,测定某氧化铜样品中氧化铜的质量分数(杂质不与氢气反应),设计了实验Ⅰ和Ⅱ、回答下列问题:
Ⅰ、制取氢气
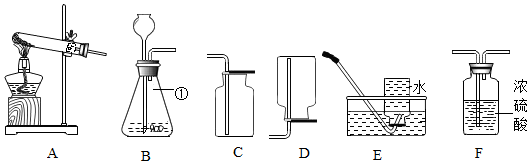
(1)写出仪器①的名称:______ 。
(2)若用锌粒与稀硫酸制取一瓶干燥 的氢气,装置的合理的连接顺序为:______ ,发生反应的化学方程式为______ 。
(3)B装置可用作实验室制取氧气,发生反应的化学方程式为______ 。
Ⅱ、测定成分
按下图连接好甲、乙装置(玻璃管中有 9 g 氧化铜样品)。实验开始时,应先通入氢气,过一会再加热。当使反应物充分反应后停止加热,待装置冷却后再停止通入氢气。反应前后称量甲、乙装置中的物质的质量如下表:
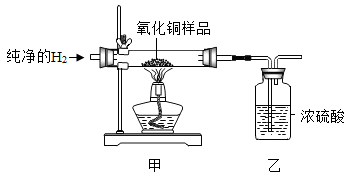
(4)加热前应先通入氢气的目的______ ,反应时甲中观察到的现象为______ ,
(5)请根据甲装置中固体质量在反应前后的变化,计算出样品中氧化铜的质量分数______ (结果保留一位小数),若利用乙装置中液体质量进行计算,会使测定的结果偏大,导致这一现象的原因可能是______ 。
Ⅰ、制取氢气

(1)写出仪器①的名称:
(2)若用锌粒与稀硫酸制取一瓶
(3)B装置可用作实验室制取氧气,发生反应的化学方程式为
Ⅱ、测定成分
按下图连接好甲、乙装置(玻璃管中有 9 g 氧化铜样品)。实验开始时,应先通入氢气,过一会再加热。当使反应物充分反应后停止加热,待装置冷却后再停止通入氢气。反应前后称量甲、乙装置中的物质的质量如下表:

| 质量 | 反应前 | 反应后 |
| 甲装置中固体的质量/g | 9 | 7.4 |
| 乙装置中液体的质量/g | 110.0 | 111.8 |
(5)请根据甲装置中固体质量在反应前后的变化,计算出样品中氧化铜的质量分数
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐3】同学们对一包干燥的红色粉末氧化铁的含量进行测定。请你参与并回答有关问题。称取该粉末5.0g装入硬质玻璃管中,按下图在通风橱中进行实验。开始时缓缓通入CO气体,过一段时间后再加热使其充分反应。待反应完全后,停止加热,继续通CO气体至玻璃管冷却。反应前后称量相关装置和物质的总质量,其数据如下表(假定粉末中的杂质不参加反应,也不发生变化):

【交流讨论】
(1)开始实验时,在A装置中应_____ (选序号“a.先通CO,排尽空气”“b.先加热红色粉末”)。
(2)选择①组的实验数据计算来确定红色粉末中氧化铁的质量分数是_____ %,造成②组洗气瓶和瓶中物质的总质量增加量过小的原因是(写一点) _____ 。
(3)实验中观察到A装置反应管中的现象为_____ 。
(4)为了防止溶液倒吸,本实验停止加热前_____ (填“需要”或“不需要”)先断开A和B的连接处。本实验中,为达到测定氧化铁含量的目的,可以用 _____ 代替CO气体。
【反思评价】从环保角度看,该实验装置设计上不足之处是_____ 。

| 反应前 | 反应后 | |
| ①组 | 玻璃管和红色粉末的总质量为37.5g | 玻璃管和固体物质的总质量为36.3g |
| ②组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为180.1g |
(1)开始实验时,在A装置中应
(2)选择①组的实验数据计算来确定红色粉末中氧化铁的质量分数是
(3)实验中观察到A装置反应管中的现象为
(4)为了防止溶液倒吸,本实验停止加热前
【反思评价】从环保角度看,该实验装置设计上不足之处是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐1】如图为某同学设计的探究分子特征的实验装置,已知:浓氨水显碱性,易挥发出氨气.氨气具有刺激性气味,酚酞遇碱溶液会变红.请按要求完成系列问题:
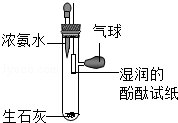
(1)滴入适量浓氨水后,观察到酚酞试纸______________ ,说明分子是______________ .
(2)放入少量生石灰的作用是______________ .
(3)装置中气球的作用是______________ .

(1)滴入适量浓氨水后,观察到酚酞试纸
(2)放入少量生石灰的作用是
(3)装置中气球的作用是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐2】结合下图多角度研究水。

(1)探究生石灰与水反应:如图进行实验观察到的现象是______ 。
(2)探究燃烧条件:该实验中水的作用是______ 。
(3)排水法收集H2:原因是______ 。
(4)电解水:实验说明水是由______ 组成的;反应的化学方程式为______ ;
(5)水在高温下也可分解,高温下分解体系中微粒含量与温度的关系如下图所示:

结合图中曲线,水开始分解的温度大约是______ ℃;A对应的微粒是______ (填符号)。

(1)探究生石灰与水反应:如图进行实验观察到的现象是
(2)探究燃烧条件:该实验中水的作用是
(3)排水法收集H2:原因是
(4)电解水:实验说明水是由
(5)水在高温下也可分解,高温下分解体系中微粒含量与温度的关系如下图所示:

结合图中曲线,水开始分解的温度大约是
您最近一年使用:0次
实验题
|
较难
(0.4)
解题方法
【推荐3】为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),某兴趣小组的同学进行了如下的实验,请你参与过程分析。

【查阅资料】
1 草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4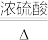 CO2↑+CO↑+H2O;
CO2↑+CO↑+H2O;
2 碱石灰主要成分为生石灰与氢氧化钠固体。
【实验设计及操作】用如图所示装置进行实验。
【问题讨论】
(1)实验中观察到E中现象是___________ ;
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是___________ (填序号);
①浓硫酸、石灰水、氢氧化钠溶液
②石灰水、氢氧化钠溶液、浓硫酸
③氢氧化钠溶液、石灰水、浓硫酸
(3)当E中固体完全反应后,先熄灭___________ 处酒精灯(填“A”或“E”);
(4)G的作用是___________ ;
(5)实验装置有一明显缺陷是___________ 。
【数据处理】(6)称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g.则样品中氧化铁质量分数为___________ (精确到0.1%)。
【实验反思】(7)当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数___________ (填“偏大”、“偏小”或“无影响”)。

【查阅资料】
1 草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为H2C2O4
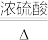 CO2↑+CO↑+H2O;
CO2↑+CO↑+H2O;2 碱石灰主要成分为生石灰与氢氧化钠固体。
【实验设计及操作】用如图所示装置进行实验。
【问题讨论】
(1)实验中观察到E中现象是
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是
①浓硫酸、石灰水、氢氧化钠溶液
②石灰水、氢氧化钠溶液、浓硫酸
③氢氧化钠溶液、石灰水、浓硫酸
(3)当E中固体完全反应后,先熄灭
(4)G的作用是
(5)实验装置有一明显缺陷是
【数据处理】(6)称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g.则样品中氧化铁质量分数为
【实验反思】(7)当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数
您最近一年使用:0次



