“84”消毒液、H2O2溶液都是常用消毒剂,兴趣小组对两种消毒剂进行了如下探究活动。
【查阅资料】“84”消毒液的有效成分是次氯酸钠(化学式为NaClO)。
【实验1】取少量“84”消毒液于试管中,滴加H2O2溶液,发现有大量气泡产生;然后______ (填写实验操作和现象),证明产生的气体是氧气。
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】
猜想一:作反应物,NaClO与H2O2溶液发生化学反应;
猜想二:作______ ,类似分解H2O2溶液制氧气时MnO2的作用。
【实验2】
(1)按如图所示组装实验装置,并_______ 。
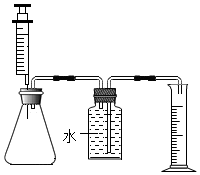
(2)向锥形瓶中加入30mL“84”消毒液,注射器中吸入25mL H2O2溶液,集气瓶中装满水,量筒中无液体。
(3)将注射器中的H2O2溶液平均分5次推入锥形瓶中:每次推入H2O2溶液,待不再产生气泡后,记录收集气体的总体积(忽略温度变化对测量结果造成的影响)见下表。
①表中的数据x=______ ,y=_______ 。
②分析表中数据得出“猜想一正确”,其依据是______ 。
【分析讨论】 NaClO与H2O2溶液反应除生成氧气外,还生成氯化钠和水,该反应的化学方程式为_______ 。
【查阅资料】“84”消毒液的有效成分是次氯酸钠(化学式为NaClO)。
【实验1】取少量“84”消毒液于试管中,滴加H2O2溶液,发现有大量气泡产生;然后
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】
猜想一:作反应物,NaClO与H2O2溶液发生化学反应;
猜想二:作
【实验2】
(1)按如图所示组装实验装置,并

(2)向锥形瓶中加入30mL“84”消毒液,注射器中吸入25mL H2O2溶液,集气瓶中装满水,量筒中无液体。
(3)将注射器中的H2O2溶液平均分5次推入锥形瓶中:每次推入H2O2溶液,待不再产生气泡后,记录收集气体的总体积(忽略温度变化对测量结果造成的影响)见下表。
| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 量筒收集到水的总体积/mL | 140 | 280 | 365 | x | 375 |
| 加入H2O2溶液的体积/mL | 5 | 5 | 5 | 5 | 5 |
| 实际收集气体的总体积/mL | 135 | 270 | 350 | y | 350 |
①表中的数据x=
②分析表中数据得出“猜想一正确”,其依据是
【分析讨论】 NaClO与H2O2溶液反应除生成氧气外,还生成氯化钠和水,该反应的化学方程式为
更新时间:2023-03-10 00:53:14
|
相似题推荐
【推荐1】研究和控制化学反应条件有重要意义。
(1)某化学兴趣小组同学在学习了催化剂的知识后,对红砖粉末也能催化过氧化氢分解产生了探究兴趣。
【查阅资料】红砖的主要成分是粘土(主要是硅酸盐)和氧化铁,其颜色来自于氧化铁(红棕色粉末).
【提出猜想】氧化铁也能作过氧化氢分解的催化剂
【设计实验】兴趣小组的同学设计了下列三组实验(其它可能影响实验的因素均忽略)
(1)写出实验②所发生反应的文字(或化学式)表达式____________________ 。
(2)表中的待测数据是指____________________ 。
(3)对比实验____ 和____ (填实验序号)的待测数据可以看出,氧化铁能加快过氧化氢的分解速率。
(4)将实验②反应后的混合物过滤、洗涤、干燥,称量得到1.5g红棕色粉末,说明__________ 。
(5)再将该红棕色粉末放入试管,进行实验,说明氧化铁的_________ 在反应前后没有发生变化。
【预期结论】氧化铁也可以作为过氧化氢分解的催化剂。
【评价设计】你认为小组同学设计实验③和实验②对比的目的是_____________
(1)某化学兴趣小组同学在学习了催化剂的知识后,对红砖粉末也能催化过氧化氢分解产生了探究兴趣。
【查阅资料】红砖的主要成分是粘土(主要是硅酸盐)和氧化铁,其颜色来自于氧化铁(红棕色粉末).
【提出猜想】氧化铁也能作过氧化氢分解的催化剂
【设计实验】兴趣小组的同学设计了下列三组实验(其它可能影响实验的因素均忽略)
| 实验序号 | 5%过氧化氢溶液的体积 | 其他物质的质量 | 待测数据 |
| ① | 5mL | 无 | |
| ② | 5mL | 1.5g氧化铁 | |
| ③ | 5mL | 1.5g二氧化锰 |
(1)写出实验②所发生反应的文字(或化学式)表达式
(2)表中的待测数据是指
(3)对比实验
(4)将实验②反应后的混合物过滤、洗涤、干燥,称量得到1.5g红棕色粉末,说明
(5)再将该红棕色粉末放入试管,进行实验,说明氧化铁的
【预期结论】氧化铁也可以作为过氧化氢分解的催化剂。
【评价设计】你认为小组同学设计实验③和实验②对比的目的是
您最近一年使用:0次
【推荐2】某兴趣小组对氧气的实验室制取进行了一些探究,请你积极参与,并回答相关问题:
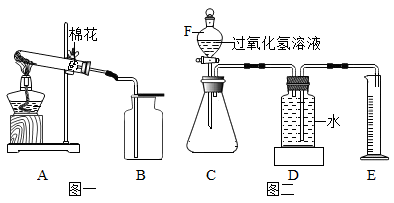
(1)按图一制取氧气,试管中发生反应的文字表达式为_____ ,试管口塞一团棉花的作用是_____ ,判断氧气是否收集满的方法是_______ 。
(2)通过学习,小组同学了解到除二氧化锰外,还有些物质也可促进过氧化氢分解的速率,为此小组同学进一步开展探究:
【提出问题】氧化铜能加快过氧化氢分解的速率吗?
【查阅资料】氧化铜是黑色粉末难溶于水。
【设计实验】利用图二装置进行实验:
【实验分析】①实验中“待记录的量”可能是_______ ;
②三次实验均加入15mL浓度为5%的过氧化氢溶液,其目的是_______ ;
③小威提出,实验时若D中未充满水,是否会对实验结论产生影响?请说出你的观点和理由:____ ;
④设计对比实验②③的目的是_______ 。
【结论】氧化铜可以加快过氧化氢分解的速率,但相同条件下,氧化铜的促进效果不如二氧化锰。
【反思】如果要证明氧化铜是过氧化氢分解的催化剂,还必需补充实验,验证_______ 。

(1)按图一制取氧气,试管中发生反应的文字表达式为
(2)通过学习,小组同学了解到除二氧化锰外,还有些物质也可促进过氧化氢分解的速率,为此小组同学进一步开展探究:
【提出问题】氧化铜能加快过氧化氢分解的速率吗?
【查阅资料】氧化铜是黑色粉末难溶于水。
【设计实验】利用图二装置进行实验:
| 序号 | 操作 | 待记录的量 |
| ① | 将仪器F中15mL浓度为5%的过氧化氢溶液加入仪器C中 | |
| ② | 仪器C中先加入2g氧化铜,再将仪器F中15mL浓度为5%的过氧化氢溶液加入仪器C中 | |
| ③ | 仪器C中先加入2g二氧化锰,再将仪器F中15mL浓度为5%的过氧化氢溶液加仪器C中 |
【实验分析】①实验中“待记录的量”可能是
②三次实验均加入15mL浓度为5%的过氧化氢溶液,其目的是
③小威提出,实验时若D中未充满水,是否会对实验结论产生影响?请说出你的观点和理由:
④设计对比实验②③的目的是
【结论】氧化铜可以加快过氧化氢分解的速率,但相同条件下,氧化铜的促进效果不如二氧化锰。
【反思】如果要证明氧化铜是过氧化氢分解的催化剂,还必需补充实验,验证
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】化学兴趣小组为了探究影响过氧化氢分解速率的因素,设计了实验装置并进行了气体的制取实验。实验时均以生成40 mL气体为标准,相关实验数据记录如下表:
【分析数据】
(1)通过实验______ 与③对比可知,其他条件相同时,过氧化氢溶液的浓度越大,分解速率越快;
(2)通过实验①与④对比可知,过氧化氢的分解速率与温度的关系是______ ;
(3)通过实验①与②对比可知,加入二氧化锰后,过氧化氢的分解速率加快了:若要证明二氧化锰是该反应的催化剂,还需要证明它在化学反应前后的质量和______ 没有发生变化。
(4)实验证明二氧化锰确实可以作过氧化氢分解反应的催化剂,请写出反应的化学符号表达式:______ 。
| 实验序号 | 过氧化氢溶液 浓度/% | 过氧化氢溶液 体积/mL | 过氧化氢溶液 温度/℃ | 二氧化锰 质量/g | 收集 40 mL气体 所用时间/s |
| ① | 5 | 10 | 20 | 0 | 128 |
| ② | 5 | 10 | 20 | 0.5 | 28 |
| ③ | 15 | 10 | 20 | 0.5 | 10 |
| ④ | 5 | 10 | 50 | 0 | 55 |
(1)通过实验
(2)通过实验①与④对比可知,过氧化氢的分解速率与温度的关系是
(3)通过实验①与②对比可知,加入二氧化锰后,过氧化氢的分解速率加快了:若要证明二氧化锰是该反应的催化剂,还需要证明它在化学反应前后的质量和
(4)实验证明二氧化锰确实可以作过氧化氢分解反应的催化剂,请写出反应的化学符号表达式:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】如图所示,超市的洗涤用品区域有一种叫做“污渍爆炸盐”的新型洗涤剂,能清除衣服上难以清洗的黄斑、血渍、奶渍等。某化学兴趣小组的同学对“污渍爆炸盐”与水作用后的产物进行了探究。

(1)查阅资料:“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4),它是白色结晶颗粒,与水作用会产生碳酸盐和其他化合物。
(2)小明猜想其他化合物为:Ⅰ.NaOH;Ⅱ.H2O2;Ⅲ.NaOH和H2O2,小明作出以上猜想的理论依据是_____ 。
(3)实验设计:探究“污渍爆炸盐”水溶液的成分完成下列表格。
(4)实验结论:猜想Ⅱ正确。
写出过碳酸钠与水反应的化学方程式_____ 。

(1)查阅资料:“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4),它是白色结晶颗粒,与水作用会产生碳酸盐和其他化合物。
(2)小明猜想其他化合物为:Ⅰ.NaOH;Ⅱ.H2O2;Ⅲ.NaOH和H2O2,小明作出以上猜想的理论依据是
(3)实验设计:探究“污渍爆炸盐”水溶液的成分完成下列表格。
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤1:取少量“污渍爆炸盐”于烧杯中,加入足 量蒸馏水,充分搅拌。 | 固体完全溶解,形成无色溶液 | / |
| 步骤2:取少量步骤1形成的溶液于试管中,再加入足量氯化钙溶液。 | 含有Na2CO3 | |
| 步骤3:取少量步骤2试管中的上层清液于另一支 试管中,再滴加少量MgCl2溶液,振荡。 | 无明显现象 | |
| 步骤4:另取一支试管,加入少量步骤1形成的溶 液,再加入少量二氧化锰,将带火星木条伸入试管中。 | 带火星的木条复燃 | 含有H2O2 |
(4)实验结论:猜想Ⅱ正确。
写出过碳酸钠与水反应的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】焦炭与水蒸气在高温下反应,产物是一种俗称水煤气的气体燃料(其中不含甲烷),为确定水煤气的成分,某实验小组进行了如下探究:
【查阅资料】新鲜的鸡血遇一氧化碳变为樱桃红色。
【提出猜想】
小组成员对水煤气的成分提出以下四种猜想:
猜想1:H2、CO2;
猜想2:H2、CO;
猜想3:CO、CO2;
猜想4:H2、CO、CO2。
请你说明猜想3不能成立的理由:__________ 。
【实验探究】小组设计了下图所示的实验装置进行探究。
【实验现象】通入水煤气后,澄清石灰水不变浑浊,新鲜鸡血变樱桃红色。
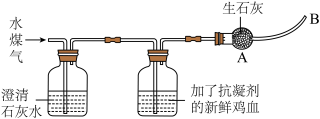
(1)由此可知,水煤气中不含__________ ,含有__________ 。(填化学式)。
【继续实验】在B处点燃气体,然后用一个干冷的烧杯罩在火焰上方。
(1)气体通过A后再在B处点燃时,观察到火焰呈__________ 色,所罩烧杯的内壁__________ ,由此证明水煤气中含有H2,猜想__________ 成立。
(2)由探究结果可知,焦炭与水蒸气在高温下反应的化学方程式为_____________ 。
【查阅资料】新鲜的鸡血遇一氧化碳变为樱桃红色。
【提出猜想】
小组成员对水煤气的成分提出以下四种猜想:
猜想1:H2、CO2;
猜想2:H2、CO;
猜想3:CO、CO2;
猜想4:H2、CO、CO2。
请你说明猜想3不能成立的理由:
【实验探究】小组设计了下图所示的实验装置进行探究。
【实验现象】通入水煤气后,澄清石灰水不变浑浊,新鲜鸡血变樱桃红色。

(1)由此可知,水煤气中不含
【继续实验】在B处点燃气体,然后用一个干冷的烧杯罩在火焰上方。
(1)气体通过A后再在B处点燃时,观察到火焰呈
(2)由探究结果可知,焦炭与水蒸气在高温下反应的化学方程式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组在一个充满O2的密闭容器中加入一定量的纯净的碳粉,在高温条件下使其充分燃烧反应,待反应结束后,容器中的碳粉已完全消失。该小组对容器中反应后的气体进行如下探究:
[阅读资料]①氢氧化钠可以吸收并除去二氧化碳气体;②浓硫酸能吸水,可做气体干燥剂。
[知识回顾]碳充分燃烧生成CO2,不充分燃烧生成CO
[提出猜想](1)小红对容器中气体的组成提出如下四种猜想,你认为其中明显不合理的有______ (填字母)。
A 可能是SO2 B 可能是CO C 可能是CO2 D 可能是CO2和O2的混合气体
(2)小明认为碳粉部分充分燃烧,还有部分没有充分燃烧,容器中的气体还可能是CO和CO2的混合气体;
[实验探究1]小明为了验证自己的猜想,按如下图所示装置进行探究。
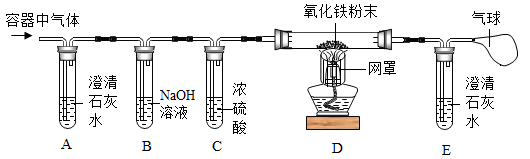
请回答下列问题:
①小明的实验设计思路:装置A的作用是______ ,A中发生反应的化学方程式是______ 。
②若原气体中含有CO气体,小明可观察到D玻璃管中的实验现象是______ ,E中气球作用是______ 。
[实验探究2]小强认为容器中的气体是CO2和O2的混合气体,并进行实验改进和探究。小强把小明实验中的氧化铁换成了铜丝网,并去掉E装置进行验证。若小强的猜想成立,则装置D中的铜丝网的变化现象是______ ,发生反应的化学方程式是______ 。
[反思交流]有同学认为,小强应先通入容器中气体一段时间再加热, 目的是______ 。
[阅读资料]①氢氧化钠可以吸收并除去二氧化碳气体;②浓硫酸能吸水,可做气体干燥剂。
[知识回顾]碳充分燃烧生成CO2,不充分燃烧生成CO
[提出猜想](1)小红对容器中气体的组成提出如下四种猜想,你认为其中明显不合理的有
A 可能是SO2 B 可能是CO C 可能是CO2 D 可能是CO2和O2的混合气体
(2)小明认为碳粉部分充分燃烧,还有部分没有充分燃烧,容器中的气体还可能是CO和CO2的混合气体;
[实验探究1]小明为了验证自己的猜想,按如下图所示装置进行探究。

请回答下列问题:
①小明的实验设计思路:装置A的作用是
②若原气体中含有CO气体,小明可观察到D玻璃管中的实验现象是
[实验探究2]小强认为容器中的气体是CO2和O2的混合气体,并进行实验改进和探究。小强把小明实验中的氧化铁换成了铜丝网,并去掉E装置进行验证。若小强的猜想成立,则装置D中的铜丝网的变化现象是
[反思交流]有同学认为,小强应先通入容器中气体一段时间再加热, 目的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】小峰同学在体育课上腿部擦伤,医务室大夫在他伤口上涂了医用过氧化氢溶液,小峰看到伤口处产生了小气泡,很好奇。为什么瓶中的过氧化氢溶液涂到伤口上,分解就加快了呢?
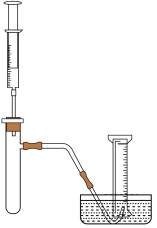
I.小峰准备用如下图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录两分钟收集的气体体积。
(1)请写出实验室用过氧化氢制取氧气的化学方程式_________ 。
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到_________ ,说明生成的气体是氧气。
Ⅱ.小峰查阅了相关资料,并进行了探究实验。
【查阅资料】
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【实验1】分两次进行实验,均注入5mL过氧化氢溶液,第一次在常温下进行,第二次将试管浸在_________ ℃的水中。量筒中2分钟收集到的气体体积均为5mL。得出结论:_________ 。
【实验2】分两次进行实验,第一次操作为_________ ,量筒中2分钟收集到的气体体积为5mL;第二次将装有一小粒过氧化氢酶的试管浸在37℃的温水中,注入5mL过氧化氢溶液,量筒中2分钟收集到的气体体积为_________ (选填“大于”“小于”或“等于”)5mL。得出结论:过氧化氢分解加快是因为过氧化氢酶的作用。
【实验反思】小峰反思课实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
通过这些数据,我们能得出的新结论是:温度不影响过氧化氢的分解速率,但是影响过氧化氢酶的分解效果;当其他条件都相同时,_________ ℃,过氧化氢酶的催化效果更好。
I.小峰准备用如下图所示装置测定过氧化氢分解的快慢,实验前在注射器中吸入过氧化氢溶液,量筒内装满水。实验开始时,向试管中注入过氧化氢溶液,并用排水法收集氧气。记录两分钟收集的气体体积。

(1)请写出实验室用过氧化氢制取氧气的化学方程式
(2)若要检验生成的气体是否为氧气,可将导气管从水中取出,取带火星的木条放在导气管口处,观察到
Ⅱ.小峰查阅了相关资料,并进行了探究实验。
【查阅资料】
①过氧化氢是人体代谢废物之一,它能够对机体造成损害,人体存在过氧化氢酶,可以催化过氧化氢分解。
②温度对化学反应的快慢有影响,人体正常体温是37℃。
【提出猜想】
猜想1:过氧化氢分解加快是因为体温比瓶中的温度高。
猜想2:过氧化氢分解加快是因为伤口中有过氧化氢酶。
【实验1】分两次进行实验,均注入5mL过氧化氢溶液,第一次在常温下进行,第二次将试管浸在
【实验2】分两次进行实验,第一次操作为
【实验反思】小峰反思课实验过程,认为人体中过氧化氢酶是在体温条件下发挥作用的,实验得出的结论可能存在不足。因此又补充进行了几组实验,数据记录如下表所示。
| 加入过氧化氢酶 | 不加过氧化氢酶 | |||||
| 反应温度/℃ | 25 | 37 | 42 | 25 | 37 | 42 |
| 收集到气体体积/mL | 39 | 56 | 34 | 5 | 5 | 5 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。三个小组均采用如图装置进行实验,记录收集10mL氧气的时间,实验室可供选择的试剂有:2.5%、5%、10%三种浓度的过氧化氢溶液、二氧化锰粉末、氧化铜粉末、红砖粉末。
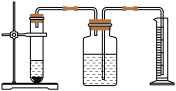
【装置分析】通过测定进入量筒中水的体积,从而确定集气瓶中收集到的氧气的体积,该测定中,集气瓶内原有空气对测定结果______________________ (填“有”或“无”)影响。
A组:探究过氧化氢溶液浓度对化学反应速率的影响
取10mL5%的过氧化氢溶液,加入0.5g二氧化锰粉末为催化剂,进行实验,记录时间t1。
取10mL2.5%的过氧化氢溶液,加入0.5g二氧化锰粉末为催化剂,进行实验,记录时间t2。
【实验数据】t1____________________ t2.(填“>”、“=”、“<”)
【实验结论】当催化剂相同时,过氧化氢溶液浓度越大,反应速率越快。
B组:探究________________ 对化学反应速率的影响。
取10mL5%的过氧化氢溶液和0.5g氧化铜粉末为催化剂进行实验,两次实验分别将试管置于冰水中和50℃热水中,收集10mL氧气的时间分别为t4、t5,且t4>t5。
【实验结论】当反应物浓度和催化剂相同时,温度越高,反应速率越快。
C组:探究催化剂种类对化学反应速率的影响
取三支试管,分别加入二氧化锰粉末、氧化铜粉末、红砖粉末各0.5g,再分别加入5mL10%
的过氧化氢溶液,记录收集10mL氧气的时间,数据如下:
【实验结论】二氧化锰粉末、氧化铜粉末、红砖粉末均可做过氧化氢溶液分解的催化剂,三者中____________________ 的催化效率最高。
【实验反思】小组同学讨论后认为,由以上数据并不能得出红砖粉末有无催化作用,应该补充一个对比实验,操作为____________________ ,记录收集10mL氧气的时间。
实验结果:长时间(大于100s),收集到很少量(小于10mL)氧气,
小组验证结论:在过氧化氢分解过程中红砖粉末__________________ (选填“有”、“无”)催化作用。
最后,老师了解到以上各组的实验设计后,建议同学们深入思考:仅探究能否改变化学反应的速率仍然不能确定其是否为催化剂,还应探究____________________ 在化学反应的前后都没有发生变化。

【装置分析】通过测定进入量筒中水的体积,从而确定集气瓶中收集到的氧气的体积,该测定中,集气瓶内原有空气对测定结果
A组:探究过氧化氢溶液浓度对化学反应速率的影响
取10mL5%的过氧化氢溶液,加入0.5g二氧化锰粉末为催化剂,进行实验,记录时间t1。
取10mL2.5%的过氧化氢溶液,加入0.5g二氧化锰粉末为催化剂,进行实验,记录时间t2。
【实验数据】t1
【实验结论】当催化剂相同时,过氧化氢溶液浓度越大,反应速率越快。
B组:探究
取10mL5%的过氧化氢溶液和0.5g氧化铜粉末为催化剂进行实验,两次实验分别将试管置于冰水中和50℃热水中,收集10mL氧气的时间分别为t4、t5,且t4>t5。
【实验结论】当反应物浓度和催化剂相同时,温度越高,反应速率越快。
C组:探究催化剂种类对化学反应速率的影响
取三支试管,分别加入二氧化锰粉末、氧化铜粉末、红砖粉末各0.5g,再分别加入5mL10%
的过氧化氢溶液,记录收集10mL氧气的时间,数据如下:
| 固体粉末 | 二氧化锰粉末0.5g | 氧化铜粉末0.5g | 红砖粉末0.5g |
| 10%的过氧化氢溶液 | 5mL | 5mL | 5mL |
| 时间/s | 10s | 20s | 60s |
【实验反思】小组同学讨论后认为,由以上数据并不能得出红砖粉末有无催化作用,应该补充一个对比实验,操作为
实验结果:长时间(大于100s),收集到很少量(小于10mL)氧气,
小组验证结论:在过氧化氢分解过程中红砖粉末
最后,老师了解到以上各组的实验设计后,建议同学们深入思考:仅探究能否改变化学反应的速率仍然不能确定其是否为催化剂,还应探究
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】有A、B两组兴趣小组对催化剂进行了探究实验。
(一)兴趣小组A组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:

(1)设置实验1的目的是_____ 。
(2)写出实验2中KClO3分解的文字表达式:_____ 。
(3)由实验1和实验4可知,KCl_____ (填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集50mLO2,所需时间明显少于171s,解释原因:_____ 。
(4)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内_____ 。
(二)兴趣小组B组选择按图1所示装置进行如下实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂接触,瓶内气压的变化如图2所示。请回答(6)-(7)题。

(5)对比分析图2中的_____ 两点(填字母符号),可知化学反应速率与催化剂的种类有关。
(6)在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同,请从催化剂的角度解释原因是_____ 。
(一)兴趣小组A组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:

| 编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s |
| 实验1 | 5 | - | - | 171 |
| 实验2 | 5 | MnO2 | 0.5 | 49 |
| 实验3 | 5 | Fe2O3 | 0.5 | 58 |
| 实验4 | 5 | KCl | 0.5 | 154 |
(2)写出实验2中KClO3分解的文字表达式:
(3)由实验1和实验4可知,KCl
(4)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内
(二)兴趣小组B组选择按图1所示装置进行如下实验,实验时倾斜锥形瓶使过氧化氢溶液与催化剂接触,瓶内气压的变化如图2所示。请回答(6)-(7)题。

(5)对比分析图2中的
(6)在实验过程中,上述两个反应虽化学反应速率不同,但完全反应后两个装置内压强相同,请从催化剂的角度解释原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】探究一:为除去铜片中混有的少量铁片,并测定该混合物中铁的质量分数,现有如下A、B两组实验方案。
A:称取一定质量的样品 过滤、洗涤、干燥、称量所得固体质量
过滤、洗涤、干燥、称量所得固体质量
B:称取一定质量的样品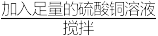 过滤、洗涤、干燥、称量所得固体质量
过滤、洗涤、干燥、称量所得固体质量
(1)两种方案,你认为不能达到目的的是_______ (填“A”或“B”),理由是_______ 。
(2)在你所选取的方案中,若采用加热烘干的方式干燥滤渣,会导致测定的铁的质量分数_______ (填“偏大”、“偏小”、“不变”或“无法判断”)。
探究二:某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
【提出猜想】
(3)放出的气体可能是SO2、O2、H2,提出猜想的依据是_______ 。
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(4)①甲同学认为是O2,则检验方法是_______ 。
②乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式_______ 。
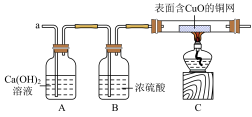
③实验小组同学合作设计了如图组合实验方案,排除和验证猜想的气体。实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色。
【实验结论】
(5)铁粉与硫酸铜溶液反应时,产生的气体是_______ 。
探究三:在铜的冶炼史中我国劳动人民有一项重大发明是“湿法冶金”。在五千年前我国劳动人民还会使用木炭炼铜。在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙)。化学兴趣小组采用图乙装置,开展以下探究活动:

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
①木炭与CuO的反应是: ,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)
,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)
②Cu2O是红色固体,能与稀硫酸反应: 。
。
【提出猜想】
(6)红色固体的成分:①全部是Cu;②全部是Cu2O;③_______ 。
【实验探究】
(7)①取木炭、CuO两种黑色粉末适量,再取少许CaCl2(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内。
②按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水_______ ,此时停止加热。
③待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
【评价反思】
(8)使用图乙装置与使用图甲装置相比,其优点是_______ (写出1条即可)。
A:称取一定质量的样品
 过滤、洗涤、干燥、称量所得固体质量
过滤、洗涤、干燥、称量所得固体质量B:称取一定质量的样品
 过滤、洗涤、干燥、称量所得固体质量
过滤、洗涤、干燥、称量所得固体质量(1)两种方案,你认为不能达到目的的是
(2)在你所选取的方案中,若采用加热烘干的方式干燥滤渣,会导致测定的铁的质量分数
探究二:某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出。生成的是什么气体呢?同学们决定进行探究。探究前老师提示,该反应生成的气体只有一种。
【提出猜想】
(3)放出的气体可能是SO2、O2、H2,提出猜想的依据是
【查阅资料】SO2易溶于水,化学性质与二氧化碳有相似之处,它能使澄清石灰水变浑浊,生成CaSO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(4)①甲同学认为是O2,则检验方法是
②乙同学认为是SO2,则只需将放出的气体通入澄清石灰水中,看澄清石灰水是否变浑浊。写出SO2与Ca(OH)2反应的化学方程式
③实验小组同学合作设计了如图组合实验方案,排除和验证猜想的气体。实验过程中发现A装置中溶液不变浑浊,C装置中表面含CuO的铜网由黑色变为光亮的红色。

【实验结论】
(5)铁粉与硫酸铜溶液反应时,产生的气体是
探究三:在铜的冶炼史中我国劳动人民有一项重大发明是“湿法冶金”。在五千年前我国劳动人民还会使用木炭炼铜。在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙)。化学兴趣小组采用图乙装置,开展以下探究活动:

【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
①木炭与CuO的反应是:
 ,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)
,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O)②Cu2O是红色固体,能与稀硫酸反应:
 。
。【提出猜想】
(6)红色固体的成分:①全部是Cu;②全部是Cu2O;③
【实验探究】
(7)①取木炭、CuO两种黑色粉末适量,再取少许CaCl2(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内。
②按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水
③待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
| 步骤 | 现象 | 结论 |
| ①取1.44g红色固体装入试管,滴入足量的 | 红色固体部分减少,溶为变为 | 猜想 |
| ②滤出试管中残留的红色固体,洗涤干燥,称其质量为1.04g | / | 猜想 |
【评价反思】
(8)使用图乙装置与使用图甲装置相比,其优点是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】“在学校的元旦联欢会上,某同学表演了‘水能生火’的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来了。”
小红看到这段话后非常感兴趣,她和同学们一起对该问题进行了探究。
[查阅资料]氢氧化钠、氢氧化钾、氢氧化钙等物质能使无色酚酞溶液变红。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
[设计装置]如右图所示

[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是_______________ ;
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:_______________
实验二:探究反应后生成的另一种物质是什么?
(3)小军猜想另一种物质可能是Na2CO3,但小红通过设计实验:向溶液中滴加少量稀盐酸,无气泡产生,证实不存在 ;
;
(3)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,小军预测反应中应有______ 生成;
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式:______________ 。
小红看到这段话后非常感兴趣,她和同学们一起对该问题进行了探究。
[查阅资料]氢氧化钠、氢氧化钾、氢氧化钙等物质能使无色酚酞溶液变红。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成②反应过程中可能有能量变化
[设计装置]如右图所示

[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:
实验二:探究反应后生成的另一种物质是什么?
(3)小军猜想另一种物质可能是Na2CO3,但小红通过设计实验:向溶液中滴加少量稀盐酸,无气泡产生,证实不存在
 ;
;(3)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,小军预测反应中应有
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】育才中学的某研究小组在探究维生素C水溶液的酸碱性时,不慎误把维C泡腾片(保健品,主要成分如图所示)当做维生素C片放入了水中,结果发现有大量气泡产生,于是引起了该小组同学的探究兴趣。
【提出问题】该气体成分是什么?
【猜想与假设】小青说:该气体可能含有CO2、O2、CO、H2、N2中的一种或几种。小丽说:不可能含有N2,因为_____ ;
小亮说:因为从药品安全角度考虑_____ 不可能含有H2和CO,最后研究小组的同学共同认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
【得出结论】
(1)由实验①可知,该气体中肯定含有_____ ,
(2)由实验②不能确定该气体中是否含氧气,理由是_____ 。

【提出问题】该气体成分是什么?
【猜想与假设】小青说:该气体可能含有CO2、O2、CO、H2、N2中的一种或几种。小丽说:不可能含有N2,因为
小亮说:因为从药品安全角度考虑
【进行实验】
| 编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入到该气体中 | 带火星的木条没有复燃 |
【得出结论】
(1)由实验①可知,该气体中肯定含有
(2)由实验②不能确定该气体中是否含氧气,理由是
您最近一年使用:0次



