某化学小组利用假期开展学科实践活动。
实践活动一、老进自来水厂
自来水厂净水过程如图所示:

(1)如图净化水的方法有:沉淀、过滤、________ 、消毒等。
(2)高铁酸钾K2FeO4是多功能水处理剂,K2FeO4中铁元素的化合价为__________ 。
(3)生活中既能降低水的硬度,又能杀菌消毒的方法是_________ 。
(4)聚合氯化铝Al2(OH)mCln是一种新型净水剂。经分析其中氢元素和氯元素的质比=2:71,则m、n推理正确的是________(填序号)。
实践活动二、走进治炼厂
钢铁厂有如下冶炼工艺流程,根据流程回答相关问题。
工艺流程一:工业炼铁的部分反应如下所示。

(5)X可以是_________ (填物质名称、下同),Y是一种铁矿石、常用___________ 。
(6)上述炼铁过程中体现了CO的还原性的反应是__________ (填序号)。
(7)根据上述炼铁过程推断反应①的主要作用是__________ 。
(8)写出反应③的化学方程式_________ 。
工艺流程二:在钢铁工业推进碳减排、碳捕集的过程中,一种以“氢能炼钢”的工艺流程如图所示。

(9)高温下,用氢气炼铁时反应的化学方程式为 ,该反应属于
,该反应属于_______ 反应(填一种基本反应类型)。
(10)工艺流程一和工艺流程二得到的产品主要区别是________ 。
实践活动三、走进采石场
小组同学从采石场收集一些石灰石,为了测定石灰石中碳酸钙的含量进行了如下实验(杂质不含钙元素,不溶于水,也不与其他物质发生反应),请回答下列问题:
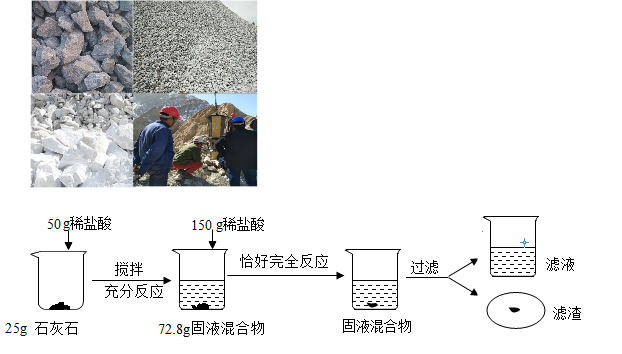
(11)上述实验过程中发生反应的化学方程式为_________ 。
(12)根据已知条件列出求解第一次加稀盐酸后参加反应的碳酸钙的质量(X)的比例式___________ 。
(13)此石灰石中碳酸钙的百分含量为________ 。
实践活动一、老进自来水厂
自来水厂净水过程如图所示:

(1)如图净化水的方法有:沉淀、过滤、
(2)高铁酸钾K2FeO4是多功能水处理剂,K2FeO4中铁元素的化合价为
(3)生活中既能降低水的硬度,又能杀菌消毒的方法是
(4)聚合氯化铝Al2(OH)mCln是一种新型净水剂。经分析其中氢元素和氯元素的质比=2:71,则m、n推理正确的是________(填序号)。
| A.m=1 n=2 | B.m=3 n=2 |
| C.m=3 n=3 | D.m=3 n=4 |
实践活动二、走进治炼厂
钢铁厂有如下冶炼工艺流程,根据流程回答相关问题。
工艺流程一:工业炼铁的部分反应如下所示。

(5)X可以是
(6)上述炼铁过程中体现了CO的还原性的反应是
(7)根据上述炼铁过程推断反应①的主要作用是
(8)写出反应③的化学方程式
工艺流程二:在钢铁工业推进碳减排、碳捕集的过程中,一种以“氢能炼钢”的工艺流程如图所示。

(9)高温下,用氢气炼铁时反应的化学方程式为
 ,该反应属于
,该反应属于(10)工艺流程一和工艺流程二得到的产品主要区别是
实践活动三、走进采石场
小组同学从采石场收集一些石灰石,为了测定石灰石中碳酸钙的含量进行了如下实验(杂质不含钙元素,不溶于水,也不与其他物质发生反应),请回答下列问题:

(11)上述实验过程中发生反应的化学方程式为
(12)根据已知条件列出求解第一次加稀盐酸后参加反应的碳酸钙的质量(X)的比例式
(13)此石灰石中碳酸钙的百分含量为
更新时间:2023-03-02 22:10:13
|
相似题推荐
综合应用题
|
适中
(0.65)
【推荐1】如图是木炭还原氧化铜的实验装置图。

(1)实验前需将木炭、氧化铜研细并混匀的目的是_______ ;
(2)该反应的基本反应类型为_______ ,氧化铜在反应中具有_______ 性;
(3)根据化学方程式计算:80 g氧化铜完全反应,理论上可制得铜的质量是多少?

(1)实验前需将木炭、氧化铜研细并混匀的目的是
(2)该反应的基本反应类型为
(3)根据化学方程式计算:80 g氧化铜完全反应,理论上可制得铜的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】填空
(1)根据要求,完成表格。
(2)中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%。工业上利用钛白粉制备海绵钛的工艺流程如图所示:_____ 。
②反应Ⅲ的化学方程式为_____ 。
③该工艺流程中,可以循环使用的物质有_____ (填化学式)。
(1)根据要求,完成表格。
| 化学符号 | 2N | 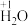 | |
| 符号意义 | 两个铵根离子 |
(2)中国首款完全自主知识产权民用客机C919飞机的钛合金用量达9.3%。工业上利用钛白粉制备海绵钛的工艺流程如图所示:
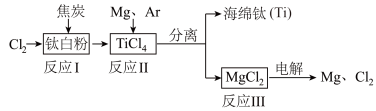
②反应Ⅲ的化学方程式为
③该工艺流程中,可以循环使用的物质有
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】化学材料和化学技术在智能房屋建设和家居生活中有着广泛的应用。

(1)智能房屋采用太阳能电池供电,生产太阳能电池需用纯硅。工业上由粗硅生产纯硅的工艺流程如图所示:

①上述三个步骤中属于物理变化的是步骤____ ;
②写出步骤Ⅲ中的化学方程式:________________________ ,该反应的基本类型属于_________ 反应;
③与太阳能电池能量转化不同,火力发电是将化石燃料燃烧产生的_____ 能转化为电能。
(2)新型碳纤维密度比铝小,强度是铁的20倍,具有抗电磁辐射、耐腐蚀的特点,化学性质与碳相似。新型碳纤维在智能房屋建设中可用作_________(填下列选项字母)。
(3)你认为该智能房屋和传统房屋相比,其优点有_____________________ 。

(1)智能房屋采用太阳能电池供电,生产太阳能电池需用纯硅。工业上由粗硅生产纯硅的工艺流程如图所示:

①上述三个步骤中属于物理变化的是步骤
②写出步骤Ⅲ中的化学方程式:
③与太阳能电池能量转化不同,火力发电是将化石燃料燃烧产生的
(2)新型碳纤维密度比铝小,强度是铁的20倍,具有抗电磁辐射、耐腐蚀的特点,化学性质与碳相似。新型碳纤维在智能房屋建设中可用作_________(填下列选项字母)。
| A.建筑材料 | B.电磁辐射屏蔽材料 | C.防火材料 |
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】金属用途广泛,其结构和性质等是化学的重要研究内容。
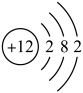
(1)如图是镁的原子结构示意图。下列说法不正确的是___________。
(2)金属活动性顺序在工农业生产和科学研究中有重要应用。
①铝比较活泼,为什么铝制品却有很好的抗腐蚀性能?_________ 。
②农业上不能用铁制容器配制波尔多液(含硫酸铜),请用化学方程式解释_________ 。
(3)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。请根据下列实验装置图回答问题:
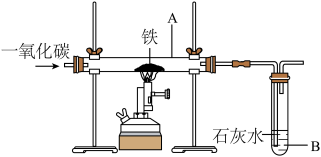
①A中玻璃管里的现象为___________ ;发生反应的化学方程式为___________ 。
②B装置中反应的化学方程式为___________ 。
③从环保的角度来看,该装置缺少了什么?请设计方案加以改正_________ 。
(4)取铜锌混合物20g放入烧杯中,加入50g的稀硫酸,恰好完全反应,测得烧杯内剩余物质的质量为69.8g,请计算:
①产生氢气的质量_________ 。
②该混合物中铜的质量_________ 。
(1)如图是镁的原子结构示意图。下列说法不正确的是___________。

| A.镁原子的质子数为12 |
| B.在化合物中镁通常显+2价 |
| C.镁是地壳中含量第二多的金属元素 |
| D.镁在燃烧时发出耀眼的白光,可用于作烟花和照明弹 |
(2)金属活动性顺序在工农业生产和科学研究中有重要应用。
①铝比较活泼,为什么铝制品却有很好的抗腐蚀性能?
②农业上不能用铁制容器配制波尔多液(含硫酸铜),请用化学方程式解释
(3)下图装置可做一氧化碳还原氧化铁的实验,并检验生成的气体产物。请根据下列实验装置图回答问题:

①A中玻璃管里的现象为
②B装置中反应的化学方程式为
③从环保的角度来看,该装置缺少了什么?请设计方案加以改正
(4)取铜锌混合物20g放入烧杯中,加入50g的稀硫酸,恰好完全反应,测得烧杯内剩余物质的质量为69.8g,请计算:
①产生氢气的质量
②该混合物中铜的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】早在春秋战国时期,我国就开始生产和使用铁器。工业上炼铁的原理是利用一氧化碳和氧化铁的反应。某中学化学兴趣小组利用如图装置进行实验探究,请按要求填空:

(1)除CO外,还有哪些物质可以还原Fe2O3?______ (请写一种物质的化学式)。
(2)该实验开始时,要先通一会儿一氧化碳再点燃酒精灯,其目的是______ 。
(3)实验中A处的现象是______ ,盛澄清石灰水的试管中可观察到的现象是______ 。
(4)右边导气管口放置点燃的酒精灯的目的是______ 。
(5)实验结束时要先______ ,直到试管冷却到室温再______ ,以防止______ 。
(6)若用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量多少?(写出解题步骤)

(1)除CO外,还有哪些物质可以还原Fe2O3?
(2)该实验开始时,要先通一会儿一氧化碳再点燃酒精灯,其目的是
(3)实验中A处的现象是
(4)右边导气管口放置点燃的酒精灯的目的是
(5)实验结束时要先
(6)若用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量多少?(写出解题步骤)
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】结合图示回答问题。

(1)写出图中标号标示的仪器名称:①______ ;
(2)实验室用KMnO4制取O2,应选用的装置组合为______ , 写出该反应的化学方程式______ ;
(3)若用B装置制取CO2,检查气密性的方法为______ ,F装置与B装置相比有什么优点______ ;
(4)铁与空气中的______ 同时作用会生锈,写一个防止铁锅生锈的方法______ ;
(5)实验室用含锌65%的粗锌20g (杂质不和稀硫酸反应)和足量的稀硫酸反应。理论上可以生成氢气多少g?

(1)写出图中标号标示的仪器名称:①
(2)实验室用KMnO4制取O2,应选用的装置组合为
(3)若用B装置制取CO2,检查气密性的方法为
(4)铁与空气中的
(5)实验室用含锌65%的粗锌20g (杂质不和稀硫酸反应)和足量的稀硫酸反应。理论上可以生成氢气多少g?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】锶(Sr)及其化合物应用广泛,常用于陶瓷、玻璃和烟花工业等。金属活动性顺序:Sr>Ca>Mg。锶的部分化合物在水中的溶解性如下表:
(1)锶元素在化合物中的常见化合价为_____ 。
(2)结合所学知识,预测氢氧化锶溶液能与下列哪些物质发生反应?_____(填标号)。
(3)设计金属锶转化为氧化锶的两种方案(写出化学方程式,要求方案1实现一步转化,方案2可多步转化)。
①方案1:_____
②方案2:_____ ,
| 物质 | 氢氧化锶 | 氯化锶 | SrSO4 | SrCO3 |
| 溶解性 | 微溶 | 易溶 | 难溶 | 难溶 |
(2)结合所学知识,预测氢氧化锶溶液能与下列哪些物质发生反应?_____(填标号)。
| A.Na2CO3溶液 | B.BaCl2溶液 | C.盐酸 | D.CO2 |
①方案1:
②方案2:

您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】苏州的许多传统与现代工艺都与化学息息相关。
I.传统工艺
(1)文物贴金。金箔不易变色,说明黄金化学性质_______ (填“稳定”或“活泼”)。
(2)传统粉墙。用石灰浆(氢氧化钙的悬浊液)抹墙后,墙壁表面变白且坚硬。在上述过程中,氢氧化钙发生反应的化学方程式为_______ 。
II.矿物颜料
(3)朱砂可制成鲜红色颜料,主要成分为硫化汞(Hg、S的化合价分别为+2和-2)。硫化汞的化学式为_______ 。
(4)赤铁矿(主要成分Fe2O3)可用于制作红棕色颜料,其中铁元素化合价为_______ 。
(5)孔雀石[主要成分为Cu2(OH)2CO3]可用于制作青色颜料,对酸敏感。补充完整下列化学方程式:Cu2(OH)2CO3+CO2+4HCl=2CuCl2+2CO2↑+3_______ 。
III.创新科技
(6)新能源客车。电池充电时的能量转化方式:电能转化为_______ 。
(7)多晶硅制备。SiH4气体被加热分解为硅和氢气,反应的化学方程式为_______ 。
I.传统工艺
(1)文物贴金。金箔不易变色,说明黄金化学性质
(2)传统粉墙。用石灰浆(氢氧化钙的悬浊液)抹墙后,墙壁表面变白且坚硬。在上述过程中,氢氧化钙发生反应的化学方程式为
II.矿物颜料
(3)朱砂可制成鲜红色颜料,主要成分为硫化汞(Hg、S的化合价分别为+2和-2)。硫化汞的化学式为
(4)赤铁矿(主要成分Fe2O3)可用于制作红棕色颜料,其中铁元素化合价为
(5)孔雀石[主要成分为Cu2(OH)2CO3]可用于制作青色颜料,对酸敏感。补充完整下列化学方程式:Cu2(OH)2CO3+CO2+4HCl=2CuCl2+2CO2↑+3
III.创新科技
(6)新能源客车。电池充电时的能量转化方式:电能转化为
(7)多晶硅制备。SiH4气体被加热分解为硅和氢气,反应的化学方程式为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐3】2023年我国锂离子电池产业增长迅速,磷酸铁锂( )是一种锂离子电池电极材料。碳酸锂、硫酸亚铁和硫酸铁是生产磷酸铁锂的原料。
)是一种锂离子电池电极材料。碳酸锂、硫酸亚铁和硫酸铁是生产磷酸铁锂的原料。

请回答下列问题:
(1)在碳酸锂( )中,锂元素的化合价为
)中,锂元素的化合价为______ 。
(2)制备硫酸铁时,通常将稀硫酸加入铁红( )中进行溶浸,该反应的化学方程式为
)中进行溶浸,该反应的化学方程式为______ 。
(3)工业上使用稀硫酸与废铁反应,制备廉价的硫酸亚铁。某公司使用含铁90%的废铁 与足量的稀硫酸反应,理论上,可以制得硫酸亚铁的质量为多少?(根据化学方程式计算,并写出计算过程)
与足量的稀硫酸反应,理论上,可以制得硫酸亚铁的质量为多少?(根据化学方程式计算,并写出计算过程)
(4)将粉末状的含铁化合物、含锂化合物和含碳化合物,按照一定比例混合均匀,高温烧结即可制得磷酸铁锂。请问将粉末状原料混合均匀的目的是______ 。
 )是一种锂离子电池电极材料。碳酸锂、硫酸亚铁和硫酸铁是生产磷酸铁锂的原料。
)是一种锂离子电池电极材料。碳酸锂、硫酸亚铁和硫酸铁是生产磷酸铁锂的原料。
请回答下列问题:
(1)在碳酸锂(
 )中,锂元素的化合价为
)中,锂元素的化合价为(2)制备硫酸铁时,通常将稀硫酸加入铁红(
 )中进行溶浸,该反应的化学方程式为
)中进行溶浸,该反应的化学方程式为(3)工业上使用稀硫酸与废铁反应,制备廉价的硫酸亚铁。某公司使用含铁90%的废铁
 与足量的稀硫酸反应,理论上,可以制得硫酸亚铁的质量为多少?(根据化学方程式计算,并写出计算过程)
与足量的稀硫酸反应,理论上,可以制得硫酸亚铁的质量为多少?(根据化学方程式计算,并写出计算过程)(4)将粉末状的含铁化合物、含锂化合物和含碳化合物,按照一定比例混合均匀,高温烧结即可制得磷酸铁锂。请问将粉末状原料混合均匀的目的是
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐1】化学是以实验为基础的科学,实验是科学探究的重要手段。根据图示回答下列问题。

(1)实验一中,比较二氧化碳的含量多少,可加入的试剂是___________ ,实验可以得出的结论是___________ 。
(2)实验二中,向两支试管中依次加入1~2小粒的碘、高锰酸钾,再各加入5mL水振荡,现象如图所示,由此得出的实验结论是___________ 。
(3)实验三中金属网罩的作用是___________ ;实验前先通入一段时间CO气体的目的是___________ ;请写出A装置中发生反应的化学方程式___________ 。
(4)证明在反应后A装置的固体中含有Fe2O3和Fe,写出简单的操作过程。
(5)某化学兴趣小组的同学取铝片样品3g(样品中杂质不溶于水,不与氢氧化钠反应),投入40g一定溶质质量分数的氢氧化钠溶液中,恰好完全反应,称量反应后物质总质量。发现比反应前总质量减少了0.3g。(已知: )求:所用氢氧化钠溶液中溶质的质量分数。
)求:所用氢氧化钠溶液中溶质的质量分数。

(1)实验一中,比较二氧化碳的含量多少,可加入的试剂是
(2)实验二中,向两支试管中依次加入1~2小粒的碘、高锰酸钾,再各加入5mL水振荡,现象如图所示,由此得出的实验结论是
(3)实验三中金属网罩的作用是
(4)证明在反应后A装置的固体中含有Fe2O3和Fe,写出简单的操作过程。
(5)某化学兴趣小组的同学取铝片样品3g(样品中杂质不溶于水,不与氢氧化钠反应),投入40g一定溶质质量分数的氢氧化钠溶液中,恰好完全反应,称量反应后物质总质量。发现比反应前总质量减少了0.3g。(已知:
 )求:所用氢氧化钠溶液中溶质的质量分数。
)求:所用氢氧化钠溶液中溶质的质量分数。
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】2015年,南澳大桥正式通车,大桥的建设及通行涉及许多的化学知识。
(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,已知生产钢材的主要原料用到赤铁矿(主要成分Fe2O3),写出工业上用赤铁矿炼铁的化学方程式:_______ 。
(2)大桥位于海上,钢铁器件容易生锈,铁生锈的条件是铁与发生反应______(填序号,下同)。
(3)大桥通车后,岛民进出南澳更快捷方便,有利于节约化石燃料的使用,从而有利减缓______。
(4)岛内某中学化学兴趣小组的同学想了解炼钢所用的赤铁矿石中氧化铁的含量,开展了如下实验:取20g赤铁矿样品(杂质不溶于水,且不与酸反应)于烧杯中,逐渐加入稀硫酸充分反应。所加稀硫酸的质量与烧杯中剩余固体质量的关系如图所示。请计算:

①该样品中氧化铁的质量为______ g。
②求所用稀硫酸中溶质的质量分数______ 。(请写出计算过程)
(1)制造大桥护栏和斜拉索等重要器件的材料都是钢,已知生产钢材的主要原料用到赤铁矿(主要成分Fe2O3),写出工业上用赤铁矿炼铁的化学方程式:
(2)大桥位于海上,钢铁器件容易生锈,铁生锈的条件是铁与发生反应______(填序号,下同)。
| A.氧气 | B.水 | C.氧气和水 | D.氧气和二氧化碳 |
(3)大桥通车后,岛民进出南澳更快捷方便,有利于节约化石燃料的使用,从而有利减缓______。
| A.雾霾天气 | B.温室效应 | C.赤潮的形成 | D.酸雨的形成 |
(4)岛内某中学化学兴趣小组的同学想了解炼钢所用的赤铁矿石中氧化铁的含量,开展了如下实验:取20g赤铁矿样品(杂质不溶于水,且不与酸反应)于烧杯中,逐渐加入稀硫酸充分反应。所加稀硫酸的质量与烧杯中剩余固体质量的关系如图所示。请计算:

①该样品中氧化铁的质量为
②求所用稀硫酸中溶质的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
【推荐3】据统计:2016年,中国粗钢产量为8.084亿吨,同比增长1.2%,占世界总产量的比重达49.6%,生产了全球近一半的钢铁。请结合以下信息和所学知识,回答问题。

(1)工业炼铁使用图Ⅰ设备,名称是____ ,炼铁时将图Ⅱ中固体原料按一定配比与图Ⅲ中的富氧热空气共同投入炼铁设备中,原料的投放口为 ______ (填“方案一”或“方案二”)。
方案一:固体原料从A口投入,热空气从B口进入;
方案二:固体原料从B口投入,热空气从A口进入;
选择此方案的优点是______ 。
(2)根据炼铁的原理:①先将焦炭燃烧产生CO2;②再进一步产生还原剂CO;③利用CO将赤铁矿中的铁还原出来。请写出③的化学反应方程式:______ ;
(3)若某炼铁厂用赤铁矿生产1吨生铁(含杂质4%),则理论上参加反应的CO为多少吨______ ?(请写出具体计算过程,注意格式)
(4)资料显示,若生产1吨生铁(含杂质4%),需要2.0吨赤铁矿、0.5吨焦炭以及0.3吨熔剂。某同学通过理论计算得出本次生产只需焦炭0.3吨,分析实际用量远高于理论值的原因可能有______ (填字母)。
A 部分焦炭与铁相互熔合,成为生铁中的部分碳元素
B 焦炭在高温下分解
C 焦炭转变成一氧化碳后,并未全部参加反应

(1)工业炼铁使用图Ⅰ设备,名称是
方案一:固体原料从A口投入,热空气从B口进入;
方案二:固体原料从B口投入,热空气从A口进入;
选择此方案的优点是
(2)根据炼铁的原理:①先将焦炭燃烧产生CO2;②再进一步产生还原剂CO;③利用CO将赤铁矿中的铁还原出来。请写出③的化学反应方程式:
(3)若某炼铁厂用赤铁矿生产1吨生铁(含杂质4%),则理论上参加反应的CO为多少吨
(4)资料显示,若生产1吨生铁(含杂质4%),需要2.0吨赤铁矿、0.5吨焦炭以及0.3吨熔剂。某同学通过理论计算得出本次生产只需焦炭0.3吨,分析实际用量远高于理论值的原因可能有
A 部分焦炭与铁相互熔合,成为生铁中的部分碳元素
B 焦炭在高温下分解
C 焦炭转变成一氧化碳后,并未全部参加反应
您最近一年使用:0次



