波尔多液是一种运用广泛的农药,由石灰乳和硫酸铜配制而成,工厂用以下反应: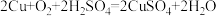 来生产硫酸铜,若要制得80kg硫酸铜。试计算:
来生产硫酸铜,若要制得80kg硫酸铜。试计算:
(1)硫酸铜中___________ (填名称)元素的质量分数最小。
(2)求参加反应的氧气的质量。
(3)若恰好消耗稀硫酸的质量为600kg,求所得硫酸铜溶液中溶质的质量分数。
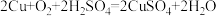 来生产硫酸铜,若要制得80kg硫酸铜。试计算:
来生产硫酸铜,若要制得80kg硫酸铜。试计算:(1)硫酸铜中
(2)求参加反应的氧气的质量。
(3)若恰好消耗稀硫酸的质量为600kg,求所得硫酸铜溶液中溶质的质量分数。
更新时间:2023-04-07 17:41:27
|
相似题推荐
计算题
|
较难
(0.4)
【推荐1】化学兴趣小组想测定Cu-Zn合金中铜、锌的成分,小华称取10g该合金粉末于烧杯中,在粉末中连续四次加入20g稀盐酸。每加一次盐酸,记录所得气体的总质量,实验数据如下,从下表数据分析:
(1)小华总共收集到氢气_____ g。第一次反应结束后,_______ 反应完了(填化学式)。
(2)求出该合金中锌的质量分数。
(3)画出实验次数与生成的氢气的质量关系曲线(在坐标图上标出必要的数据)。

| 次数 | 一 | 二 | 三 | 四 |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 |
| 生成氢气的总质量/g | 0.1 | 0.2 | 0.3 | 0.3 |
(1)小华总共收集到氢气
(2)求出该合金中锌的质量分数。
(3)画出实验次数与生成的氢气的质量关系曲线(在坐标图上标出必要的数据)。

您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】博波同学为测定某黄铜样品中铜的含量,按下图步骤和环节所示进行实验:
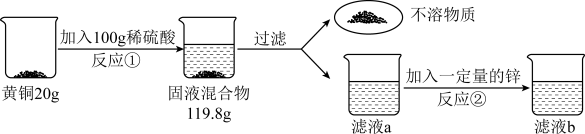
若反应①结束后,所加稀硫酸刚好反应了一半,反应②恰好完全反应。在请回答下列问题:
(1)实验中发生反应的化学方程式为________ 。
(2)根据已知条件列出求解此黄铜样品中参加反应①的物质的质量(X)的比例式________ 。
(3)该黄铜样品中铜的含量为________ 。
(4)用98%的浓硫酸配制上述实验所需稀硫酸,需要向浓硫酸中加入水的质量为_______ 。
(5)反应②结束后,向所得溶液中加入87.4g水,所得溶液中溶质的质量分数为________ 。
(6)若用含杂质为32.5%的辉铜矿【主要成分是Cu2S】100t来冶炼黄铜,冶炼过程中铜的损失率为20%,则可得上述黄铜的质量为______ 。

若反应①结束后,所加稀硫酸刚好反应了一半,反应②恰好完全反应。在请回答下列问题:
(1)实验中发生反应的化学方程式为
(2)根据已知条件列出求解此黄铜样品中参加反应①的物质的质量(X)的比例式
(3)该黄铜样品中铜的含量为
(4)用98%的浓硫酸配制上述实验所需稀硫酸,需要向浓硫酸中加入水的质量为
(5)反应②结束后,向所得溶液中加入87.4g水,所得溶液中溶质的质量分数为
(6)若用含杂质为32.5%的辉铜矿【主要成分是Cu2S】100t来冶炼黄铜,冶炼过程中铜的损失率为20%,则可得上述黄铜的质量为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】某科学兴趣小组同学取8.5g铁放到含少量硫酸的硫酸铜溶液中,完全反应后,最终得到9.2g固体。为测定所得固体中各成分的含量,同学们将62.5g稀盐酸分五次加入该固体中,得到数据如表:
请计算:
(1)表中a的值是___________ 。
(2)9.2g固体中铁的质量是___________ 。
(3)稀盐酸的溶质质量分数是多少?(写出计算过程)
(4)与硫酸铜反应的铁的质量是多少?(写出计算过程)
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸质量/g | 12.5 | 12.5 | 12.5 | 12.5 | 12.5 |
| 剩余固体质量/g | 8.5 | 7.8 | a | 6.4 | 6.4 |
请计算:
(1)表中a的值是
(2)9.2g固体中铁的质量是
(3)稀盐酸的溶质质量分数是多少?(写出计算过程)
(4)与硫酸铜反应的铁的质量是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】实验室有一包含杂质的碳酸氢钠样品100g(杂质不含钠元素,受热不变化),其中钠元素质量分数为23%,180℃时,将样品加热一段时间后称得固体质量为87.6g,则分解的碳酸氢钠占原碳酸氢钠的质量分数为多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】儿童缺锌会引起食欲不振、发育不良等症状,如图为某补锌口服液说明书的部分信息,图中葡萄糖酸锌化学式不完整,请根据相关信息回答下列问题:

(1)葡萄糖酸锌中碳、氧元素的原子个数比为多少?若相对分子质量是455,则葡萄糖酸锌化学式中氢原子右下角的数字x值是多少?
(2)若儿童Ikg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半。体重为20kg的儿童,理论上一天还需服该口服液多少支?
(3)该品牌补锌口服液中葡萄糖酸锌的质量分数为多少?(结果保留两位小数)

(1)葡萄糖酸锌中碳、氧元素的原子个数比为多少?若相对分子质量是455,则葡萄糖酸锌化学式中氢原子右下角的数字x值是多少?
(2)若儿童Ikg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半。体重为20kg的儿童,理论上一天还需服该口服液多少支?
(3)该品牌补锌口服液中葡萄糖酸锌的质量分数为多少?(结果保留两位小数)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】将16.9g碳酸钠与氯化钠的混合物加入100g足量的7.3%的稀盐酸中,求恰好完全反应后所得溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】黄铜是锌和铜的合金,可以用来制造机器零件及日常用品.为了测定某粉末状黄铜样品中锌的质量分数,取10g这种样品放入烧杯中,再将40g稀盐酸分四次加入到该烧杯中,均充分反应.测得的实验数据如下表:
分析表中数据,完成下列问题:
(1)在第_____次实验结束时样品中的锌就已完全反应.
(2)计算该黄铜样品中锌的质量分数_____.
(3)计算所用稀盐酸的溶质质量分数_____.
| 实验次数 | 1 | 2 | 3 | 4 |
| 稀盐酸的用量 | 10g | 10g | 10g | 10g |
| 剩余固体的质量 | 8.7g | 7.4g | 6.7g | 6.7g |
分析表中数据,完成下列问题:
(1)在第_____次实验结束时样品中的锌就已完全反应.
(2)计算该黄铜样品中锌的质量分数_____.
(3)计算所用稀盐酸的溶质质量分数_____.
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】为了测定石灰石样品中钙元素的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验:请回答下列问题:

(1)写出上述实验中发生反应的化学方程式为______ ;
(2)根据稀盐酸中氯化氢的质量列出求解石灰石样品中碳酸钙质量(x)的比例式为______ ;
(3)该石灰石样品中钙元素的质量分数是______ ;
(4)配制实验中所需要稀盐酸,需要质量分数为36.5%的浓盐酸的质量是______ ;
(5)最后得到固体纯净物的名称和质量分别是______ ;
(6)某工厂要想制得140t的氧化钙,理论上需要这种石灰石的质量为______ 。

(1)写出上述实验中发生反应的化学方程式为
(2)根据稀盐酸中氯化氢的质量列出求解石灰石样品中碳酸钙质量(x)的比例式为
(3)该石灰石样品中钙元素的质量分数是
(4)配制实验中所需要稀盐酸,需要质量分数为36.5%的浓盐酸的质量是
(5)最后得到固体纯净物的名称和质量分别是
(6)某工厂要想制得140t的氧化钙,理论上需要这种石灰石的质量为
您最近一年使用:0次




