回答:
(1)初中化学有许多实验,若按照实验方法分类,可将实验______ (填字母)分为一类;分类的依据是______ 。
(2)下列反应: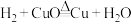 ,
,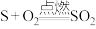 ,
, 均属于氧化还原反应,据查资料可知,氧化还原反应中一定存在着电子转移。
均属于氧化还原反应,据查资料可知,氧化还原反应中一定存在着电子转移。
①请从化合价变化角度分析______ 的物质具有还原性;
②下列反应中一定属于氧化还原反应的是______ 。
A.化合反应 B.复分解反应 C.置换反应
(1)初中化学有许多实验,若按照实验方法分类,可将实验
 |  | 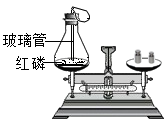 | 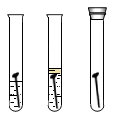 |
| A.测定空气中氧气的含量 | B.探究可燃物燃烧的条件 | C.探究反应前后物质的质量关系 | D.探究铁钉生锈的条件 |
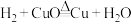 ,
,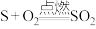 ,
, 均属于氧化还原反应,据查资料可知,氧化还原反应中一定存在着电子转移。
均属于氧化还原反应,据查资料可知,氧化还原反应中一定存在着电子转移。①请从化合价变化角度分析
②下列反应中一定属于氧化还原反应的是
A.化合反应 B.复分解反应 C.置换反应
更新时间:2023-04-06 23:58:00
|
相似题推荐
实验题
|
适中
(0.65)
解题方法
【推荐1】分类类比是初中化学常用的学习方法。
(1)初中化学有很多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等,据此应将下列实验中的D与______________ (填“A”或“B”或“C”)归为一类,依据是______________ 。
(2)氢气、碳都能做还原剂: ,
, ,我们发现发生化学变化时,还原剂所含元素的化合价
,我们发现发生化学变化时,还原剂所含元素的化合价_____________ (填“升高”或“降低”)。由此可以推知反应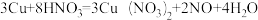 中还原剂是
中还原剂是______________ 。
 |  | 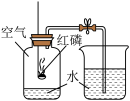 |  |
| A | B | C | D |
(2)氢气、碳都能做还原剂:
 ,
, ,我们发现发生化学变化时,还原剂所含元素的化合价
,我们发现发生化学变化时,还原剂所含元素的化合价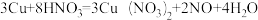 中还原剂是
中还原剂是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
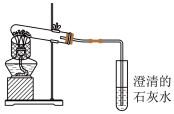
【推荐2】实验是验证物质性质的重要方法。用木炭还原氧化铜的实验装置如图所示。回答下列问题:______ 性。
(2)写出木炭还原氧化铜的化学方程式:_______ 。
(3)实验中木炭与氧化铜的质量比应控制在约_______,确保氧化铜完全反应。
(2)写出木炭还原氧化铜的化学方程式:
(3)实验中木炭与氧化铜的质量比应控制在约_______,确保氧化铜完全反应。
| A.1:10 | B.3:40 | C.1:16 |
您最近一年使用:0次
实验题
|
适中
(0.65)
真题
解题方法
【推荐1】2015年8月12日,天津港某化工仓库发生爆炸,其中有一种有毒物质是氰化钠(化学式为NaCN),消防队员用过氧化氢溶液处理该有毒物质的化学方程式是: NaCN+H2O2+X=NaHCO3+NH3↑。
(1)其中X的化学式为_________ ,NaHCO3中C元素的化合价为_________ 价。
(2)过氧化氢常用作实验室制取氧气,该反应的化学方程式为___________________ ,属于四种基本反应类型中的_________ 反应,发生装置和收集装置可选用下图中的_________ (填序号)。
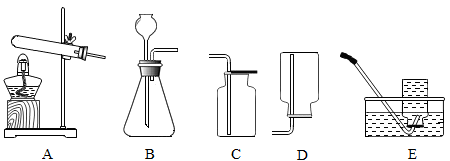
(1)其中X的化学式为
(2)过氧化氢常用作实验室制取氧气,该反应的化学方程式为

您最近一年使用:0次
【推荐2】电石是一种灰色的块状固体,化学式为CaC2,它能与水发生剧烈的化学反应,生成一种可燃性气体乙炔(化学式为:C2H2)和一种白色固体。
(1)CaC2中C的化合价是_________ ;
(2)高兴和高明两位同学对生成的白色固体产生了兴趣,对白色固体作出了猜想,高明同学认为:白色固体是氧化钙;高兴同学认为:白色固体是碳酸钙;
①你认为________ 同学的猜想肯定是错误的,理由是__________ (用化学方程式表示)
②如果你的猜想不同于他们,那么你猜想白色固体是什么呢?请你设计一个实验方案来验证你的猜想是正确的,并填入下表的空格中。
(1)CaC2中C的化合价是
(2)高兴和高明两位同学对生成的白色固体产生了兴趣,对白色固体作出了猜想,高明同学认为:白色固体是氧化钙;高兴同学认为:白色固体是碳酸钙;
①你认为
②如果你的猜想不同于他们,那么你猜想白色固体是什么呢?请你设计一个实验方案来验证你的猜想是正确的,并填入下表的空格中。
| 提出问题 | 实验操作 | 实验现象 | 实验结论 |
| 白色固体是 |
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
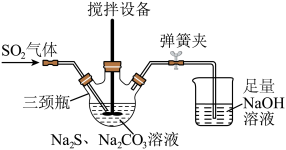
【推荐3】在初中阶段我们学习了苏打和小苏打,那有没有大苏打呢?通过自主学习,小岗同学获得了以下信息:硫代硫酸钠(Na2S2O3)俗称大苏打。实验室会将SO2气体通入Na2S(硫化钠)和Na2CO3的混合溶液中来制备Na2S2O3(实验装置如图)。请根据信息回答下列问题:______ Na2S+Na2CO3+______ SO2=3Na2S2O3+CO2,请在空白处填上合适的化学计量数,使化学方程式正确。Na2S中硫元素的化合价为______ 。
(2)烧杯中NaOH溶液的作用是______ 。
(3)实验装置中弹簧夹的作用是防止烧杯内的液体倒吸入三颈瓶,若实验过程中出现倒吸的现象,是因为三颈瓶内的气体压强______ (填“>”或“<”)外界大气压强。
(2)烧杯中NaOH溶液的作用是
(3)实验装置中弹簧夹的作用是防止烧杯内的液体倒吸入三颈瓶,若实验过程中出现倒吸的现象,是因为三颈瓶内的气体压强
您最近一年使用:0次
实验题
|
适中
(0.65)
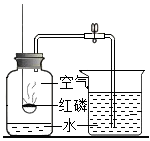
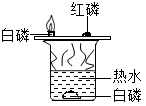
【推荐1】某化学兴趣小组的同学利用以下三组装置探究物质燃烧的条件。(提示:着火点:白磷40℃,红磷240℃)
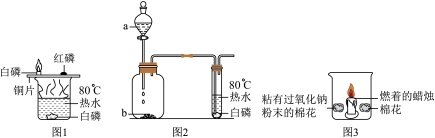
(1)如图1所示,能燃烧的物质是___________(填字母序号)。
(2)如图2所示,将无色液体a滴入瓶中并与黑色固体b接触,能观察到试管里的白磷燃烧,则瓶内发生反应的化学方程式为___________ 。
(3)如图3所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:①___________ ;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧。通过上述实验的对比分析,写出产生现象②的原因___________ 。完成三组实验之后,同学们成功探究出了燃烧所需要的条件。

(1)如图1所示,能燃烧的物质是___________(填字母序号)。
| A.水中的白磷 | B.铜片上的白磷 | C.铜片上的红磷 |
(2)如图2所示,将无色液体a滴入瓶中并与黑色固体b接触,能观察到试管里的白磷燃烧,则瓶内发生反应的化学方程式为
(3)如图3所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:①
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】已知白磷的着火点为40℃,某化学兴趣小组为探究可燃物的燃烧条件,设计并进行了如下实验(实验过程中长颈漏斗下端始终在液面以下,注射器的摩擦力忽略不计):

(1)实验前需检验装置的气密性,写出检验该装置气密性的方法:______ 。
(2)实验步骤和现象如下表所示:
写出白磷燃烧的化学方程式______ 。
(3)步骤①中白磷没燃烧的原因是______ 。对比步骤②和③可知,可燃物燃烧的条件之一是______ 。
(4)步骤④中瓶内水面上升,原因是_______ 。
【实验拓展】
(5)用仪器测定白磷燃烧时集气瓶内氧气体积分数的变化,结果如图2所示。分析图2中曲线变化趋势可知,在______ (填字母)点时白磷全部熄灭。

(1)实验前需检验装置的气密性,写出检验该装置气密性的方法:
(2)实验步骤和现象如下表所示:
| 实验步骤 | 实验现象 |
| ①将白磷放在燃烧匙内,塞好胶塞 | 白磷没燃烧 |
| ②从长颈漏斗向瓶内迅速注入80℃的水至刚刚浸没白磷 | 白磷没燃烧 |
| ③连接好注射器,向瓶内推入空气,瓶内水面下降;当白磷露出水面时,停止推入空气 | 白磷燃烧,有白烟产生 |
| ④白磷熄灭后,瓶内水面上升,最后淹没白磷 | 白磷熄灭 |
写出白磷燃烧的化学方程式
(3)步骤①中白磷没燃烧的原因是
(4)步骤④中瓶内水面上升,原因是
【实验拓展】
(5)用仪器测定白磷燃烧时集气瓶内氧气体积分数的变化,结果如图2所示。分析图2中曲线变化趋势可知,在
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】化学是一门以实验为基础的自然科学。
(一) 对比是初中化学重要的实验方法。
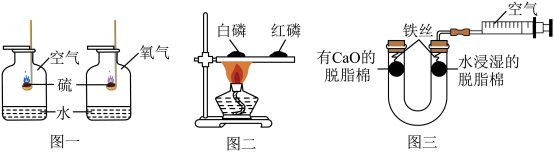
(1)图一可对比得出影响反应剧烈程度的因素是_______ 。为更有效的减少空气污染,可将水换成_______ (填名称)。
(2)图二实验_______ (填“能”或“不能”)比较白磷和红磷着火点的高低。
(3)图三中CaO的作用是_______ (用化学方程式解释),该实验能证明铁生锈与_______ (填序号)有关。
①氧气 ②水蒸气 ③氧气、水蒸气
(二)根据如图所示实验回答下列问题:
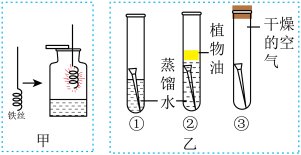

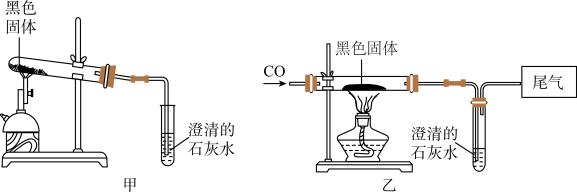
(4)甲图是铁丝在氧气中燃烧的实验。实验时瓶底有水,其目的是_____ 。
(5)乙图中,一段时间后,试管_____ (填数字序号)的铁钉生锈,对比试管①③的现象,得出的结论是_____ 。
(6)丙图中进行CO还原,Fe2O3的实验(提示:氢氧化钠溶液与一氧化碳不反应)。写出CO还原Fe2O3的化学方程式_____ ;除了吸收反应生成二氧化碳外,B装置还具有的作用是_____ 。
(一) 对比是初中化学重要的实验方法。

(1)图一可对比得出影响反应剧烈程度的因素是
(2)图二实验
(3)图三中CaO的作用是
①氧气 ②水蒸气 ③氧气、水蒸气
(二)根据如图所示实验回答下列问题:


(4)甲图是铁丝在氧气中燃烧的实验。实验时瓶底有水,其目的是
(5)乙图中,一段时间后,试管
(6)丙图中进行CO还原,Fe2O3的实验(提示:氢氧化钠溶液与一氧化碳不反应)。写出CO还原Fe2O3的化学方程式
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组选择“影响金属与酸反应速率的因素”为课题开展探究。
Ⅰ.甲同学分别用相同质量和大小的锌粒和足量稀硫酸反应的三组实验数据:
(1)实验前需准备不同浓度的稀硫酸,若要配制98.0g质量分数为10%的稀硫酸,需质量分数为98%的浓硫酸______ g。稀释过程如图所示,则a是_____ (填“水”或“浓硫酸”)。
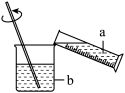
(2)能表明硫酸浓度对反应快慢有影响的实验编号是:_____ 。
(3)如果把实验②中温度提高至25℃,请你推测锌粒消失时间(用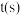 表示)的取值范围:
表示)的取值范围:____ 。
(4)该实验除了用锌粒消失的时间来衡量反应的快慢外,你还能通过_____ 来衡量该反应的快慢。
Ⅱ.乙同学在 稀硫酸中加入适量锌粒,用排水集气法收集生成的氢气,实验记录如下(累计值)。
稀硫酸中加入适量锌粒,用排水集气法收集生成的氢气,实验记录如下(累计值)。
(5)由上述数据可知,______ min时(选0~1、1~2、2~3、3~4、4~5作答)反应速率最大。
Ⅲ.丙同学探究加入CuSO4溶液的体积对H2生成速率的影响。实验中温度一定,Zn粒过量且颗粒大小相同,饱和CuSO4溶液用量0~4.0mL,保持溶液总体积为100.0mL,记录获得相同体积(336mL)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。
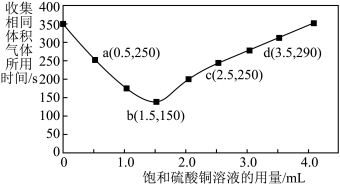
(6)由图可知:a、c两点对应的氢气生成速率______ (填“相等”或“不相等”)。
(7)对这个实验结果,丙同学感到不甚理解,请教老师得知:少量 的硫酸铜溶液会和锌反应生成少量 铜,与锌形成原电池后产生氢气的速率要比纯锌快,请写出锌和硫酸铜溶液反应的化学方程式________ 。
(8)你认为出现bd段变化趋势的原因可能是_______ 。
Ⅰ.甲同学分别用相同质量和大小的锌粒和足量稀硫酸反应的三组实验数据:
| 试验编号 | 硫酸浓度/% | 反应温度/℃ | 锌粒消失的时间/s |
| ① | 10 | 20 | 500 |
| ② | 20 | 20 | 300 |
| ③ | 20 | 30 | 80 |

(2)能表明硫酸浓度对反应快慢有影响的实验编号是:
(3)如果把实验②中温度提高至25℃,请你推测锌粒消失时间(用
 表示)的取值范围:
表示)的取值范围:(4)该实验除了用锌粒消失的时间来衡量反应的快慢外,你还能通过
Ⅱ.乙同学在
 稀硫酸中加入适量锌粒,用排水集气法收集生成的氢气,实验记录如下(累计值)。
稀硫酸中加入适量锌粒,用排水集气法收集生成的氢气,实验记录如下(累计值)。| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 290 | 310 |
Ⅲ.丙同学探究加入CuSO4溶液的体积对H2生成速率的影响。实验中温度一定,Zn粒过量且颗粒大小相同,饱和CuSO4溶液用量0~4.0mL,保持溶液总体积为100.0mL,记录获得相同体积(336mL)的气体所需时间,实验结果如图所示(气体体积均转化为标况下)。

(6)由图可知:a、c两点对应的氢气生成速率
(7)对这个实验结果,丙同学感到不甚理解,请教老师得知:
(8)你认为出现bd段变化趋势的原因可能是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】某小组为了证实中和反应生成水,进行了如下实验:小组同学取变色硅胶(吸水后由蓝色变红色)、无水醋酸(一种酸,常温下为无色液体)和氢氧化钠固体进行如图所示的三个实验。
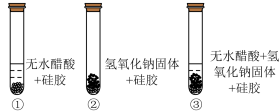
(1)设计实验①和②的目的是证明:___________________ ;
(2)能证明酸和碱反应有水生成的实验现象:_____________________ ;
(3)若反应结束后滴入紫色石蕊试液,溶液变红色,则说明溶液呈_____________ 性。

(1)设计实验①和②的目的是证明:
(2)能证明酸和碱反应有水生成的实验现象:
(3)若反应结束后滴入紫色石蕊试液,溶液变红色,则说明溶液呈
您最近一年使用:0次

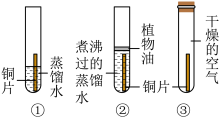
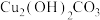 ]。结合已学知识,铜生锈需要的条件还可能有需要与
]。结合已学知识,铜生锈需要的条件还可能有需要与

