氢气是目前人类最理想的绿色燃料,氢气燃烧的化学方程式为___________ ;将一定质量的甲烷和氧气置于密闭容器中,点燃使其恰好完全反应,产物为CO、CO2和H2O,待容器恢复至室温,测得容器内CO和CO2的混合气体中碳元素与氧元素的质量比为9:16,则反应前甲烷和氧气的质量比为___________ (填最简整数比)。
2023九年级下·河南南阳·专题练习 查看更多[3]
2023年河南省南阳名校联谊第一次联考化学试题2020年河南省周口市郸城县南丰镇第一初级中学中考一模化学试题(已下线)5.2 如何正确书写化学方程式(专题训练)【三大题型】-2023-2024学年九年级化学上册同步考点解读与专题训练(人教版)
更新时间:2023-04-17 11:18:49
|
相似题推荐
计算题
|
较难
(0.4)
真题
【推荐1】为了测定某硫酸铜溶液的质量分数,小杨同学取50.0g样品置于烧杯中,逐滴加入氢氧化钠溶液,加入氢氧化钠溶液质量和生成沉淀质量的关系如下图所示。请计算:
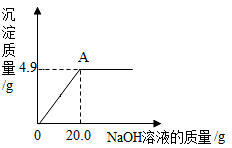
(1)NaOH的化学式量为_________。
(2)硫酸铜刚好完全反应时,所得溶液的质量为_____g(保留一位小数)。
(3)硫酸铜溶液中溶质的质量分数是________?(写出计算过程)

(1)NaOH的化学式量为_________。
(2)硫酸铜刚好完全反应时,所得溶液的质量为_____g(保留一位小数)。
(3)硫酸铜溶液中溶质的质量分数是________?(写出计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】食醋是厨房中常用的调味品,其中含有醋酸(化学式为CH3COOH)。请回答:
(1)醋酸由________种元素组成,每个醋酸分子共含有________个原子,其相对分子质量为________。
(2)醋酸中碳、氢两种元素质量比为________。(要求写出计算式及计算结果)
(3)醋酸中氧元素的质量分数为________。(要求写出计算式及计算结果,精确到0.1%)
(4)12g醋酸中氧元素的质量为________g。
(1)醋酸由________种元素组成,每个醋酸分子共含有________个原子,其相对分子质量为________。
(2)醋酸中碳、氢两种元素质量比为________。(要求写出计算式及计算结果)
(3)醋酸中氧元素的质量分数为________。(要求写出计算式及计算结果,精确到0.1%)
(4)12g醋酸中氧元素的质量为________g。
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】某炼铜厂排放的废水中含有硫酸和硫酸铜两种污染物,取废水400g,向其中加入溶质质量分数为20%的氢氧化钠溶液,测得质量关系如下图:

(1)CuSO4由_____ 元素组成。
(2)H2SO4中硫原子与氧原子的个数比为_____ 。
(3)NaOH的相对分子质量为_______ ,其中氧元素的质量分数为_______ 。
(4)计算该废水中硫酸的溶质质量分数是多少?

(1)CuSO4由
(2)H2SO4中硫原子与氧原子的个数比为
(3)NaOH的相对分子质量为
(4)计算该废水中硫酸的溶质质量分数是多少?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】根据甲酸甲酯(C2H4O2)的化学式计算:
(1)C2H4O2的相对分子质量为______________
(2)C2H4O2中各元素的质量比为______________
(3)C2H4O2中碳元素的质量分数为_______________
(4)实验测得由甲酸甲酯(C2H4O2)、甲酸乙酯(C3H6O2)组成的混合物中碳元素的质量分数是43.2%,求氧元素的质量分数为__________
(1)C2H4O2的相对分子质量为______________
(2)C2H4O2中各元素的质量比为______________
(3)C2H4O2中碳元素的质量分数为_______________
(4)实验测得由甲酸甲酯(C2H4O2)、甲酸乙酯(C3H6O2)组成的混合物中碳元素的质量分数是43.2%,求氧元素的质量分数为__________
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】2017年5月18日,中国在南海成功试采可燃冰,它将推动世界能源利用格局的改变。可燃冰是在高压低温环境条件下,水分子笼中装有甲烷分子而成的“冰块”,可直接点燃。已知某种可燃冰的化学式为:CH4·8H2O。请计算:
(1)这种可燃冰中碳、氢、氧元素质量比是多少?
(2)这种可燃冰的质量为多少克时,与44g二氧化碳所含碳元素质量相等?
(1)这种可燃冰中碳、氢、氧元素质量比是多少?
(2)这种可燃冰的质量为多少克时,与44g二氧化碳所含碳元素质量相等?
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】兴趣小组的同学为了测定某铜锌合金中锌的质量分数,小明同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下(实验中的误差忽略不计)
①上表数据分析,第_____次中的锌与稀硫酸中的硫酸恰好完全反应
②试计算该铜锌合金中锌的质量分数为_____
③恰好完全反应后所得溶液中溶质的质量分数____(保留0.1%)
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀硫酸的质量/g | 120 | 100 | 100 |
| 反应后烧杯中物质的质量/g | 144.6 | 124.6 | 149.6 |
①上表数据分析,第_____次中的锌与稀硫酸中的硫酸恰好完全反应
②试计算该铜锌合金中锌的质量分数为_____
③恰好完全反应后所得溶液中溶质的质量分数____(保留0.1%)
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】生产的NH4HCO3化肥中常含有NH4Cl,现取含NH4Cl的NH4HCO3样品89.7g,其中氯元素的质量为7.1g。向该样品中加入一定量的稀盐酸,恰好完全反应时得到545.7g溶液。
(注明:NaHCO3和NH4HCO3跟盐酸反应的原理完全一样)
(1)上述过程中发生反应的化学方程式为________ 。
(2)样品中NH4Cl的质量为________ g。
(3)计算盐酸的溶质质量分数_______ (写出计算过程,结果精确到0.1%)。
(注明:NaHCO3和NH4HCO3跟盐酸反应的原理完全一样)
(1)上述过程中发生反应的化学方程式为
(2)样品中NH4Cl的质量为
(3)计算盐酸的溶质质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】为了测定大理石样品中钙元素的质量分数(杂质不含钙元素,不溶于水,也不与其他物质发生反应),进行了如下实验。请回答下列问题:

(1)上述实验过程中发生反应的化学方程式为______ 。
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质的质量(x)的比例式______ 。
(3)此大理石样品中钙元素的质量分数______ 。
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需浓盐酸的质量为______ 。
(5)若将反应后的滤液蒸发11.2g水,无晶体析出,所得溶液中溶质的质量分数为______ 。
(6)现有上述大理石样品100t,可以制得含杂质的生石灰的质量为______ 。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解第一次所加的稀盐酸中溶质的质量(x)的比例式
(3)此大理石样品中钙元素的质量分数
(4)用36.5%的浓盐酸配制200g上述稀盐酸,所需浓盐酸的质量为
(5)若将反应后的滤液蒸发11.2g水,无晶体析出,所得溶液中溶质的质量分数为
(6)现有上述大理石样品100t,可以制得含杂质的生石灰的质量为
您最近一年使用:0次




