青团是一种传统美食,家庭制作时常出现蒸制后变黄的现象。兴趣小组探究了影响青团颜色的因素。

【查阅资料】
①艾䓍含大量叶绿素,汁水可使青团着色。叶绿素不稳定,易被氧化、酸化变色。
②NaHCO3可以与植物细胞中酸性物质反应,阻碍叶绿素分解,使青团保持鲜亮的绿色。
【进行实验】
取等体积鲜榨艾草汁,分别加入等质量糯米粉中,搅拌,揉制成大小相同的糯米团,蒸制后观察青团颜色。实验记录如下表:
【解释与结论】
(1)NaHCO3的俗称是_______ 。
(2)④中青团比①中颜色偏绿的原因是_______ 。
(3)依据⑤~⑦得出的结论是_______ 。
(4)探究蒸制火候对青团颜色影响的实验是_______ (填序号)。
【反思与评价】
(5)探究NaHCO3最佳用量的实验中,在中火,蒸制15min的条件下,没有再进行NaHCO3添加量为2.0g的实验,理由是_______ 。
(6)青团蒸制前后常会在其表面刷一层食用油,刷油的目的可能是_______ 。

【查阅资料】
①艾䓍含大量叶绿素,汁水可使青团着色。叶绿素不稳定,易被氧化、酸化变色。
②NaHCO3可以与植物细胞中酸性物质反应,阻碍叶绿素分解,使青团保持鲜亮的绿色。
【进行实验】
取等体积鲜榨艾草汁,分别加入等质量糯米粉中,搅拌,揉制成大小相同的糯米团,蒸制后观察青团颜色。实验记录如下表:
| 实验序号 | NaHCO3添加量/g | 蒸制火候 | 蒸制时间/min | 是否蒸熟 | 青团颜色 |
| ① | 0 | 大火 | 15 | 是 | 深黄色 |
| ② | 0.5 | 小火 | 15 | 否 | 绿色 |
| ③ | 0.5 | 中火 | 15 | 是 | 黄绿色 |
| ④ | 0.5 | 大火 | 15 | 是 | 黄绿色 |
| ⑤ | 1.0 | 中火 | 15 | 是 | 绿色 |
| ⑥ | 1.0 | 中火 | 18 | 是 | 黄色 |
| ⑦ | 1.0 | 中火 | 21 | 是 | 深黄色 |
| ⑧ | 1.5 | 中火 | 15 | 是 | 黄色 |
(1)NaHCO3的俗称是
(2)④中青团比①中颜色偏绿的原因是
(3)依据⑤~⑦得出的结论是
(4)探究蒸制火候对青团颜色影响的实验是
【反思与评价】
(5)探究NaHCO3最佳用量的实验中,在中火,蒸制15min的条件下,没有再进行NaHCO3添加量为2.0g的实验,理由是
(6)青团蒸制前后常会在其表面刷一层食用油,刷油的目的可能是
2023·北京通州·一模 查看更多[2]
更新时间:2023-05-01 22:39:43
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】某化学兴趣小组的同学对碳酸钠、碳酸氢钠和稀盐酸的反应进行了探究,请你参与实验。
(1)分别在盛有少量碳酸钠、碳酸氢钠固体的试管中加入足量稀盐酸,都观察到_____________ ,写出碳酸钠和稀盐酸反应的化学方程式___________________________ 。
为探究碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的快慢是否相同,小组同学取等体积、含碳元素质量也相同的碳酸钠和碳酸氢钠溶液,分别和相同体积、相同浓度的足量稀盐酸反应,按图1所示装置进行实验(提示:连通管的作用是平衡压强,控制分液漏斗活塞使稀盐酸顺利匀速流下)。压强传感器测得广口瓶内气压随时间变化如图2所示。

【进行实验】
(2)用分液漏斗滴加稀盐酸的好处是____________________ 。
(3)图1装置中连通器的作用是______________________________ 。
【实验结论】
(4)分析图2所示的实验数据可得到的结论是:其他条件相同时,__________ 和稀盐酸反应产生二氧化碳较快,理由是______________________________ 。
【反思交流】
(5)下列关于碳酸氢钠和碳酸钠的叙述中,正确的是__________。
(6)该实验中同学们用的是“等体积、含有碳元素质量相等的碳酸钠和碳酸氢钠溶液”,为什么不能用“等质量、等溶质质量分数的碳酸钠和碳酸氢钠溶液”呢?请说明理由______________________________ 。
(1)分别在盛有少量碳酸钠、碳酸氢钠固体的试管中加入足量稀盐酸,都观察到
为探究碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的快慢是否相同,小组同学取等体积、含碳元素质量也相同的碳酸钠和碳酸氢钠溶液,分别和相同体积、相同浓度的足量稀盐酸反应,按图1所示装置进行实验(提示:连通管的作用是平衡压强,控制分液漏斗活塞使稀盐酸顺利匀速流下)。压强传感器测得广口瓶内气压随时间变化如图2所示。

【进行实验】
(2)用分液漏斗滴加稀盐酸的好处是
(3)图1装置中连通器的作用是
【实验结论】
(4)分析图2所示的实验数据可得到的结论是:其他条件相同时,
【反思交流】
(5)下列关于碳酸氢钠和碳酸钠的叙述中,正确的是__________。
| A.碳酸氢钠是小苏打的主要成分,可以用作发酵粉 |
| B.碳酸钠可广泛用于玻璃、造纸、纺织和洗涤剂的生产 |
| C.为证明碳酸钠溶液中是否含有碳酸氢钠,可向溶液中滴加稀盐酸 |
(6)该实验中同学们用的是“等体积、含有碳元素质量相等的碳酸钠和碳酸氢钠溶液”,为什么不能用“等质量、等溶质质量分数的碳酸钠和碳酸氢钠溶液”呢?请说明理由
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】维生素C(C6H8O6)具有增强机体抵抗力,预防和治疗坏血病等作用。某研究小组发现,维C泡腾片溶于水时,有许多气泡产生,该小组同学进行了如下探究。
【提出问题】维生素C泡腾片溶于水后产生的气体是什么?
【查阅资料】
①某品牌维生素C泡腾片主要成分如图。

②柠檬酸为食用酸类,可增强体内正常代谢,适当剂量对人体无害。柠檬酸易溶于水,20℃时,其2%水溶液的pH为2.1。
【猜想与假设】
(1)同学甲认为该气体中不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO________ 。
(2)同学乙认为该气体也不可能含有N2,因为________ 。
同学丙认为该气体可能含有O2、CO2中的一种或两种。
【进行试验】
【解释与结论】
(3)同学丁认为由实验Ⅱ不能确定该气体中不含O2,理由是_________ 。同学们经过讨论,设计了更为严谨的实验,最终证明了该气体中不含氧气。
(4)实验Ⅲ中,澄清石灰水变浑浊反应的化学方程式为_____________ ,结论是该气体中一定含有______ 。
【反思与评价】
(5)维生素C泡腾片的保存注意事项是_________ 。
(6)在医疗上,碳酸氢钠是治疗_____ 的一种药剂。
(7)通过本次探究活动,你觉得柠檬酸还可能有的用途是___ (填字母序号)。
【提出问题】维生素C泡腾片溶于水后产生的气体是什么?
【查阅资料】
①某品牌维生素C泡腾片主要成分如图。

②柠檬酸为食用酸类,可增强体内正常代谢,适当剂量对人体无害。柠檬酸易溶于水,20℃时,其2%水溶液的pH为2.1。
【猜想与假设】
(1)同学甲认为该气体中不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO
(2)同学乙认为该气体也不可能含有N2,因为
同学丙认为该气体可能含有O2、CO2中的一种或两种。
【进行试验】
| 实验编号 | 实验操作 | 实验现象 |
| Ⅰ | 将一片维生素C泡腾片放入装有水的试管中 | 有大量气泡产生 |
| Ⅱ | 将带火星的木条伸入试管 | 带火星的木条没有复燃 |
| Ⅲ | 将气体通入澄清石灰水中 | 澄清石灰水变浑浊 |
(3)同学丁认为由实验Ⅱ不能确定该气体中不含O2,理由是
(4)实验Ⅲ中,澄清石灰水变浑浊反应的化学方程式为
【反思与评价】
(5)维生素C泡腾片的保存注意事项是
(6)在医疗上,碳酸氢钠是治疗
(7)通过本次探究活动,你觉得柠檬酸还可能有的用途是___ (填字母序号)。
| A.作碳酸饮料的添加剂 | B.作金属除锈剂 | C.作水壶除垢剂 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】松花蛋是一种美食,但直接吃会有一种涩味。为了解其原因,化学兴趣小组的同学们在老师的带领下,深入某食品加工厂对其制作过程展开探究。
任务一:调查配料
技术检验部工作人员提供了配料:鸭蛋、水、生石灰、纯碱、食盐、红茶末等,其中纯碱的化学式为____________ 。
任务二:腌制松花蛋的浸泡液中有哪些溶质?
【做出猜想】猜想一:CaO、Ca(OH)2、NaOH、NaCl
猜想二:Na2 CO3、NaOH、NaCl
猜想三:Ca(OH)2、NaOH、NaCl
猜想四:NaOH、NaCl
同学们一致认为猜想一不成立,因为浸泡液中一定没有__________ ,为探究其余褙想同学们设计了以下实验方案:
【实验方案】
但老师认为:由以上方案得出猜想二不成立不够严谨,他认为不改变药品种类只需改用_______________ 即可得出正确结论。
任务三:食用时如何改善松花蛋表面的涩味?
同学们一致认为:松花蛋浸泡液中各物质无论是否恰好反应,浸泡液一定显碱性,请你用化学方程式表示:__________ 。
结合以上探究过程,请你选出改善涩味的调料______________ (填字母)。
A.食盐 B.食醋 C.小苏打
【交流反思】从绿色化学角度考虑,浸泡松花蛋的废液应加入酸性物质处理至达标后排放。
任务一:调查配料
技术检验部工作人员提供了配料:鸭蛋、水、生石灰、纯碱、食盐、红茶末等,其中纯碱的化学式为
任务二:腌制松花蛋的浸泡液中有哪些溶质?
【做出猜想】猜想一:CaO、Ca(OH)2、NaOH、NaCl
猜想二:Na2 CO3、NaOH、NaCl
猜想三:Ca(OH)2、NaOH、NaCl
猜想四:NaOH、NaCl
同学们一致认为猜想一不成立,因为浸泡液中一定没有
【实验方案】

| 实验操作 | 实验现象 | 实验结论 |
| ①取样滴加少量稀盐酸 | 若 | 则猜想二不成立 |
| ②取样通入适量气体 | 若有白色沉淀生成 | 则猜想三成立、猜想四不成立 |
任务三:食用时如何改善松花蛋表面的涩味?
同学们一致认为:松花蛋浸泡液中各物质无论是否恰好反应,浸泡液一定显碱性,请你用化学方程式表示:
结合以上探究过程,请你选出改善涩味的调料
A.食盐 B.食醋 C.小苏打
【交流反思】从绿色化学角度考虑,浸泡松花蛋的废液应加入酸性物质处理至达标后排放。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】为探究碳酸钠的化学性质,某兴趣小组的同学做了图一图二两组实验。实验结束后,将两组实验试管中的物质分别倒入甲、乙两个洁净的烧杯中,请根据图回答下列问题。

(1)试管①中能够观察到的现象是______
(2)写出试管②中发生的化学方程式______
(3)试管③④中产生的现象均为______ 写出试管③中发生的化学方程式______ 。
(4)兴趣小组的同学完成上述实验后,为继续探究酸碱盐之间的反应,又对甲乙烧杯内的反应混合物进行下图所示的实验探究。

①根据上述实验分析推断,图一中试管②完全反应后所得的溶液中一定含有的溶质是______ (填化学式)。
②沉淀N的化学式为______ 小组同学把沉淀M、N混合后置于烧杯屏中,向其中加入过量的稀盐酸,观察到的实验现象为______ 。

(1)试管①中能够观察到的现象是
(2)写出试管②中发生的化学方程式
(3)试管③④中产生的现象均为
(4)兴趣小组的同学完成上述实验后,为继续探究酸碱盐之间的反应,又对甲乙烧杯内的反应混合物进行下图所示的实验探究。

①根据上述实验分析推断,图一中试管②完全反应后所得的溶液中一定含有的溶质是
②沉淀N的化学式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】为预防冠状病毒肺炎,小博在家进行空中课堂学习,同时又帮助父母做些家务。在洗碗的过程中,他发现洗洁精能清洗油污,引起了他的探究兴趣。他上网查阅发现能去除油污的厨房用品还有炉灶清洁剂、碳酸钠等物质。
(1)他根据学习的化学知识知道,洗涤剂清洗油污是________ 原理。
探究一:炉灶清洁剂除油污的原因:
【查阅资料】①炉灶清洁剂的主要成分为氢氧化钠。
②炉灶清洁剂中的氢氧化钠能与油污发生化学反应,生成可溶于水的物质,达到去除油污的目的。
(2)由此联想到洗洁精与炉灶清洁剂的洗涤原理________ (填“一样”或“不一样”)。
(3)炉灶清洁剂使用完后应盖上盖子,否则与空气中的成分发生化学反应。写出反应的化学方程式_________ 。
探究二:碳酸钠除油污的原因:
【查阅资料】碳酸钠的热溶液碱性较强,是因为Na2CO3可与热水发生少量的化学反应,反应的化学方程式可简单表示为: ,X是一种钠盐。油污与碱性物质反应生成易溶于水的盐类物质而洗去。
,X是一种钠盐。油污与碱性物质反应生成易溶于水的盐类物质而洗去。
(4)写出X在日常生活中的一种用途____________ 。
(5)小博在吃饭时衣服上沾染油污,他的妈妈告诉他可以用棉签浸入汽油慢慢擦拭去除油污。汽油去除油污是___________ 原理。
(1)他根据学习的化学知识知道,洗涤剂清洗油污是
探究一:炉灶清洁剂除油污的原因:
【查阅资料】①炉灶清洁剂的主要成分为氢氧化钠。
②炉灶清洁剂中的氢氧化钠能与油污发生化学反应,生成可溶于水的物质,达到去除油污的目的。
(2)由此联想到洗洁精与炉灶清洁剂的洗涤原理
(3)炉灶清洁剂使用完后应盖上盖子,否则与空气中的成分发生化学反应。写出反应的化学方程式
探究二:碳酸钠除油污的原因:
【查阅资料】碳酸钠的热溶液碱性较强,是因为Na2CO3可与热水发生少量的化学反应,反应的化学方程式可简单表示为:
 ,X是一种钠盐。油污与碱性物质反应生成易溶于水的盐类物质而洗去。
,X是一种钠盐。油污与碱性物质反应生成易溶于水的盐类物质而洗去。(4)写出X在日常生活中的一种用途
(5)小博在吃饭时衣服上沾染油污,他的妈妈告诉他可以用棉签浸入汽油慢慢擦拭去除油污。汽油去除油污是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】“极限挑战”化学创客团队对碳酸钠、碳酸氢钠分别与稀盐酸的反应进行了探究。
(1)分别在盛有少量碳酸钠、碳酸氢钠固体的试管中加入足量稀盐酸,观察到都剧烈反应且产生大量气泡。其中,碳酸氢钠和稀盐酸反应的化学方程式为__________________ 。
【提出问题】碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的快慢是否相同?

【设计与实验】
(2)甲设计的实验如图1所示。同时全部推出足量稀盐酸后,观察到图2所示现象。于是他得出_____________ 和稀盐酸反应产生二氧化碳较快的结论。
(3)同学通过计算可知,0.318g碳酸氢钠约产生0.167g二氧化碳,而0.318g碳酸钠产生二氧化碳为_______________ g,等质量两种固体分别与足量稀盐酸反应,碳酸氢钠产生二氧化碳的质量更多,显然甲同学的设计不妥,应取含碳元素质量相同的碳酸钠和碳酸氢钠进行实验。若碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为_____________________ 。
(4)甲、乙同学在导师指导下设计了如图3所示的实验。连通管的作用除了平衡装置内压强,便于液体顺利滴下外,还有________________ 的作用。

分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液),以及相同体积、相同浓度的足量稀盐酸进行实验。实验时,溶液颜色变化记录如表,广口瓶内压强随时间变化如图4所示。
(5)分析图4所示的实验数据可得到的结论是:相同条件下,碳酸氢钠和稀盐酸反应产生二氧化碳较快。你判断的理由是________________ 。
(6)甲、乙同学分析上表记录的实验现象和图4数据,得出碳酸钠能与稀盐酸反应产生二氧化碳,反应是分步进行的,第一步发生反应的化学方程式为_______ ,第二步发生反应的化学方程式为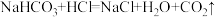 。
。
(1)分别在盛有少量碳酸钠、碳酸氢钠固体的试管中加入足量稀盐酸,观察到都剧烈反应且产生大量气泡。其中,碳酸氢钠和稀盐酸反应的化学方程式为
【提出问题】碳酸钠、碳酸氢钠和稀盐酸反应产生二氧化碳的快慢是否相同?

【设计与实验】
(2)甲设计的实验如图1所示。同时全部推出足量稀盐酸后,观察到图2所示现象。于是他得出
(3)同学通过计算可知,0.318g碳酸氢钠约产生0.167g二氧化碳,而0.318g碳酸钠产生二氧化碳为
(4)甲、乙同学在导师指导下设计了如图3所示的实验。连通管的作用除了平衡装置内压强,便于液体顺利滴下外,还有

分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液),以及相同体积、相同浓度的足量稀盐酸进行实验。实验时,溶液颜色变化记录如表,广口瓶内压强随时间变化如图4所示。
| 滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
| 碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
| 碳酸氢钠溶液 | 浅红色 | 浅红色→无色 |
(5)分析图4所示的实验数据可得到的结论是:相同条件下,碳酸氢钠和稀盐酸反应产生二氧化碳较快。你判断的理由是
(6)甲、乙同学分析上表记录的实验现象和图4数据,得出碳酸钠能与稀盐酸反应产生二氧化碳,反应是分步进行的,第一步发生反应的化学方程式为
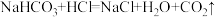 。
。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐1】工业用水对硬度有明确要求,硬度过大会造成危险,使用时需进行软化。某兴趣小组对水的硬度进行如下探究:
【查阅资料】水的硬度:水中可溶性钙镁化合物含量的多少,含量较少或不含即为软水。
(一)探究水的硬度、肥皂水用量与产生泡沫量的关系
【进行实验】各试剂用量与现象记录如下:
【解释与结论】
(1)②中x应为________ 。
(2)对比①和③可知:肥皂水能区分软水和硬水,依据的现象是_____ 。
(3)设计③④⑤实验的目的是_______ 。
(4)②和④记录的现象相同,有同学认为两试管中水样的硬度也相同,判断正误并说明理由_____ 。
(二)比较不同水样的硬度
【进行实验】用三种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
【解释与结论】
(5)硬度最大的水样是______ 。
(6)由上述实验可知,家庭里常用于降低水硬度的方法是_____ 。该过程发生的反应之一是水中可溶性Ca(HCO3)2在相应条件下分解生成碳酸钙、水和二氧化碳,其化学方程式为______ 。
【查阅资料】水的硬度:水中可溶性钙镁化合物含量的多少,含量较少或不含即为软水。
(一)探究水的硬度、肥皂水用量与产生泡沫量的关系
【进行实验】各试剂用量与现象记录如下:
| 实验操作 |  | ||||
| 实验序号 | ① | ② | ③ | ④ | ⑤ |
| 混合液用量/滴 | 0 | x | 2 | 2 | 2 |
| 肥皂水用量/滴 | 10 | 10 | 10 | 20 | 30 |
| 产生泡沫量 | 多 | 少 | 无 | 少 | 多 |
(1)②中x应为
(2)对比①和③可知:肥皂水能区分软水和硬水,依据的现象是
(3)设计③④⑤实验的目的是
(4)②和④记录的现象相同,有同学认为两试管中水样的硬度也相同,判断正误并说明理由
(二)比较不同水样的硬度
【进行实验】用三种水样完成实验,记录观察到泡沫产生时所需肥皂水的用量。
| 实验操作 | 水样 | 肥皂水用量/滴 |
 | 市售纯净水 | 8 |
| 煮沸后的自来水 | 5 | |
| 自来水 | 7 |
(5)硬度最大的水样是
(6)由上述实验可知,家庭里常用于降低水硬度的方法是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】化学课上老师进行以下实验探究分子的特性。

如图1,烧杯甲中装有20mL蒸馏水,并滴入了几滴酚酞,在烧杯乙中装有10mL浓氨水。用一个大烧杯将甲、乙两个小烧杯罩在一起。一段时间后,甲烧杯中的溶液由无色变为红色。关于酚酞变红,同学们提出了三种猜想:
猜想一:从乙烧杯中蒸发出水蒸气,部分水分子运动进入甲烧杯,水使酚酞变红。
猜想二:从乙烧杯中挥发出氨气,部分氨气分子运动进入甲烧杯,氨气使酚酞变红。
猜想三:从乙烧杯中挥发出氨气,部分氨气分子运动进入甲烧杯与水结合形成氨水,氨水使酚酞变红。
(1)同学们经过讨论后一致认为猜想一是不可能的,理由是_____ 。
(2)为了探究另外两种猜想是否正确,同学们设计了如下实验方案,请补充下表:
课堂上老师按图1装置进行分子运动探究实验时,同学们闻到一股难闻的刺激性气味,课后在老师的指导下,化学兴趣小组对原实验装置进行了改进,并探究分子的运动及影响分子运动快慢的因素。
【进行实验】
改进装置如图2所示(夹持装置已省略)。在U形管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL酚酞溶液插入橡皮塞慢慢注入棉纱布B中,使其润湿;在另一管口插入吸取了2mL浓氨水的注射器并注入棉纱布A中。
【分析讨论】
(3)几分钟后看到的现象是_____ 。
(4)通过该实验可得出分子具有的特性是_____ 。
【拓展延伸】
同学们经过讨论后认为,仅通过上述实验并不能得出影响分子运动快慢的因素,于是又设计了两个实验。
实验1:
组装一套与图2装置完全相同的装置(如图3),并用热毛巾捂住插有浓氨水注射器的管口,用图2、图3装置同时进行实验。
(5)实验现象是_____ 。该现象说明分子运动速率与温度的关系是_____ 。
实验2:
已知氯化氢分子的质量大于氨气分子的质量。如图4将装置平放在桌面上,同时用注射器分别向棉纱布上注入等量的浓氨水和浓盐酸。过一会儿后,观察到产生的白烟并不是在U形管的中间位置,而在如图所示位置。
(6)该现象说明分子运动速率与分子质量的关系是_____ 。

如图1,烧杯甲中装有20mL蒸馏水,并滴入了几滴酚酞,在烧杯乙中装有10mL浓氨水。用一个大烧杯将甲、乙两个小烧杯罩在一起。一段时间后,甲烧杯中的溶液由无色变为红色。关于酚酞变红,同学们提出了三种猜想:
猜想一:从乙烧杯中蒸发出水蒸气,部分水分子运动进入甲烧杯,水使酚酞变红。
猜想二:从乙烧杯中挥发出氨气,部分氨气分子运动进入甲烧杯,氨气使酚酞变红。
猜想三:从乙烧杯中挥发出氨气,部分氨气分子运动进入甲烧杯与水结合形成氨水,氨水使酚酞变红。
(1)同学们经过讨论后一致认为猜想一是不可能的,理由是
(2)为了探究另外两种猜想是否正确,同学们设计了如下实验方案,请补充下表:
| 实验操作 | 实验现象 | 实验结论 | |
| 将一张滤纸浸入酚酞溶液中,1分钟后取出,悬挂在通风处晾干,用剪刀将其剪成两片 | 将其中一片干燥滤纸放入收集满氨气的集气瓶中 | 滤纸不变色 | 猜想 |
| 在另一片滤纸上滴几滴蒸馏水,再放入收集满氨气的集气瓶中 | 滤纸变成红色 | ||
课堂上老师按图1装置进行分子运动探究实验时,同学们闻到一股难闻的刺激性气味,课后在老师的指导下,化学兴趣小组对原实验装置进行了改进,并探究分子的运动及影响分子运动快慢的因素。
【进行实验】
改进装置如图2所示(夹持装置已省略)。在U形管的两个管口分别放入卷成筒状的棉纱布,并用橡皮塞塞紧。用注射器吸取2mL酚酞溶液插入橡皮塞慢慢注入棉纱布B中,使其润湿;在另一管口插入吸取了2mL浓氨水的注射器并注入棉纱布A中。
【分析讨论】
(3)几分钟后看到的现象是
(4)通过该实验可得出分子具有的特性是
【拓展延伸】
同学们经过讨论后认为,仅通过上述实验并不能得出影响分子运动快慢的因素,于是又设计了两个实验。
实验1:
组装一套与图2装置完全相同的装置(如图3),并用热毛巾捂住插有浓氨水注射器的管口,用图2、图3装置同时进行实验。
(5)实验现象是
实验2:
已知氯化氢分子的质量大于氨气分子的质量。如图4将装置平放在桌面上,同时用注射器分别向棉纱布上注入等量的浓氨水和浓盐酸。过一会儿后,观察到产生的白烟并不是在U形管的中间位置,而在如图所示位置。
(6)该现象说明分子运动速率与分子质量的关系是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】如图是铁丝在氧气中燃烧实验过程示意图,请回答下列问题。

(1)实验初探
取出一根细铁丝,用砂纸打磨至光亮,并绕成螺旋状,在下端系上一根火柴(如图B)。接着点燃火柴,当火柴快要熄灭时慢慢地伸入盛有少量水的集气瓶中(如图D),观察到铁丝剧烈燃烧,火星四射。
①用砂纸打磨铁丝的目的是_______ 。
②铁丝绕成螺旋状的原因是_______ 。
③写出铁丝在氧气中燃烧的文字或符号表达式_______ 。
(2)实验再探
某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积分数。

①已知试管剩余空间和导管的体积为40mL,导管截面积约为1cm2,形成稳定液柱时,读取读数为8.2cm。则空气中氧气的体积分数为_______ %。
②实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析:
【提出假设】假设一:溶液的pH不同;假设二:_______ 不同;
【进行实验】借助上述实验装置,通过取体积、浓度相同NaCl溶液调节溶液的pH获得了如下实验数据:
【实验结论】根据实验数据分析,为缩短实验测定时间,pH的最佳范围是_______ 。
(3)创新应用

①上图是某品牌暖宝宝的标签,暖宝宝发热的原因是袋内的铁粉与_______ 反应放热。外袋材料使用不透气塑料是为了_______ 。
②暖宝宝袋内使用极细的铁粉而不是铁块,其原因是_______ 。

(1)实验初探
取出一根细铁丝,用砂纸打磨至光亮,并绕成螺旋状,在下端系上一根火柴(如图B)。接着点燃火柴,当火柴快要熄灭时慢慢地伸入盛有少量水的集气瓶中(如图D),观察到铁丝剧烈燃烧,火星四射。
①用砂纸打磨铁丝的目的是
②铁丝绕成螺旋状的原因是
③写出铁丝在氧气中燃烧的文字或符号表达式
(2)实验再探
某化学学习小组借助下列装置(夹持装置已略)及相关试剂粗略测量空气中O2的体积分数。

①已知试管剩余空间和导管的体积为40mL,导管截面积约为1cm2,形成稳定液柱时,读取读数为8.2cm。则空气中氧气的体积分数为
②实验时发现上述测量过程因反应较慢耗时较长,对其影响因素作如下分析:
【提出假设】假设一:溶液的pH不同;假设二:
【进行实验】借助上述实验装置,通过取体积、浓度相同NaCl溶液调节溶液的pH获得了如下实验数据:
| pH | 2.0 | 5.5 | 6.0 | 6.5 | 7.0 | 8.0 |
| 液柱高度(cm) | 0 | 1.3 | 8.2 | 8.2 | 8.2 | 8.2 |
| 形成稳定液柱时间(min) | 3.0 | 3.0 | 5.1 | 5.3 | 15.6 | 17.5 |
(3)创新应用

①上图是某品牌暖宝宝的标签,暖宝宝发热的原因是袋内的铁粉与
②暖宝宝袋内使用极细的铁粉而不是铁块,其原因是
您最近一年使用:0次



