氧化亚铜(Cu2O)常用于红色玻璃染色剂,还用作陶瓷和搪瓷的着色剂。工业上一种以胆矾(CuSO4·5H2O)为原料制备Cu2O的流程如下。

已知:Cu2O在潮湿空气中会逐渐氧化成CuO;
(1)溶解时,需用玻璃棒搅拌的目的是______ 。
(2)沉淀时的反应原理为2CuSO4+ 3Na2SO3 Cu2O↓+2SO2↑+3
Cu2O↓+2SO2↑+3_____ 。
(3)沉淀时,反应温度和反应液pH对产品中Cu2O的含量影响分别如下图1和图2所示:

①根据图1,最佳反应温度为100℃,请分析该温度时Cu2O含量高的原因有________ 。
②根据图2,最佳pH为_____ ;若pH过高, 产品中会有______ (填化学式)杂质;若pH过低,产品中会有铜单质,则产品中铜元素的质量分数将______ (填 “偏大”、“偏小” 或“不变”)。
(4)检验沉淀是否洗涤干净的方法是_____ ;若无白色沉淀产生, 则已洗净。
(5)烘干时,若产品中出现少量黑色物质,可能的原因是_____ 。
(6)现有CuSO4·5H2O 10kg,最终制得Cu2O产品27.5kg,请计算所得产品的产率。(写出计算过程,结果精确到0.1%) (产品的产率=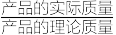 ×100%)
×100%)
(7)若所得产品的产率偏低,可能的原因有______(填字母) 。

已知:Cu2O在潮湿空气中会逐渐氧化成CuO;
(1)溶解时,需用玻璃棒搅拌的目的是
(2)沉淀时的反应原理为2CuSO4+ 3Na2SO3
 Cu2O↓+2SO2↑+3
Cu2O↓+2SO2↑+3(3)沉淀时,反应温度和反应液pH对产品中Cu2O的含量影响分别如下图1和图2所示:

①根据图1,最佳反应温度为100℃,请分析该温度时Cu2O含量高的原因有
②根据图2,最佳pH为
(4)检验沉淀是否洗涤干净的方法是
(5)烘干时,若产品中出现少量黑色物质,可能的原因是
(6)现有CuSO4·5H2O 10kg,最终制得Cu2O产品27.5kg,请计算所得产品的产率。(写出计算过程,结果精确到0.1%) (产品的产率=
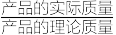 ×100%)
×100%)(7)若所得产品的产率偏低,可能的原因有______(填字母) 。
| A.溶解时,加的水过多 | B.反应物未完全沉淀 |
| C.过滤时,滤纸破损 | D.产品未洗涤干净 |
更新时间:2023-05-18 12:58:28
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】硅芯片是很多电子产品的核心。下图是某种制取硅反应的微观示意图。

(1)请写出该反应的化学方程式:___________ 。
(2)该反应的基本反应类型为___________ 。
(3)若要制取5.6g丙则至少需要甲的质量为___________ 。

(1)请写出该反应的化学方程式:
(2)该反应的基本反应类型为
(3)若要制取5.6g丙则至少需要甲的质量为
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
【推荐2】多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界。
(1)根据下表提供的信息,填写有关含碳物质的对应特性。
(2)液态二氧化碳灭火器可用于扑救档案资料室发生的火灾,下列说法正确的有____ (填标号)。
A 液态二氧化碳气化后不会污染档案资料
B 二氧化碳可覆盖在燃烧物表面,隔绝空气
C 液态二氧化碳气化时吸热,降低了可燃物的着火点
(3)过多的二氧化碳加剧了“温室效应”,写出一条减少二氧化碳排放的建议____ 。
(4)二氧化碳是一种宝贵的资源。固定和利用二氧化碳的一个成功范例是:在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水。该反应的化学方程式_______ .
(5)目前,人类以化石燃料为主要能源。化石燃料有煤、___ 和天然气,它们都属于___ (填“可再生”或“不可再生”)能源。
(6)从下表数据分析,与煤相比,用天然气作燃料的优点有____ 。
(7)天然气的主要成分是甲烷,甲烷不仅是重要的燃料,同时也是重要的化工原料,下图是以甲烷为原料,一定条件下制取某液体燃料的微观过程示意图。由此得出:进程I中参加反应的各物质分子个数比为____ ,进程Ⅱ反应的化学方程式为_____ 。

(1)根据下表提供的信息,填写有关含碳物质的对应特性。
| 物质用途 | 金刚石切割玻璃 | 石墨做电极 | 用炭黑等制墨汁 |
| 对应特征 | ① | ② | ③ |
A 液态二氧化碳气化后不会污染档案资料
B 二氧化碳可覆盖在燃烧物表面,隔绝空气
C 液态二氧化碳气化时吸热,降低了可燃物的着火点
(3)过多的二氧化碳加剧了“温室效应”,写出一条减少二氧化碳排放的建议
(4)二氧化碳是一种宝贵的资源。固定和利用二氧化碳的一个成功范例是:在高温高压下,CO2和NH3可以合成尿素[CO(NH2)2],同时生成水。该反应的化学方程式
(5)目前,人类以化石燃料为主要能源。化石燃料有煤、
(6)从下表数据分析,与煤相比,用天然气作燃料的优点有
| 1g物质完全燃烧 | ||
| 产生二氧化碳的质量/g | 放出的热量/KJ | |
| 甲烷 | 2.75 | 56 |
| 碳 | 3.67 | 32 |

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】从制造感光材料的含硝酸银的废液中提取贵金属银有重要的经济价值。某化学兴趣小组用 500g 废液(含 AgNO3,其他成分不与铁粉反应)回收金属 Ag,实验流程如下图所示(部分生成物已略去)。

(1)步骤 A 发生反应的化学方程式为______ ,该反应属于基本反应类型中的______ 反应;
(2)固体 X 成分为______ ;
(3)操作Ⅱ用到的玻璃仪器有烧杯、玻璃棒和______ (填仪器名称);
(4)经过洗涤、烘干后称量,获得 Ag 的质量为 21.6g,计算 500g 废液中硝酸银的质量为______ g。

(1)步骤 A 发生反应的化学方程式为
(2)固体 X 成分为
(3)操作Ⅱ用到的玻璃仪器有烧杯、玻璃棒和
(4)经过洗涤、烘干后称量,获得 Ag 的质量为 21.6g,计算 500g 废液中硝酸银的质量为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】2022年3月全国两会期间,“碳达峰”“碳中和”“能源”再度成为热词。
(1)下列不属于新能源的是________(填序号)。
(2)“碳中和”是指在一定时期内排放的二氧化碳等温室气体的总量,通过各种形式加以抵消,达到相对“零排放”,请写出一种可实现“碳中和”的措施________ 。
(3)2022北京冬奥会期间,大量不惧严寒的氢能源汽车几乎包揽了所有山区赛事的保障用车。氢化镁(MgH2)固体与水反应生成氢氧化镁和氢气,可为氢能源汽车提供能源,写出该反应的化学方程式_______ 。
(4) 是生活中常见的燃料,等质量的
是生活中常见的燃料,等质量的 分别与足量的氧气反应,消耗氧气的质量由多到少的顺序是
分别与足量的氧气反应,消耗氧气的质量由多到少的顺序是_______ 。
(1)下列不属于新能源的是________(填序号)。
| A.天然气 | B.风能 | C.太阳能 | D.地热能 |
(3)2022北京冬奥会期间,大量不惧严寒的氢能源汽车几乎包揽了所有山区赛事的保障用车。氢化镁(MgH2)固体与水反应生成氢氧化镁和氢气,可为氢能源汽车提供能源,写出该反应的化学方程式
(4)
 是生活中常见的燃料,等质量的
是生活中常见的燃料,等质量的 分别与足量的氧气反应,消耗氧气的质量由多到少的顺序是
分别与足量的氧气反应,消耗氧气的质量由多到少的顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】运用所学知识回答问题
(1)在自来水厂取水口管道入口处设有拦污栅,此处相当于实验基本操作中的_________ 。水厂工人在清理拦污栅的垃圾时经常发现有:①菜叶 ②纸皮 ③香蕉皮 ④易拉罐 ⑤塑料饮料瓶,其中可回收的有______ (填序号)。
(2)地球上总水量虽然很大,但淡水资源很少,我们必须爱护水资源,一方面要___________ ,另一方面要________ 。
(3)在常温下完全电解90mL的水,正极与负极产生的气体的体积比为______ ,产生氧气的质量为_____ 克(设常温下水的密度为1g/cm3)。
(1)在自来水厂取水口管道入口处设有拦污栅,此处相当于实验基本操作中的
(2)地球上总水量虽然很大,但淡水资源很少,我们必须爱护水资源,一方面要
(3)在常温下完全电解90mL的水,正极与负极产生的气体的体积比为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属及金属材料在生产、生活中有广泛的应用。
(1)我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于______________ (填“金属材料”或“合成材料”)。
(2)金、银在自然界有单质形式存在,说明他们的化学性质都______________ ,武德合金常用作保险丝,是因为合金的熔点比组成它的纯金属的熔点要______________ (填“高”或“低”)。
(3)镁铝合金被誉为“21世纪绿色金属结构材料”。一种镁铝合金Mg17A112是特殊的储氢材料,完全吸收氢气后得到MgH2和A1,该反应的化学方程式为______________ 。
(4)向硝酸铜、硝酸铝和硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤,滤液呈无色,则滤出的固体一定有______________ ,滤液中含有的金属离子是______________ (写离子符号)。
(5)若锌和镁混合物的质量为4.8g,与100g溶质质量分数为9.8%的稀硫酸恰好完全反应,则生成H2的质量为______________ g。
(1)我国自主研制的C919大型客机试飞成功,标志着我国飞机制造技术又有了新的突破。飞机外壳的主要材料是铝合金,“铝合金”属于
(2)金、银在自然界有单质形式存在,说明他们的化学性质都
(3)镁铝合金被誉为“21世纪绿色金属结构材料”。一种镁铝合金Mg17A112是特殊的储氢材料,完全吸收氢气后得到MgH2和A1,该反应的化学方程式为
(4)向硝酸铜、硝酸铝和硝酸银的混合溶液中加入一定量的锌粉,充分反应后过滤,滤液呈无色,则滤出的固体一定有
(5)若锌和镁混合物的质量为4.8g,与100g溶质质量分数为9.8%的稀硫酸恰好完全反应,则生成H2的质量为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D中均含同一种元素,它们的转化关系如图。其中A是白色难溶性固体,相对分子质量为100,金属元素的质量分数为40%;C常作干燥剂;D属于碱。

请分析回答下列问题。
(1)A转化为B的反应基本类型为_____ 。
(2)D的用途为_____ (写一种即可);
(3)A转化为C时,发生的化学反应方程式为_____ 。

请分析回答下列问题。
(1)A转化为B的反应基本类型为
(2)D的用途为
(3)A转化为C时,发生的化学反应方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐3】如图所示是六种物质(两种已经标出)间的反应及转化关系,用“一”表示两种物质能发生化学反应,用“→”表示一种物质可以通过一步反应转化为另一种物质。A、B、C、D四种物质中,A、B、C都含有相同的金属元素,且分别属于不同类别的化合物,其中A为一种黑色固体,B为一种蓝色固体,D物质为一种无色盐溶液。

(1)请在①②③④处写出字母序号和相应物质的化学式:①________ ;②________ ;③________ ;④________ 。
(2)写出③→②反应的化学方程式:________ 。

(1)请在①②③④处写出字母序号和相应物质的化学式:①
(2)写出③→②反应的化学方程式:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】(8分)氢能源是最具应用前景的能源之一,高纯氢的制备是目前的研究热点。
(1)实验室可用_____ 和_____ 反应制取氢气,写出反应的化学方程式_____ 。
(2)甲烷水蒸气催化重整是制高纯氢的方法之一、
①反应器中初始反应的生成物为H2和CO2,其化学计量数之比为4∶1,甲烷和水蒸气反应的方程式是_____ 。
②反应物投料比采用分子数目比为n(H2O)∶n(CH4)=4∶1,大于初始反应的化学计量数之比,目的是_____ (选填字母序号)。
A 促进CH4转化 B 促进CO转化为CO2 C 减少积炭生成
③用CaO可以去除CO2.H2体积分数和CaO消耗率随时间变化关系如图所示。

从t1时开始,H2体积分数显著降低,单位时间CaO消耗率_____ (填“升高”“降低”或“不变”)。
(3)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

①制O2时,连接_____ 。
②改变开关连接方式,可得H2。
(1)实验室可用
(2)甲烷水蒸气催化重整是制高纯氢的方法之一、
①反应器中初始反应的生成物为H2和CO2,其化学计量数之比为4∶1,甲烷和水蒸气反应的方程式是
②反应物投料比采用分子数目比为n(H2O)∶n(CH4)=4∶1,大于初始反应的化学计量数之比,目的是
A 促进CH4转化 B 促进CO转化为CO2 C 减少积炭生成
③用CaO可以去除CO2.H2体积分数和CaO消耗率随时间变化关系如图所示。

从t1时开始,H2体积分数显著降低,单位时间CaO消耗率
(3)可利用太阳能光伏电池电解水制高纯氢,工作示意图如下。通过控制开关连接K1或K2,可交替得到H2和O2。

①制O2时,连接
②改变开关连接方式,可得H2。
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
名校
解题方法
【推荐2】纳米海绵是一种新型环保清洁产品,具有网状多孔的结构,有良好的吸油能力、循环利用以及环境友好等特性,清洁过程中可以吸附物体表面污渍,可用于清洁茶垢、油垢等。
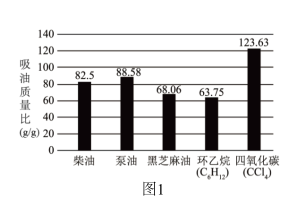
科学家测定了纳米海绵对不同油品的吸收能力(吸油质量比越高,其吸油能力越强),结果如图1所示。吸油能力的差异性取决于油品自身的密度。油品密度越大,纳米海绵的吸油能力越强。
依据科普内容回答下列问题。
(1)纳米海绵有_______ 等特性(写一点即可),可以吸附物体表面污渍的原因是_______ 。
(2)已知CCl4中氯元素为-1价,CCl4中碳元素的化合价为_______ 价。
(3)由图1可知,与黑芝麻油比较,柴油的吸油质量比更高,因此纳米海绵对柴油的吸收能力比黑芝麻油的_______ (填“强”或“弱”)。
(4)图2是纳米海绵和细菌纤维素循环吸油能力的对比,可得到的结论:在其它相同条件下,循环使用次数1~8之间时,随循环使用次数的增加,纳米海绵吸油能力变化不明显,细菌纤维素的吸油能力变_______ (填“好”或“差”)。

(5)下列说法正确的是_______ (多选,填字母)。
a.纳米海绵可用于清洁茶垢、油垢等
b.油品密度越大,纳米海绵的吸油能力越弱
c.化学科学的发展极大地推动了人类社会的进步
科学家测定了纳米海绵对不同油品的吸收能力(吸油质量比越高,其吸油能力越强),结果如图1所示。吸油能力的差异性取决于油品自身的密度。油品密度越大,纳米海绵的吸油能力越强。
依据科普内容回答下列问题。

(1)纳米海绵有
(2)已知CCl4中氯元素为-1价,CCl4中碳元素的化合价为
(3)由图1可知,与黑芝麻油比较,柴油的吸油质量比更高,因此纳米海绵对柴油的吸收能力比黑芝麻油的
(4)图2是纳米海绵和细菌纤维素循环吸油能力的对比,可得到的结论:在其它相同条件下,循环使用次数1~8之间时,随循环使用次数的增加,纳米海绵吸油能力变化不明显,细菌纤维素的吸油能力变

(5)下列说法正确的是
a.纳米海绵可用于清洁茶垢、油垢等
b.油品密度越大,纳米海绵的吸油能力越弱
c.化学科学的发展极大地推动了人类社会的进步
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】阅读下列短文。
碳在自然界中的循环变化,对于生态环境有极为重要的意义。随着工业生产的高速发展和人们生活水平的提高,排入大气中的 越来越多,导致温室效应增强。减少
越来越多,导致温室效应增强。减少 排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的主要途径。研究机构发明了转化大气中二氧化碳的技术,该技术是在一定条件下,二氧化碳和氢气反应生成甲醇
排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的主要途径。研究机构发明了转化大气中二氧化碳的技术,该技术是在一定条件下,二氧化碳和氢气反应生成甲醇 和水。甲醇的产率除受浓度、温度、压强等因素影响外,还受催化剂
和水。甲醇的产率除受浓度、温度、压强等因素影响外,还受催化剂 的质量分数影响(如图1)。“碳循环”(如图2)是指碳元素在地球上的生物圈、岩石圈、水圈及大气圈中交换,并随地球的运动循环不止的现象。
的质量分数影响(如图1)。“碳循环”(如图2)是指碳元素在地球上的生物圈、岩石圈、水圈及大气圈中交换,并随地球的运动循环不止的现象。
(2)写出 和
和 在催化剂条件下生成
在催化剂条件下生成 和水的化学方程式:
和水的化学方程式:_________ 。
(3)根据图1写出一条甲醇的产率与 质量分数的规律(或关系)
质量分数的规律(或关系)____________ 。
(4)请你谈一谈生活中实现“碳中和”具体措施________ (写一条)。
碳在自然界中的循环变化,对于生态环境有极为重要的意义。随着工业生产的高速发展和人们生活水平的提高,排入大气中的
 越来越多,导致温室效应增强。减少
越来越多,导致温室效应增强。减少 排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的主要途径。研究机构发明了转化大气中二氧化碳的技术,该技术是在一定条件下,二氧化碳和氢气反应生成甲醇
排放,实现碳中和,已成为全球共识。碳替代、碳减排、碳封存、碳循环是实现碳中和的主要途径。研究机构发明了转化大气中二氧化碳的技术,该技术是在一定条件下,二氧化碳和氢气反应生成甲醇 和水。甲醇的产率除受浓度、温度、压强等因素影响外,还受催化剂
和水。甲醇的产率除受浓度、温度、压强等因素影响外,还受催化剂 的质量分数影响(如图1)。“碳循环”(如图2)是指碳元素在地球上的生物圈、岩石圈、水圈及大气圈中交换,并随地球的运动循环不止的现象。
的质量分数影响(如图1)。“碳循环”(如图2)是指碳元素在地球上的生物圈、岩石圈、水圈及大气圈中交换,并随地球的运动循环不止的现象。
A. 的产生途径主要有化石燃料的燃烧、动植物的呼吸作用和绿色植物的光合作用 的产生途径主要有化石燃料的燃烧、动植物的呼吸作用和绿色植物的光合作用 |
B.碳循环和氧循环分别是指 和 和 的循环 的循环 |
| C.碳循环和氧循环过程中均发生了化学反应 |
(2)写出
 和
和 在催化剂条件下生成
在催化剂条件下生成 和水的化学方程式:
和水的化学方程式:(3)根据图1写出一条甲醇的产率与
 质量分数的规律(或关系)
质量分数的规律(或关系)(4)请你谈一谈生活中实现“碳中和”具体措施
您最近一年使用:0次

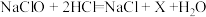 ,则X的化学式为
,则X的化学式为

