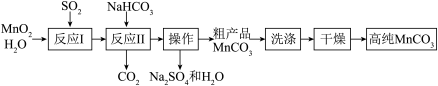
实验室以MnO2为原料制备少量高纯MnCO3的流程如下:
已知:①反应Ⅰ的化学方程式:MnO2+SO2=MnSO4;②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解,NaHCO3溶液呈碱性。
(1)流程图中“操作”的名称为_______ ;该操作需要的玻璃仪器有烧杯、玻璃棒和_______ ;
(2)反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有______ (填化学式)。
(3)为获得高纯MnCO3,需选择“低温”干燥的原因是_______ 。

已知:①反应Ⅰ的化学方程式:MnO2+SO2=MnSO4;②MnCO3、Mn(OH)2均难溶于水,MnCO3在100℃时开始分解,NaHCO3溶液呈碱性。
(1)流程图中“操作”的名称为
(2)反应Ⅱ需控制溶液的酸碱性,若碱性过强,MnCO3粗产品中将混有
(3)为获得高纯MnCO3,需选择“低温”干燥的原因是
更新时间:2023-05-27 08:35:31
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】我省海洋资源十分丰富。
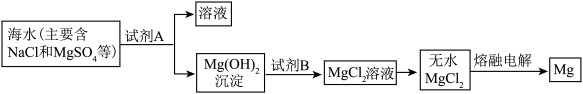
(1)目前世界上60%的镁是从海水中提取的。其主要步骤如下:提取Mg的过程中,试剂A可以选用______ ,由无水MgCl2制取Mg的反应类型为______ 。
(2)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是______ 。

(1)目前世界上60%的镁是从海水中提取的。其主要步骤如下:提取Mg的过程中,试剂A可以选用
(2)目前海水淡化普遍采用“多级闪急蒸馏法”,证明蒸馏得到的水为淡水的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】金属镍(Ni)是电动车动力电池制造的关键原料。近期镍价上升引发了新能源汽车价格上涨。已知:镍的金属活动性介于铁和锡之间,镍元素在化合物中常见化合价为+2价,20℃时,硫酸镍易溶于水,氢氧化镍和碳酸镍难溶于水。
(1)根据金属化学性质的一般规律,下列关于镍的化学性质预测合理的是___________(填标号)。
(2)下图是以碳酸镍(NiCO3)为原料制取硫酸镍晶体的过程,请回答相关问题:

①结合所学知识预测,试剂A属于___________ 。(填物质类别)
②系列操作包括加入适量的硫酸。目的之一为控制硫酸镍溶液的pH,以稳定硫酸镍晶体的质量。若过程中硫酸加入过量,现需减少该硫酸镍溶液中硫酸的量,请设计下列减少硫酸的方案(要求依据两种不同的反应规律)。完成下表:
(1)根据金属化学性质的一般规律,下列关于镍的化学性质预测合理的是___________(填标号)。
| A.一定条件下,镍能与氧气反应 |
| B.镍能与稀盐酸反应 |
| C.高温时,CO能将氧化镍转化为金属镍 |
| D.镁放入硫酸镍溶液无明显变化 |
(2)下图是以碳酸镍(NiCO3)为原料制取硫酸镍晶体的过程,请回答相关问题:

①结合所学知识预测,试剂A属于
②系列操作包括加入适量的硫酸。目的之一为控制硫酸镍溶液的pH,以稳定硫酸镍晶体的质量。若过程中硫酸加入过量,现需减少该硫酸镍溶液中硫酸的量,请设计下列减少硫酸的方案(要求依据两种不同的反应规律)。完成下表:
| 方案 | 试剂 | 预测反应的化学方程式 | 依据的反应规律 |
| Ⅰ | Ni | 活泼金属与酸反应,生成盐和氢气 | |
| Ⅱ | 略 | ||
| Ⅲ | 略 |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】硫酸铜晶体常用作农业和渔业的杀虫剂、杀菌剂,如图所示是由废铜料(含铁)生产硫酸铜晶体的流程。

(1)操作a的名称是________ 。
(2)②的反应基本类型为________ ;反应①、③的化学方程式分别为①________ ;③________ 。
(3)已知: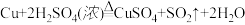 ,从环保和经济的角度分析,对比途径Ⅰ、Ⅱ,途径Ⅰ的优点有:不产生有害气体和
,从环保和经济的角度分析,对比途径Ⅰ、Ⅱ,途径Ⅰ的优点有:不产生有害气体和________ 。

(1)操作a的名称是
(2)②的反应基本类型为
(3)已知:
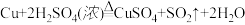 ,从环保和经济的角度分析,对比途径Ⅰ、Ⅱ,途径Ⅰ的优点有:不产生有害气体和
,从环保和经济的角度分析,对比途径Ⅰ、Ⅱ,途径Ⅰ的优点有:不产生有害气体和
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】Na2SO4是制造纸张、药品、染料稀释剂的重要原料。某Na2SO4样品中含有少量CaCl2和MgCl2,实验室提纯Na2SO4的流程如下图所示。
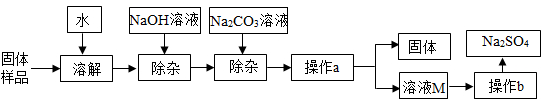
(1)加入NaOH溶液主要除去的阳离子是________ (填离子符号),其反应的化学方程式为______ 。
(2)若加入的NaOH溶液和Na2CO3溶液都过量,可在后续的流程中加入适量的______ (填名称)除去。
(3)操作a的名称是_______ ,该操作中需要用到的玻璃仪器有烧杯、玻璃棒、_________ 。
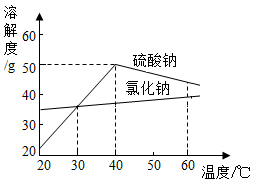
(4)若溶液M中的溶质是Na2SO4和NaCl,根据下图的溶解度曲线可知,操作b应为:先将溶液M____ ,再降温结晶、过滤。降温结晶的最佳温度范围是____ ℃以下,这是因为____________ 。

(1)加入NaOH溶液主要除去的阳离子是
(2)若加入的NaOH溶液和Na2CO3溶液都过量,可在后续的流程中加入适量的
(3)操作a的名称是
(4)若溶液M中的溶质是Na2SO4和NaCl,根据下图的溶解度曲线可知,操作b应为:先将溶液M

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】以FeSO4•7H2O为原料制备铁红(Fe2O3)的一种方法如图:
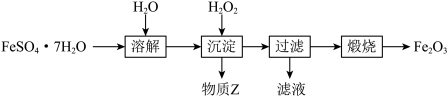
(1)“溶解”时能加快溶解的方法有______ (写一种)。
(2)“沉淀”时的主要反应为: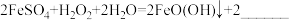
______ 标出 中铁元素的化合价
中铁元素的化合价______ 。“沉淀”时反应温度不宜过高,其原因是______ 。
(3)“过滤”后需对固体进行洗涤与干燥。实验室进行过滤时需要的玻璃仪器有烧杯、玻璃棒和______ ,其中玻璃棒的作用是______ 。检验沉淀是否洗涤干净应选用的试剂是______ (填化学式)。
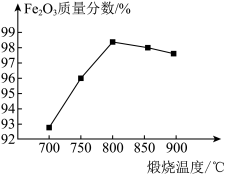
(4)“煅烧”时反应的化学方程式为______ 。如图为其他条件相同时不同煅烧温度对产品中Fe2O3质量分数的影响。最适宜的煅烧温度为______ ℃,若煅烧后所得产品发黑,其可能原因是______ 。

(1)“溶解”时能加快溶解的方法有
(2)“沉淀”时的主要反应为:
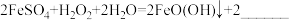
 中铁元素的化合价
中铁元素的化合价(3)“过滤”后需对固体进行洗涤与干燥。实验室进行过滤时需要的玻璃仪器有烧杯、玻璃棒和
(4)“煅烧”时反应的化学方程式为

您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
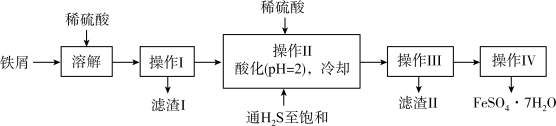
【推荐1】铁元素是人体血液中血红蛋白的重要组成元素。绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。下面是以某工厂的铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
查询资料,得有关物质的相关数据如下表:
(1)操作Ⅰ的名称是_________ 。
(2)为了提高溶解的速率,可采用的措施是_______ (填一种即可)。
(3)已知金属活动性:铁>锡>氢,请写出稀硫酸与锡(反应后为+2价)发生反应的化学方程式________ 。
(4)通过分析查阅资料数据,操作Ⅱ中通入硫化氢至饱和并且用硫酸酸化至pH=2的目的之一是_____ 。
(5)操作Ⅳ得到的绿矾晶体用少量水洗涤,洗涤的目的是_________ 。

查询资料,得有关物质的相关数据如下表:
| 25℃时 | 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
(1)操作Ⅰ的名称是
(2)为了提高溶解的速率,可采用的措施是
(3)已知金属活动性:铁>锡>氢,请写出稀硫酸与锡(反应后为+2价)发生反应的化学方程式
(4)通过分析查阅资料数据,操作Ⅱ中通入硫化氢至饱和并且用硫酸酸化至pH=2的目的之一是
(5)操作Ⅳ得到的绿矾晶体用少量水洗涤,洗涤的目的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在生产生活中用途广泛,如碳酸亚铁(FeCO3)可用作补血剂。工业上可用硫酸厂的炉渣(含Fe2O3、FeO、SiO2)制备FeCO3。其流程如图:
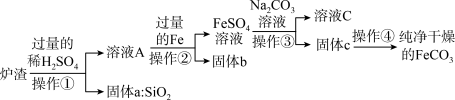
已知:Na2CO3+FeSO4=FeCO3↓+Na2SO4
(1)要提高炉渣与稀硫酸的反应速率,可采用的措施有______ (填1条)。
(2)溶液A的溶质有______ 种;往A中加入过量Fe,发生化合反应得到FeSO4溶液的方程式为______ 。
(3)已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀,现用1%的Na2CO3溶液(溶液pH≈11.62,浓度越大,碱性越强)在烧杯中制备FeCO3,应选用的加料方式是 (填字母)
(4)若整个流程共消耗10%的硫酸0.49t。
①需要98%的浓硫酸______ t。
②理论上最后得到的FeCO3质量最多为______ t。

已知:Na2CO3+FeSO4=FeCO3↓+Na2SO4
(1)要提高炉渣与稀硫酸的反应速率,可采用的措施有
(2)溶液A的溶质有
(3)已知溶液pH大于8.8时,Fe2+完全生成Fe(OH)2沉淀,现用1%的Na2CO3溶液(溶液pH≈11.62,浓度越大,碱性越强)在烧杯中制备FeCO3,应选用的加料方式是 (填字母)
| A.将FeSO4溶液与Na2CO3溶液同时加入烧杯中 |
| B.将Na2CO3溶液缓慢加入盛有FeSO4溶液的烧杯中 |
| C.将FeSO4溶液缓慢加入盛有Na2CO3溶液的烧杯中 |
(4)若整个流程共消耗10%的硫酸0.49t。
①需要98%的浓硫酸
②理论上最后得到的FeCO3质量最多为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
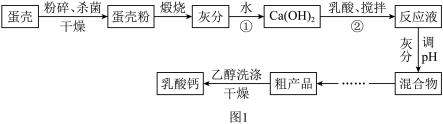
【推荐3】我国是全球规模最大的禽蛋生产国和消费国。对蛋壳中的钙源(主要成分是CaCO3)进行回收利用,可以变废为宝。蛋壳高温煅烧法制备乳酸钙的工艺流程如图1:
(1)将蛋壳粉碎的目的是_______ 。
(2)写出反应①的化学方程式_______ 。
(3)已知反应②:Ca(OH)2+2CH3CH(OH)COOH(乳酸)=Ca[CH3CH(OH)COO]2(乳酸钙)+2X,请写出X的化学式_______ ;调节pH时,常用_______ 测量溶液的pH。
(4)乳酸钙产率与温度的关系如图2所示,则灰分与乳酸反应时,反应的最佳温度是_______ ,用乙醇洗涤粗产品,而不用水洗涤的原因是_______ 。
(1)将蛋壳粉碎的目的是
(2)写出反应①的化学方程式
(3)已知反应②:Ca(OH)2+2CH3CH(OH)COOH(乳酸)=Ca[CH3CH(OH)COO]2(乳酸钙)+2X,请写出X的化学式
(4)乳酸钙产率与温度的关系如图2所示,则灰分与乳酸反应时,反应的最佳温度是

您最近一年使用:0次