在下列溶液中离子可以大量共存的是
A.Cu+;H+;K+; | B.Ag+;Na+;Cl-; |
| C.H+;Na+;Ba2+;OH- | D.K+;Ba2+; ;OH- ;OH- |
更新时间:2023-05-27 15:48:53
|
【知识点】 复分解反应发生的条件解读
相似题推荐
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐1】我国化学家侯德榜所创立的侯氏联合制碱波,既提高了原料利用率,又“变废为宝”,降低了生产成本,促进了世界制碱技术的发展。侯氏联合制碱法的部分工艺流程如图1。图2为NH4Cl、NaCl、NaHCO3三种物质的溶解度曲线。回答下列问题:
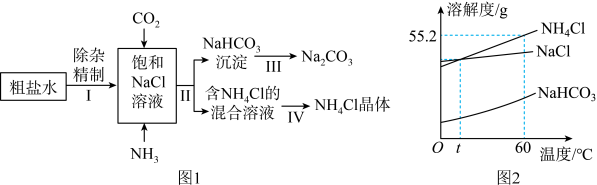
(1)粗盐水中主要含有Na2SO4、MgCl2、CaCl2 三种可溶性杂质,工业上常用加入稍过量的____________ (填化学式,下同)溶液、NaOH溶液、______ 溶液及适量的盐酸等除杂、精制。
(2)Ⅱ中发生反应的化学方程式为______ 。
(3)碳酸氢钠晶体首先从溶液中析出的原因是______ 。
(4)从含氯化铵的混合溶液中得到氯化铵晶体的操作为:蒸发浓缩、______ 过滤、洗涤、干燥。
(5)实验过程中先通入足量氨气,再缓慢通入二氧化碳。先通氨气后通二氧化碳的主要原因是______ 。
(6)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是______(填字母)。

(1)粗盐水中主要含有Na2SO4、MgCl2、CaCl2 三种可溶性杂质,工业上常用加入稍过量的
(2)Ⅱ中发生反应的化学方程式为
(3)碳酸氢钠晶体首先从溶液中析出的原因是
(4)从含氯化铵的混合溶液中得到氯化铵晶体的操作为:蒸发浓缩、
(5)实验过程中先通入足量氨气,再缓慢通入二氧化碳。先通氨气后通二氧化碳的主要原因是
(6)将60℃时氯化铵和氯化钠的饱和溶液各100g分别蒸发掉10g水,然后降温至t℃,过滤,得到溶液甲和溶液乙,下列说法正确的是______(填字母)。
| A.甲和乙都是饱和溶液 | B.溶剂的质量:甲<乙 |
| C.溶液的质量:甲>乙 | D.溶质的质量分数:甲=乙 |
您最近一年使用:0次
【推荐2】通过分析表格、总结规律及含义是培养学生能力的重要手段。下表是“部分酸、碱、盐在20℃时的溶解性”。请回答下列问题:
(1)写出碳酸钠溶液与氯化钡溶液反应的化学方程式_______ ;该反应的基本反应类型为___________ 。
(2)氯化钠溶液___________ (填“能”或“不能”)与硝酸钡溶液发生反应,判断理由是___________ 。
(3)下列各组离子在溶液中不能大量共存的是___________ (填编号)。
A.Na+、Ba2+、 、Cl-
、Cl-
B.Cu2+、 、Ba2+、Cl-
、Ba2+、Cl-
C.Mg2+、 、OH-、Na+
、OH-、Na+
D.H+、Ba2+、Cl-、
| OH- |  | Cl- |  |  | |
| H+ | - | 溶、挥 | 溶、挥 | 溶、挥 | 溶 |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Mg2+ | 不 | 溶 | 溶 | 微 | 溶 |
(2)氯化钠溶液
(3)下列各组离子在溶液中不能大量共存的是
A.Na+、Ba2+、
 、Cl-
、Cl-B.Cu2+、
 、Ba2+、Cl-
、Ba2+、Cl-C.Mg2+、
 、OH-、Na+
、OH-、Na+D.H+、Ba2+、Cl-、

您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】学习了物质分类与转化规律后,某同学绘制了部分物质间相互反应的关系图。图中阴影部分表示相邻两类物质的反应。

(1)在阴影部分①②③④中,属于中和反应的为__________ (填序号);写出符合反应②的一个化学方程式_________ ,该反应属于________ (填基本反应类型)。
(2)反应③属于复分解反应,依据反应条件判断能否利用“氢氧化锌与硫酸铜反应制取硫酸锌”?(若能,请写出化学方程式;若不能请解释原因)________ 。
(3)宏观和微观相联系是化学独特的思维方式,根据下列微观示意图回答问题:
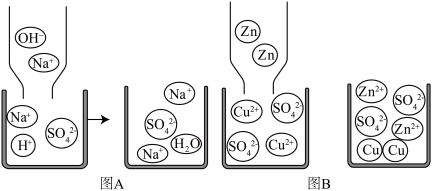
从微粒的角度说明图A反应的实质是_________ ;图B所示反应中,参加反应的微粒是________ (写出微粒的符号),该反应对应上图中阴影部分________ (填序号①②③④)。

(1)在阴影部分①②③④中,属于中和反应的为
(2)反应③属于复分解反应,依据反应条件判断能否利用“氢氧化锌与硫酸铜反应制取硫酸锌”?(若能,请写出化学方程式;若不能请解释原因)
(3)宏观和微观相联系是化学独特的思维方式,根据下列微观示意图回答问题:

从微粒的角度说明图A反应的实质是
您最近一年使用:0次



