在 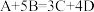 的反应中,已知 11g 物质 A 完全反应生成 33g 物质 C 和 18g 物质 D。若B 的相对分子质量为 32,试计算物质 A 的相对分子质量。
的反应中,已知 11g 物质 A 完全反应生成 33g 物质 C 和 18g 物质 D。若B 的相对分子质量为 32,试计算物质 A 的相对分子质量。
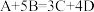 的反应中,已知 11g 物质 A 完全反应生成 33g 物质 C 和 18g 物质 D。若B 的相对分子质量为 32,试计算物质 A 的相对分子质量。
的反应中,已知 11g 物质 A 完全反应生成 33g 物质 C 和 18g 物质 D。若B 的相对分子质量为 32,试计算物质 A 的相对分子质量。
21-22九年级下·安徽芜湖·自主招生 查看更多[3]
2022年安徽省芜湖一中高一自主招生化学试题(已下线)课堂例题(沪教版)第4章第3节化学方程式的书写与应用A卷2023-2024九化同步课题例题与随堂检测AB卷(沪教上册)山东省烟台市经济技术开发区2023-2024学年八年级下学期期中考试化学试卷
更新时间:2023-05-28 17:51:05
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某小组同学用氯酸钾和二氧化锰的混合物制取 ,并记录下不同时间试管内固体的质量,小华代表小组同学进行了分享:
,并记录下不同时间试管内固体的质量,小华代表小组同学进行了分享:
(1)观点分享:t4之后试管中固体的质量不再改变,原因是______ 。
(2)展示交流:该混合物中氯酸钾的质量是多少?请在答题卡上写出解题过程。
 ,并记录下不同时间试管内固体的质量,小华代表小组同学进行了分享:
,并记录下不同时间试管内固体的质量,小华代表小组同学进行了分享:时间 | 0 | t1 | t2 | t3 | t4 | t5 |
试管中固体质量/g | 6 | 5.8 | 5.6 | 5.3 | 5.04 | 5.04 |
(2)展示交流:该混合物中氯酸钾的质量是多少?请在答题卡上写出解题过程。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定贺兰山石样品中碳酸钙的含量,某校实验室取10.0g样品于烧杯中,向其中加入稀盐酸50.0g,恰好完全反应(杂质不参与反应),反应后烧杯中物质的总质量为57.8g。请计算:
(1)生成二氧化碳的质量为___________ g。
(2)计算加入的稀盐酸溶液中溶质的质量分数。
(1)生成二氧化碳的质量为
(2)计算加入的稀盐酸溶液中溶质的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】化学实践小组的同学们在老师的指导下设计了一款简易制氧器,其原理图如图所示。
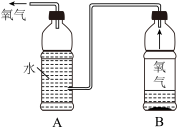
(1)观点分享:利用上图装置制取氧气,反应原理为_______ (填文字表达式)。A塑料瓶中利用氧气_______ 溶于水的原理,使氧气湿润。
(2)展示交流:已知每68份质量的过氧化氢完全反应可生成32份质量的氧气,若要获取6.72L氧气(在标准状况下,氧气的密度为1.429g/L),需要过氧化氢的质量是多少?(结果精确到0.1g)

(1)观点分享:利用上图装置制取氧气,反应原理为
(2)展示交流:已知每68份质量的过氧化氢完全反应可生成32份质量的氧气,若要获取6.72L氧气(在标准状况下,氧气的密度为1.429g/L),需要过氧化氢的质量是多少?(结果精确到0.1g)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】为了测定某种贝壳中碳酸钙的质量分数,取贝壳10克,加入100克7.3%的盐酸溶液,充分反应后,称得剩余物质的总质量为106.48克(假设贝壳中其它物质不与盐酸反应)。小军认为,根据上述实验数据,可按如下方案计算:根据“100克7.3%的盐酸溶液”,得出参加反应的盐酸质量,再求得碳酸钙的质量,最后求出贝壳中碳酸钙的质量分数。
(1)小明认为此方案不正确。你认为他的理由是______________ 。
(2)计算贝壳中碳酸钙的质量分数_________ 。
(1)小明认为此方案不正确。你认为他的理由是
(2)计算贝壳中碳酸钙的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】我国航天事业发展迅猛。若你是航天科技人员,请试着解决空间站二氧化碳和水再利用的问题。
(1)空间站里的二氧化碳主要产生于人的呼吸,请完成下列产生CO2的化学方程式: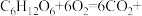
_______ 。
(2)空间站中科学家采用水气整合系统实现CO2的清除和O2的再生,流程如图所示。反应器1发生的反应: ;反应器2发生的反应:
;反应器2发生的反应: ;若消耗0.22吨二氧化碳,则会产生多少甲烷?
;若消耗0.22吨二氧化碳,则会产生多少甲烷?_______ (填“能”或“不能”)完全实现水的循环,理由是_______ 。
(1)空间站里的二氧化碳主要产生于人的呼吸,请完成下列产生CO2的化学方程式:
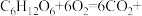
(2)空间站中科学家采用水气整合系统实现CO2的清除和O2的再生,流程如图所示。反应器1发生的反应:
 ;反应器2发生的反应:
;反应器2发生的反应: ;若消耗0.22吨二氧化碳,则会产生多少甲烷?
;若消耗0.22吨二氧化碳,则会产生多少甲烷?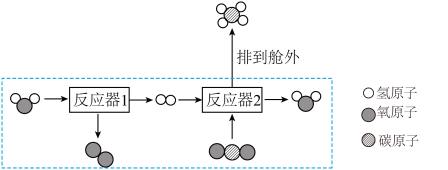
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】如图是诺氟沙星胶囊的说明书,某患者遵医嘱,每次服用诺 氟沙星胶囊400mg,一段时间后病情有了好转.请回答以下问题:
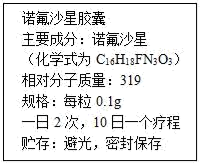
(1)诺氟沙星分子中碳、氢的原子个数比为_____.
(2)诺氟沙星分子中碳元素的质量分数是_____(精确到0.1%).
(3)从组成上可知诺氟沙星属于_____(填“有机化合物”或“无机化合物”);患者一个疗程共服用了_____粒诺氟沙星.摄入了_____mg氟元素.

(1)诺氟沙星分子中碳、氢的原子个数比为_____.
(2)诺氟沙星分子中碳元素的质量分数是_____(精确到0.1%).
(3)从组成上可知诺氟沙星属于_____(填“有机化合物”或“无机化合物”);患者一个疗程共服用了_____粒诺氟沙星.摄入了_____mg氟元素.
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】钢铁产业是工业发展的基础。工业上主要利用一氧化碳还原赤铁矿(主要成分为Fe2O3)冶炼金属铁,其反应原理为Fe2O3+3CO 2Fe + 3CO2。
2Fe + 3CO2。
(1)Fe2O3中铁元素的质量分数为______ 。
(2)参加反应的CO和生成的CO2的分子个数比为______ 。
(3)要冶炼制得112tFe,计算理论上需要的CO的质量_____ 。
 2Fe + 3CO2。
2Fe + 3CO2。(1)Fe2O3中铁元素的质量分数为
(2)参加反应的CO和生成的CO2的分子个数比为
(3)要冶炼制得112tFe,计算理论上需要的CO的质量
您最近一年使用:0次



