进一步了解金属的性质,才能使金属材料更好的为人类服务。
(1)金属的物理性质建造高铁使用了大量的铝合金,该合金的物理性质有___________ (填一条)。
(2)金属的化学性质:
①铝制品在空气中不易锈蚀的原因是___________ (用化学方程式表示)。
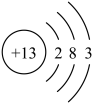
②如图是铝原子的结构示意图,最外层电子数是___________ ,在化学反应中容易___________ 电子变成阳离子,化学性质比较活泼。
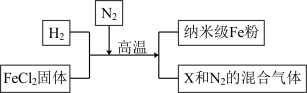
(3)新型金属材料的研发,如图新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如图所示,请回答下列问题:
①纳米级Fe粉在氧气中能容易燃烧生成黑色固体,此黑色固体的化学式为___________ 。
②在制备纳米级Fe粉的工艺流程中,N2不参与反应,则N2作用是___________ 。
③研究人员发现最后制得的纳米级Fe粉样品中混有少量的FeCl2杂质,请设计实验方案除去杂质,方案是___________ 。
(1)金属的物理性质建造高铁使用了大量的铝合金,该合金的物理性质有
(2)金属的化学性质:
①铝制品在空气中不易锈蚀的原因是
②如图是铝原子的结构示意图,最外层电子数是

(3)新型金属材料的研发,如图新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如图所示,请回答下列问题:

①纳米级Fe粉在氧气中能容易燃烧生成黑色固体,此黑色固体的化学式为
②在制备纳米级Fe粉的工艺流程中,N2不参与反应,则N2作用是
③研究人员发现最后制得的纳米级Fe粉样品中混有少量的FeCl2杂质,请设计实验方案除去杂质,方案是
更新时间:2023-06-13 15:12:05
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2020年5月31日下午4时53分,我国在酒泉卫星发射中心使用长征二号丁运载火箭,成功将高分九号02星、和德四号卫星送入预定轨道,发射取得圆满成功。

(1)长征二号丁运载火箭的某些机器零件使用硬铝,硬铝的主要成分是_______ 和镁。工业上常采用电解氯化镁的方式冶炼镁,此反应前后镁元素的化合价分别为______ 。用硬铝作为制造火箭的材料,是利用了硬铝______ (填字母)的性质。
A 硬度好、强度好
B 光泽好、弹性好
C 不易老化、不导电
(2)长征二号丁运载火箭采用四氧化二氮和偏二甲肼(C2H8N2)作为推进剂,二者混合后剧烈反应,放出巨大的能量,并生成水、二氧化碳和空气中含量最高的气体,请写出此反应的化学方程式____ ,火箭升空过程中的能量转化为______ (用“→”表示转化)。

(1)长征二号丁运载火箭的某些机器零件使用硬铝,硬铝的主要成分是
A 硬度好、强度好
B 光泽好、弹性好
C 不易老化、不导电
(2)长征二号丁运载火箭采用四氧化二氮和偏二甲肼(C2H8N2)作为推进剂,二者混合后剧烈反应,放出巨大的能量,并生成水、二氧化碳和空气中含量最高的气体,请写出此反应的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】物质的性质决定其用途,从下列物质中选择适当的序号填空:
①钛合金 ②氮气 ③干冰 ④甲烷 ⑤红磷
(1)用于人工降雨的是_______ 。
(2)用于食品保护气的是_______ 。
(3)用于制人造骨骼的是_______ 。
(4)用于作燃料的是_______ 。
(5)用于测定空气中氧气含量的是_______ 。
①钛合金 ②氮气 ③干冰 ④甲烷 ⑤红磷
(1)用于人工降雨的是
(2)用于食品保护气的是
(3)用于制人造骨骼的是
(4)用于作燃料的是
(5)用于测定空气中氧气含量的是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】金属制品与我们的日常生活密不可分,请回答下列问题。
(1)有镁、锌、银三种金属,与同浓度稀硫酸发生反应,最剧烈的是_____ (填化学式)。
(2)合金比纯金属有更广泛的用途,下列属于合金的_____ (填字母)。
A 不锈钢 B 水银 C 黄铜 D 金刚石
(3)为验证Zn、Cu、Ag三种金属的活动性顺序,某同学选用如下试剂组进行实验,其中不合理的一组_____ (填序号)。
①Zn、Ag、CuSO4溶液 ②Cu、AgNO3溶液、ZnSO4溶液 ③Ag、Cu、ZnSO4溶液
(4)已知金属单质的活泼性Fe>Cu,则Fe+CuSO4=Cu+FeSO4,非金属单质与金属单质有类似性质,活泼性Cl2>Br2,将Cl2通入NaBr溶液中发生反应的化学方程式为_____ 。
(1)有镁、锌、银三种金属,与同浓度稀硫酸发生反应,最剧烈的是
(2)合金比纯金属有更广泛的用途,下列属于合金的
A 不锈钢 B 水银 C 黄铜 D 金刚石
(3)为验证Zn、Cu、Ag三种金属的活动性顺序,某同学选用如下试剂组进行实验,其中不合理的一组
①Zn、Ag、CuSO4溶液 ②Cu、AgNO3溶液、ZnSO4溶液 ③Ag、Cu、ZnSO4溶液
(4)已知金属单质的活泼性Fe>Cu,则Fe+CuSO4=Cu+FeSO4,非金属单质与金属单质有类似性质,活泼性Cl2>Br2,将Cl2通入NaBr溶液中发生反应的化学方程式为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国正在以改革创新推进汽车转型,新能源汽车发展成为主要趋势。
(1)纯电动汽车、混合动力汽车、燃料电池电动汽车等属于新能源汽车。纯电动汽车和传统能源汽车相比,其优点是__________ (答一条即可)。
(2)钴酸锂(LiCoO2)电池是一种常见的新能源汽车电池。已知LiCoO2中锂元素的化合价为+1,则钴元素的化合价为_____________ 。
(3)氢燃料电池汽车将化学能转化为电能来提供动力,氢气燃烧的化学方程式为_______________ 。
(4)新能源汽车采用铝基复合材料制动盘使汽车轻量化。铝具有很好的抗腐蚀性,是因为其表面生成一层致密的薄膜,该薄膜是__________ (填化学式)。
(1)纯电动汽车、混合动力汽车、燃料电池电动汽车等属于新能源汽车。纯电动汽车和传统能源汽车相比,其优点是
(2)钴酸锂(LiCoO2)电池是一种常见的新能源汽车电池。已知LiCoO2中锂元素的化合价为+1,则钴元素的化合价为
(3)氢燃料电池汽车将化学能转化为电能来提供动力,氢气燃烧的化学方程式为
(4)新能源汽车采用铝基复合材料制动盘使汽车轻量化。铝具有很好的抗腐蚀性,是因为其表面生成一层致密的薄膜,该薄膜是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】小亮和父母利用假日到郊外野炊,在野炊过程中遇到一些有趣的化学问题。
(1)小亮在郊外闻到淡淡的花香,从微观角度分析其原因是____________ 。
(2)野炊时,他取来一些清澈的泉水,加热煮沸。从化学角度分析,给泉水加热煮沸既可以消毒杀菌,又可以____________ 。
(3)做饭结束后,为了防止火灾,必须将柴火熄灭,可采用的一种灭火方法是___________ 。
(4)他在喝饮料时,发现盛装饮料的易拉罐是铝制的,于是他联想到铝具有优良的抗腐蚀性能,其原因是___________ (用化学方程式表示)。
(1)小亮在郊外闻到淡淡的花香,从微观角度分析其原因是
(2)野炊时,他取来一些清澈的泉水,加热煮沸。从化学角度分析,给泉水加热煮沸既可以消毒杀菌,又可以
(3)做饭结束后,为了防止火灾,必须将柴火熄灭,可采用的一种灭火方法是
(4)他在喝饮料时,发现盛装饮料的易拉罐是铝制的,于是他联想到铝具有优良的抗腐蚀性能,其原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】氯化钙(CaCl2)可用作干燥剂、混凝土防冻剂等。实验室用工业大理石(含少量Al2O3、Fe2O3、SiO2等杂质)制备氯化钙的主要流程如图所示。

资料链接:①SiO2不溶于水,不溶于稀盐酸,不与稀盐酸反应;
②CaCl2.6H2O的溶解度随温度的升高而增大。
回答问题:
(1)配制31%的盐酸730g, 需要36.5%的浓盐酸___ g。
(2)酸溶时碳酸钙参与反应的化学方程式为_____ 。
(3)滤渣I的成分为_______ (填化学式,下同),滤渣II含有Al(OH)3和_______ 。
(4)操作I采用的方法是:蒸发浓缩、_______ 、过滤。
(5)加入试剂a中和稍过量的石灰水,该反应的化学方程式__________ 。

资料链接:①SiO2不溶于水,不溶于稀盐酸,不与稀盐酸反应;
②CaCl2.6H2O的溶解度随温度的升高而增大。
回答问题:
(1)配制31%的盐酸730g, 需要36.5%的浓盐酸
(2)酸溶时碳酸钙参与反应的化学方程式为
(3)滤渣I的成分为
(4)操作I采用的方法是:蒸发浓缩、
(5)加入试剂a中和稍过量的石灰水,该反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】某一无色透明的溶液,可能含有Na2SO4、NaOH、Na2CO3、Ca(OH)2中的一种或几种,向其中加入氯化钡溶液,产生白色沉淀,再加稀硝酸,沉淀全部消失。则溶液中一定存在__________ ,一定不存在___________ 、______________ ,可能存在___________ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH﹣=H2O.像这种实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)①写出Na2SO4与BaCl2反应的化学方程式:___________ ; ②把易溶于水的物质写成离子形式,把难溶的物质、气体和水等仍用化学式表示。上述方程式可改写成:2Na﹢+SO42-+Ba²++2Cl-=BaSO4↓+2Na﹢+2Cl- ③删去方程式两边不参加反应的离子:Ba2++SO4²-═BaSO4↓。 ④检查方程式两边各元素的原子个数和电荷总数是否相等。

请回答:
(1)下列各组中的离子,能在溶液中大量共存的是________
A、Na+、Mg2+、Cl﹣、SO4 ²﹣ B、Na+、H+、Cl﹣、OH﹣
C、Na+、Cu²+、Cl﹣、SO42﹣ D、Na+、NH4+、Cl﹣、OH﹣
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式_________ .
(3)写出一个与离子方程式Mg+2H+=Mg2++H2↑相对应的化学方程式________ .

请回答:
(1)下列各组中的离子,能在溶液中大量共存的是
A、Na+、Mg2+、Cl﹣、SO4 ²﹣ B、Na+、H+、Cl﹣、OH﹣
C、Na+、Cu²+、Cl﹣、SO42﹣ D、Na+、NH4+、Cl﹣、OH﹣
(2)写出稀盐酸滴在石灰石上所发生反应的离子方程式
(3)写出一个与离子方程式Mg+2H+=Mg2++H2↑相对应的化学方程式
您最近一年使用:0次



