某化学兴趣小组用推断题的模式设计了一个特殊的校徽。
已知A、B、C、D、E、F、G是初中化学常见的物质,其中D的浓溶液在实验室中常用作干燥剂,B、C、D、E、F分别属于不同类别的物质。它们之间相互关系如图所示,图中“—”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以通过一步反应转化成另一种物质,“ ”表示两种物质之间可以实现双向转化。(部分反应物、生成物及反应条件已略去)。请回答下列问题:
”表示两种物质之间可以实现双向转化。(部分反应物、生成物及反应条件已略去)。请回答下列问题:

(1)D的化学式_________ ;
(2)G→A反应的化学方程式__________________ 。
已知A、B、C、D、E、F、G是初中化学常见的物质,其中D的浓溶液在实验室中常用作干燥剂,B、C、D、E、F分别属于不同类别的物质。它们之间相互关系如图所示,图中“—”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以通过一步反应转化成另一种物质,“
 ”表示两种物质之间可以实现双向转化。(部分反应物、生成物及反应条件已略去)。请回答下列问题:
”表示两种物质之间可以实现双向转化。(部分反应物、生成物及反应条件已略去)。请回答下列问题:
(1)D的化学式
(2)G→A反应的化学方程式
更新时间:2023-06-15 20:26:42
|
相似题推荐
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】甲、乙、丙、丁、戊均为初中化学常见物质,其中甲、乙、丙、丁均含有同一种元素,丙是一种温室气体。它们之间部分转化关系如图所示。(提示:碳与水蒸气在高温下反应生成一氧化碳和氢气;“→”表示某一种物质经一步反应可转化为另一种物质;“—”表示两种物质可以发生化学反应)。试回答下列问题:

(1)丙物质的化学式为_____ 。
(2)丁的化学性质之一是_____ (用化学方程式表示)。
(3)“丙→丁”的化学方程式为_____ 。
(4)若甲为单质,下列说法正确的是_____ (填字母序号)。
a.戊→丁的反应可能是吸热反应
b.戊→丁的反应可能是放热反应
c.乙与戊的反应中有元素的化合价发生了变化
d.丙是目前计入空气质量评价的主要污染物之一
e.丁→丙的反应一定是化合反应

(1)丙物质的化学式为
(2)丁的化学性质之一是
(3)“丙→丁”的化学方程式为
(4)若甲为单质,下列说法正确的是
a.戊→丁的反应可能是吸热反应
b.戊→丁的反应可能是放热反应
c.乙与戊的反应中有元素的化合价发生了变化
d.丙是目前计入空气质量评价的主要污染物之一
e.丁→丙的反应一定是化合反应
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E是初中化学常见的物质,它们的转化关系如图所示(“→”表示物质间转化关系,部分反应物、生成物及反应条件已略去)。其中A、B、E均为氧化物,B的固体俗称干冰且B、E组成元素相同;C、D为酸、碱、盐中不同类别的化合物,D在工业上广泛用于玻璃、造纸、纺织和洗涤剂的生产等。

(1)B的化学式为是________ ;
(2)D→A反应中可以观察到的现象是________ 。
(3)写出B→A反应的化学方程式________ 。

(1)B的化学式为是
(2)D→A反应中可以观察到的现象是
(3)写出B→A反应的化学方程式
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐3】有限的元素可组成种类繁多的物质,请依据H、C、O、Cu等元素回答下列问题。
(1)上述元素中处于第一周期的元素是________ 。
(2)酒精灯的燃料是_________ (写化学式)。
(3)三千多年前我国古代工匠就掌握了较成熟的“火法炼铜”技术。“火法炼铜”是用炭与氧化铜发生反应,从而将铜还原出来。请写出该反应的化学方程式_________ 。
(4)甲、乙、丙是由上述部分元素组成的初中化学常见物质,已知乙的固体叫“干冰”。它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“→”表示某一物质经一步反应可转化为另一种物质)。

①若丙是一种有毒气体,则甲的化学式为________ 。
②若丙是一种无色液体,下列说法正确的是________ (填字母序号)。
A.反应甲→乙、甲→丙不可能是化合反应 B.反应甲→乙、甲→丙不可能是分解反应
C.甲、乙、丙可分别为状态不同的氧化物 D.甲中一定含有氧元素
(1)上述元素中处于第一周期的元素是
(2)酒精灯的燃料是
(3)三千多年前我国古代工匠就掌握了较成熟的“火法炼铜”技术。“火法炼铜”是用炭与氧化铜发生反应,从而将铜还原出来。请写出该反应的化学方程式
(4)甲、乙、丙是由上述部分元素组成的初中化学常见物质,已知乙的固体叫“干冰”。它们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“→”表示某一物质经一步反应可转化为另一种物质)。

①若丙是一种有毒气体,则甲的化学式为
②若丙是一种无色液体,下列说法正确的是
A.反应甲→乙、甲→丙不可能是化合反应 B.反应甲→乙、甲→丙不可能是分解反应
C.甲、乙、丙可分别为状态不同的氧化物 D.甲中一定含有氧元素
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】金属及其制品是现代生活中常见的材料,请回答下列问题
(1)铁和铝都可以制作炊具,主要利用了它们的_____ (填“导电”或“导热”)性.
(2)依据金属活动性顺序,可知人类对铝的利用要比铜和铁_____ (填“早”或“晚”)得多.
(3)铁锈的主要成分是氧化铁,写出氧化铁和稀盐酸反应的化学方程式_____ .
(4)将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到滤渣和无色滤液,则滤渣中一定含有_____ (填化学式),滤液中一定含有的溶质是 _____ (填化学式).
(5)等质量的A和B两金属,其相对原子质量A1(A)<B1(B),将A放入质量分数为16%的稀硫酸中,B放入质量分数为16%的稀盐酸中,在反应生成物中A、B两种元素均显正二价,产生氢气的质量随反应时间变化曲线如图所示,下列说法正确的是_____ (填字母).
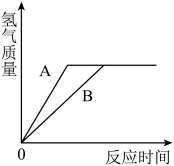
A 产生氢气的速率B>A
B 消耗的稀硫酸和稀盐酸质量一定不相等
C 反应后A和B一定都有剩余
D 消耗B的质量一定小于A的质量
(1)铁和铝都可以制作炊具,主要利用了它们的
(2)依据金属活动性顺序,可知人类对铝的利用要比铜和铁
(3)铁锈的主要成分是氧化铁,写出氧化铁和稀盐酸反应的化学方程式
(4)将适量的铜粉和镁粉的混合物放入一定量的硝酸银溶液中,充分反应后过滤,得到滤渣和无色滤液,则滤渣中一定含有
(5)等质量的A和B两金属,其相对原子质量A1(A)<B1(B),将A放入质量分数为16%的稀硫酸中,B放入质量分数为16%的稀盐酸中,在反应生成物中A、B两种元素均显正二价,产生氢气的质量随反应时间变化曲线如图所示,下列说法正确的是

A 产生氢气的速率B>A
B 消耗的稀硫酸和稀盐酸质量一定不相等
C 反应后A和B一定都有剩余
D 消耗B的质量一定小于A的质量
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐2】已知A与B、甲与乙均为为初中化学常见的物质,其转化关系如图所示。

(1)若甲为氧气,则A的化学式为_____ 。
(2)若甲是种红色固体,乙的溶液呈黄色,A为盐酸,则甲的化学式为_____ 。
(3)若B为硫酸钠,乙为氧化物,且在A溶液中加入锌粉能产生氢气,则A为_____ 。
(4)若甲、乙是常见的碱,A、B是常见的盐。写出甲转化为乙的化学方程式_____ 。

(1)若甲为氧气,则A的化学式为
(2)若甲是种红色固体,乙的溶液呈黄色,A为盐酸,则甲的化学式为
(3)若B为硫酸钠,乙为氧化物,且在A溶液中加入锌粉能产生氢气,则A为
(4)若甲、乙是常见的碱,A、B是常见的盐。写出甲转化为乙的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
真题
解题方法
【推荐3】二氧化氯(ClO2)是一种常用的消毒剂,工业以粗盐水(含少量Ca2+、Mg2+、 等杂质离子)为原料生产ClO2,工艺流程如图8所示。
等杂质离子)为原料生产ClO2,工艺流程如图8所示。________ 。
(2)“精制”中,用下列药品除去杂质离子,请写出一组合理的添加顺序____ (填序号)。
①Na2CO3②BaCl2③NaOH
(3)“精制”最后应加入适量盐酸,其目的是除去溶液中的______ (填离子符号)。
(4)电解池中发生的主要化学反应方程式为_________________ 。
(5)生产过程中能循环利用的物质X是________ (填化学式)。
 等杂质离子)为原料生产ClO2,工艺流程如图8所示。
等杂质离子)为原料生产ClO2,工艺流程如图8所示。
(2)“精制”中,用下列药品除去杂质离子,请写出一组合理的添加顺序
①Na2CO3②BaCl2③NaOH
(3)“精制”最后应加入适量盐酸,其目的是除去溶液中的
(4)电解池中发生的主要化学反应方程式为
(5)生产过程中能循环利用的物质X是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】氯化钙是多用途的干燥剂和建筑防冻剂。实验室里用石灰石和盐酸制备二氧化碳的含酸废液(含有MgCl2、FeCl3等)通过以下途径制得无水氯化钙。

(1)操作I的名称为_____ ,操作II的名称为______ 。滤渣的化学成分有____________________ 。
(2)石灰乳的作用是①_____________________ ,②_________________________ ,写出其中1个反应的化学方程式____________________________________ 。

(1)操作I的名称为
(2)石灰乳的作用是①
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】钛白粉是一种建筑涂料。工业上可利用生产钛白粉时生成的副产品FeSO4和含H2SO4的废液生产Fe2O3,其主要生产流程如图所示,分析流程,回答问题。
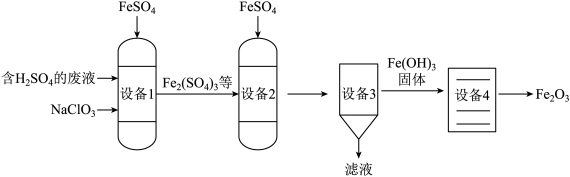
(1)设备1中铁元素的化合价___________ (选“升高”、“降低”或“不变”)。
(2)设备2中,Fe2(SO4)3与NaOH发生复分解反应的化学方式为___________ 。
(3)设备3中得到Fe(OH)3固体的操作包括___________ 、洗涤、干燥等,若要检验Fe(OH)3已洗涤干净,可向最后一次洗涤液中加入___________ 。
(4)设备4中Fe(OH)3在加热下反应生成Fe2O3和另一种氧化物,另一种氧化物为___________ 。

(1)设备1中铁元素的化合价
(2)设备2中,Fe2(SO4)3与NaOH发生复分解反应的化学方式为
(3)设备3中得到Fe(OH)3固体的操作包括
(4)设备4中Fe(OH)3在加热下反应生成Fe2O3和另一种氧化物,另一种氧化物为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】碳酸锂(Li2CO3)是制备手机锂电池的重要原料。正衡某化学兴趣小组欲了解工业制锂的主要流程,并设计实验测定碳酸锂粗产品的纯度。
I制备碳酸锂粗产品
工业上以锂辉石精矿(主要成分为Li2O,其余成分不溶于水,也不参与反应)为原料制取Li2CO3,其主要工艺流程如图所示:

提示:①Li2CO3微溶于水,其溶解度随温度的升高而减小。
②反应器中发生的反应的化学方程式: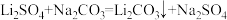
(1)在投入酸浸槽前,锂辉石需进行粉碎研磨的预处理,其目的是_______ 。
(2)写出酸浸槽中发生的反应的化学方程式_______ 。
(3)沉锂池中分离出的滤液中含有的溶质有_______ (填化学式)。
(4)沉锂池中分离出的滤渣主要成分是碳酸锂,洗涤时使用热水的原因是_______ 。
Ⅱ测定碳酸锂粗产品的纯度
为测定碳酸锂粗产品纯度(杂质不溶于水,也不参与反应),小组同学设计了如下实验装置。

查阅资料:碳酸锂与碳酸钙类似,能与稀硫酸发生复分解反应。碱石灰能吸收水和二氧化碳。
操作步骤:
①连接好装置,检查装置的气密性。
②在D中加入10g碳酸锂粗产品。打开弹簧夹C,在A处缓缓通入一段时间的空气。
③称量F的质量。
④关闭弹簧夹C,慢慢滴加稀硫酸至过量,直至D中无气泡冒出。
⑤再次称量F的质量。
试回答下列问题:
(5)B装置的作用是_______ (用方程式表示)
(6)下列各项措施中。能提高测定准确度的是 (填字母)。
(7)上述操作步骤②中通空气的目的是_______ 。
(8)若F装置在反应后增重5.28g,则根据该数据计算可知碳酸锂粗产品的纯度为_______ 。
I制备碳酸锂粗产品
工业上以锂辉石精矿(主要成分为Li2O,其余成分不溶于水,也不参与反应)为原料制取Li2CO3,其主要工艺流程如图所示:

提示:①Li2CO3微溶于水,其溶解度随温度的升高而减小。
②反应器中发生的反应的化学方程式:
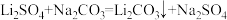
(1)在投入酸浸槽前,锂辉石需进行粉碎研磨的预处理,其目的是
(2)写出酸浸槽中发生的反应的化学方程式
(3)沉锂池中分离出的滤液中含有的溶质有
(4)沉锂池中分离出的滤渣主要成分是碳酸锂,洗涤时使用热水的原因是
Ⅱ测定碳酸锂粗产品的纯度
为测定碳酸锂粗产品纯度(杂质不溶于水,也不参与反应),小组同学设计了如下实验装置。

查阅资料:碳酸锂与碳酸钙类似,能与稀硫酸发生复分解反应。碱石灰能吸收水和二氧化碳。
操作步骤:
①连接好装置,检查装置的气密性。
②在D中加入10g碳酸锂粗产品。打开弹簧夹C,在A处缓缓通入一段时间的空气。
③称量F的质量。
④关闭弹簧夹C,慢慢滴加稀硫酸至过量,直至D中无气泡冒出。
⑤再次称量F的质量。
试回答下列问题:
(5)B装置的作用是
(6)下列各项措施中。能提高测定准确度的是 (填字母)。
| A.缓慢滴加稀硫酸 | B.在B、D之间增加装有浓硫酸的洗气瓶 |
| C.将E、F装置调换顺序 | D.去除G装置 |
| E.在步骤⑤之前,再次打开弹簧夹C,在A处缓缓通入一段时间的空气 | |
(8)若F装置在反应后增重5.28g,则根据该数据计算可知碳酸锂粗产品的纯度为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
【推荐1】某无色溶液由澄清石灰水、盐酸、氢氧化钠溶液、氯化钠溶液、碳酸钠溶液中的两种溶液组成。
(1)若取适量样品溶液放入试管中,滴加酚酞溶液,溶液呈无色。则溶液的组成是________ (填名称)。
(2)若取适量样品溶液放入试管中,滴加酚酞溶液,溶液呈红色,再向试管中加入过量的氢氧化钙溶液,观察到有沉淀产生,该反应的化学方程式为__________ ;由此可知该样品中 一定含有的物质是_________ (填化学式)。过滤,滤液仍为红色,滤液中除酚酞以外,还一定含有的溶质为_________ (填化学式)。
(3)在(2)的基础上,为确定样品溶液的组成,取适量样品溶液放入试管中,滴加过量的氯化钙溶液(氯化钙溶液呈中性),再滴加酚酞溶液,若溶液呈无色,证明样品中还含有__________ (填化学式)。
(1)若取适量样品溶液放入试管中,滴加酚酞溶液,溶液呈无色。则溶液的组成是
(2)若取适量样品溶液放入试管中,滴加酚酞溶液,溶液呈红色,再向试管中加入过量的氢氧化钙溶液,观察到有沉淀产生,该反应的化学方程式为
(3)在(2)的基础上,为确定样品溶液的组成,取适量样品溶液放入试管中,滴加过量的氯化钙溶液(氯化钙溶液呈中性),再滴加酚酞溶液,若溶液呈无色,证明样品中还含有
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐2】硫酸铜在纺织、印刷等行业有广泛用途。工业上以辉铜矿(主要含Cu2S,还含少量的Fe2O3、SiO2及一些不溶性杂质)为原料制备CuSO4•5H2O晶体。主要流程如下:

已知:①SiO2不溶于水,也不溶于酸。
②CuSO4•5H2O易溶于水,难溶于乙醇。
③CuSO4的溶解度曲线如图所示。

(1)高温焙烧中生成一种黑色固体,该反应的化学方程式为__ 。为防止污染,可用石灰乳吸收尾气SO2,该步骤用石灰乳而不用澄清石灰水的原因是__ 。吸收过程中为了防止液体倒吸,可以选用如图 装置中的__ 。

(2)实验室用溶质质量分数为 98%、密度是 1.84g•mL-1的浓硫酸配制 20%的稀硫酸 196 g,需要浓硫酸的体积为__ mL(结果保留一位小数)。量取该体积的浓硫酸所选用的仪器为_ 填字母)。
a 50 mL量筒
b 50 mL烧杯
c 100 mL量筒
d 胶头滴管
(3)滤渣 2 为红褐色,化学式为__ 。调节 pH 时,最好选用的试剂是__ (填字母)。
a Cu
b CuO
c NaOH 溶液
d NH3•H2O
(4)流程中“一系列操作”主要过程为:①蒸发浓缩,__ ,过滤,__ ,最后低温烘干,得到CuSO4•5H2O。低温烘干的原因是__ 。
(5)欲测定该产品中CuSO4•5H2O的质量分数,某兴趣小组进行如下实验:
①称取 21.00 g 样品配成 100 mL 溶液,量取 25.00 mL,加足量标准BaCl2溶液,过滤、洗涤、烘干,得到沉淀 4.66 g,则该产品中CuSO4•5H2O的质量分数为__ 。(结果精确到 0.1%,写出计算过程)
②有同学用该方法测定发现样品中CuSO4•5H2O的质量分数大于 100%(测定过程中产生的误差可忽略),其原因可能是__ (任写一种)。

已知:①SiO2不溶于水,也不溶于酸。
②CuSO4•5H2O易溶于水,难溶于乙醇。
③CuSO4的溶解度曲线如图所示。

(1)高温焙烧中生成一种黑色固体,该反应的化学方程式为

(2)实验室用溶质质量分数为 98%、密度是 1.84g•mL-1的浓硫酸配制 20%的稀硫酸 196 g,需要浓硫酸的体积为
a 50 mL量筒
b 50 mL烧杯
c 100 mL量筒
d 胶头滴管
(3)滤渣 2 为红褐色,化学式为
a Cu
b CuO
c NaOH 溶液
d NH3•H2O
(4)流程中“一系列操作”主要过程为:①蒸发浓缩,
(5)欲测定该产品中CuSO4•5H2O的质量分数,某兴趣小组进行如下实验:
①称取 21.00 g 样品配成 100 mL 溶液,量取 25.00 mL,加足量标准BaCl2溶液,过滤、洗涤、烘干,得到沉淀 4.66 g,则该产品中CuSO4•5H2O的质量分数为
②有同学用该方法测定发现样品中CuSO4•5H2O的质量分数大于 100%(测定过程中产生的误差可忽略),其原因可能是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐3】过氧化钙(CaO2)难溶于水,常温下稳定,在潮湿空气及水中缓慢放出氧气,广泛应用于渔业等领域。下图是以大理石(含Al2O3及其他不溶于水也不溶于酸的杂质)等为原料制取CaO2的流程图:

(1)操作a、b、c的名称都是_____________ 。
(2)操作a的目的是______________________ 。
(3)从滤液C中可回收的副产品的化学式为____________ 。
(4)写出反应①的化学方程式_________________________ 。
(5)反应②的基本反应类型是________________________ 。
(6)在该生产过程中,用110kg大理石制得了72Kg的过氧化钙。如果不考虑过程中的损耗,可计算出大理石中CaCO3的质量分数为_____________ 。(结果保留一位小数)

(1)操作a、b、c的名称都是
(2)操作a的目的是
(3)从滤液C中可回收的副产品的化学式为
(4)写出反应①的化学方程式
(5)反应②的基本反应类型是
(6)在该生产过程中,用110kg大理石制得了72Kg的过氧化钙。如果不考虑过程中的损耗,可计算出大理石中CaCO3的质量分数为
您最近一年使用:0次



