“波尔多液”是农业上应用历史最长的一 种杀菌剂。化工厂常利用废弃铜料(只含有铜和一定量的铁)和石灰石制备“波尔多液”,流程如下图所示,请回答下列问题。______________ 。
(2)反应器2中发生反应的化学方程式是__________________ 。
(3)反应器3和反应器4的内壁均不能为铁制品,原因是____________ (请用文字来表述)。
(4)废液A中溶质有___________________ 。
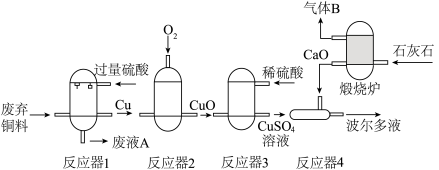
(2)反应器2中发生反应的化学方程式是
(3)反应器3和反应器4的内壁均不能为铁制品,原因是
(4)废液A中溶质有
更新时间:2023-06-27 09:25:09
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】金属在生产和生活中的应用极为广泛。
(1)地铁站供电系统多用铜作导线,是因为铜具有良好的延展性和________ 性(填“导电”或“导热”)。
(2)地铁站使用的铜,我国早在西汉时期利用湿法冶金技术就可以进行炼制。其原理是利用铁和硫酸铜溶液发生反应制取铜,其反应的化学方程式为________ 。
(3)修地铁所用金属材料中的铁是用一氧化碳和赤铁矿(主要成分氧化铁)反应炼制的,其反应的化学方程式为_______ ,如果用2000t含氧化铁80%的赤铁矿,理论上能炼出含铁96%的生铁的质量为_____ t(计算结果保留一位小数)。
(4)将一定质量的锌粉加入到硝酸银和硝酸铜的混合溶液,溶液质量变化情况如图所示。下列说法不正确的是 (填序号)。

(1)地铁站供电系统多用铜作导线,是因为铜具有良好的延展性和
(2)地铁站使用的铜,我国早在西汉时期利用湿法冶金技术就可以进行炼制。其原理是利用铁和硫酸铜溶液发生反应制取铜,其反应的化学方程式为
(3)修地铁所用金属材料中的铁是用一氧化碳和赤铁矿(主要成分氧化铁)反应炼制的,其反应的化学方程式为
(4)将一定质量的锌粉加入到硝酸银和硝酸铜的混合溶液,溶液质量变化情况如图所示。下列说法不正确的是 (填序号)。

| A.反应后溶液一定是无色的 |
| B.反应后过滤,滤渣一定含有银和铜 |
| C.反应后,生成银与铜的质量比为1:1 |
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐2】金属是重要的资源,请根据所学知识解决以下问题。
1.将一定量的铁粉加入到硝酸锌、硝酸银混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸无现象,则滤液中一定含有的溶质的化学式为___________ ,加入铁粉后发生反应的化学方程式是____________________ 。
2.某钢炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如图所示。

A、写出②③三步反应的化学方程式
②_________________________ ;③____________________ ;
B、在炼铁过程中石灰石的作用是_________________________ 。
3.全世界每年因生锈损失的钢铁,约占世界年产量的十分之一。某学生想弄清楚铁生锈是否必须同时有空气和水,他将干净的铁钉放入A、B、C三支试管中,进行研究。
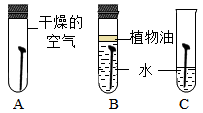
①一周后,编号为__________ 的试管中铁钉最易生锈;
②铁生锈的条件是_________________ ;
③如何防止家庭中常见的铁制品生锈,简单易行的方法有(列举二种方法)_________________ 、______________ 。
1.将一定量的铁粉加入到硝酸锌、硝酸银混合溶液中,充分反应后过滤,向滤渣中加入稀盐酸无现象,则滤液中一定含有的溶质的化学式为
2.某钢炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如图所示。

A、写出②③三步反应的化学方程式
②
B、在炼铁过程中石灰石的作用是
3.全世界每年因生锈损失的钢铁,约占世界年产量的十分之一。某学生想弄清楚铁生锈是否必须同时有空气和水,他将干净的铁钉放入A、B、C三支试管中,进行研究。

①一周后,编号为
②铁生锈的条件是
③如何防止家庭中常见的铁制品生锈,简单易行的方法有(列举二种方法)
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】铁及铁的合金是应用最广泛的金属材料。
(1)生活中常使用铁锅炒菜,这是利用了金属的_______ 性。铁生锈的条件是_____
(2)向含有硫酸亚铁和硫酸铜的废液中加入某种金属,可回收硫酸亚铁和铜。该反应的化学方程式是_____ 。
(3)以硫铁矿【主要成分是二硫化亚铁(FeS2)】为原料可生产硫酸,炉渣回收可炼铁。其主要流程如下(反应条件已略去):

①上述流程出现的物质中,硫元素显+6价的物质的化学式是_________
②炉渣炼铁的化学方程式是________ 。
③将硫铁矿和空气反应的化学方程式补充完整:4FeS2+________  2Fe2O3+8SO2
2Fe2O3+8SO2
(1)生活中常使用铁锅炒菜,这是利用了金属的
(2)向含有硫酸亚铁和硫酸铜的废液中加入某种金属,可回收硫酸亚铁和铜。该反应的化学方程式是
(3)以硫铁矿【主要成分是二硫化亚铁(FeS2)】为原料可生产硫酸,炉渣回收可炼铁。其主要流程如下(反应条件已略去):

①上述流程出现的物质中,硫元素显+6价的物质的化学式是
②炉渣炼铁的化学方程式是
③将硫铁矿和空气反应的化学方程式补充完整:4FeS2+
 2Fe2O3+8SO2
2Fe2O3+8SO2
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】完成下列变化的化学方程式,并注明反应类型。
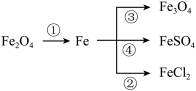
①_____
②_____ ( )
③_____ ( )
④_____ ( )

①
②
③
④
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】常见的金属有镁、铝、铜、银等。请根据金属的化学性质回答下列问题:
(1)将一定质量的镁粉放入到含有溶质为硝酸铝、硝酸铜、硝酸银的溶液中,充分反应后过滤,得到滤渣和滤液。
①若滤液呈蓝色,则滤渣中可能含有的金属是_____ 。
②若向滤渣中加入稀盐酸无气泡产生,则滤液中一定含有的溶质是_____ 。(填化学式)
(2)某金属粉末中含有镁、铝、铜、银中的一种或几种,取12g该金属粉末与足量稀盐酸反应产生1g氢气,则该金属粉末的组成有_____ 种情况。
(1)将一定质量的镁粉放入到含有溶质为硝酸铝、硝酸铜、硝酸银的溶液中,充分反应后过滤,得到滤渣和滤液。
①若滤液呈蓝色,则滤渣中可能含有的金属是
②若向滤渣中加入稀盐酸无气泡产生,则滤液中一定含有的溶质是
(2)某金属粉末中含有镁、铝、铜、银中的一种或几种,取12g该金属粉末与足量稀盐酸反应产生1g氢气,则该金属粉末的组成有
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下列短文,回答相关问题。
奥美拉唑
胃酸是胃液中非常重要的消化液,它能够促进营养物质的消化和吸收,但胃酸并不是越多越好。当胃酸分泌过多时,会直接损害胃粘膜,严重的会导致胃溃疡,也会使定居于胃粘膜的幽门螺旋杆菌大量繁殖,引起各类胃肠道疾病。奥美拉唑是治疗胃酸过多引起的各种消化系统疾病的常用药物。
1988年,奥美拉唑由瑞典Astra公司研发上市,是目前胃酸抑制剂中疗效最强的药物之一。奥美拉唑能使细胞壁内的 无法转运到人体的胃液当中,从而有效抑制胃酸的分泌。但是奥美拉唑在酸性或者光照条件下极不稳定,在胃液中会迅速分解。将奥美拉唑制成肠溶片、肠溶胶囊或奥美拉唑和碳酸氢钠的包芯片,都能很好的解决该问题。
无法转运到人体的胃液当中,从而有效抑制胃酸的分泌。但是奥美拉唑在酸性或者光照条件下极不稳定,在胃液中会迅速分解。将奥美拉唑制成肠溶片、肠溶胶囊或奥美拉唑和碳酸氢钠的包芯片,都能很好的解决该问题。
肠溶片:将奥美拉唑做制成肠溶片,肠溶膜衣在酸中不溶解,在肠液中溶解,这种工艺保护了奥美拉唑,但是包肠溶膜衣技术要求高,物料和人工成本增加。
肠溶胶囊:将奥美拉唑和碳酸氢钠直接混合灌装于胶囊,服用后,碳酸氢钠快速释放,在胃液中反应,同时给奥美拉唑提供稳定的碱性环境。但由于其工艺仅仅将奥美拉唑与碳酸氢钠及辅料简单混合,无法确保药物释放的先后顺序。
奥美拉唑包芯片:如图1所示结构,设计奥美拉唑和碳酸氢钠包芯片,其中碳酸氢钠为包芯片的外层,可迅速的崩解,避免奥美拉唑直接接触胃液,碳酸氢钠外层崩解后,奥美拉唑也能够迅速在胃内释放,有效提高了奥美拉唑的生物利用度。图2为包芯片和市面上的奥美拉唑普通片在胃酸中不同时间点pH值的变化趋势。
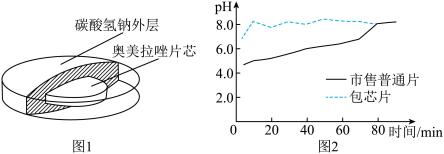
通过制剂工艺的改进,生产的复方奥美拉唑包芯片质量及效果优于原药,且制药成本及稳定性都有很大优势。因此,在药品研发的过程中,不宜盲目迷信其生产及制作工艺,需要增强自信,大胆创新,自主研发新药剂。
回答下列问题:
(1)奥美拉唑的化学式为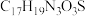 ,其中氮元素和硫元素的质量比为
,其中氮元素和硫元素的质量比为______ 。
(2)碳酸氢钠俗称______ ,碳酸氢钠在胃液中发生反应的化学方程式为______ 。
(3)结合图1和图2,简述奥美拉唑包芯片质量及效果更优的原因________ 。
(4)下列关于奥美拉唑相关药品描述正确的是______ (填序号)。
a.幽门螺旋杆菌在胃酸过多的情况下会大量繁殖,影响人体健康
b.奥美拉唑胶囊和奥美拉唑包芯片一样,都加入了碳酸氢钠,效果一致
c.奥美拉唑药物中加入碳酸氢钠除了能够提供碱性环境外,还能中和胃酸
d.在药品研发过程中,不仅要考虑药效,还要综合考虑药物研发的工艺和成本
奥美拉唑
胃酸是胃液中非常重要的消化液,它能够促进营养物质的消化和吸收,但胃酸并不是越多越好。当胃酸分泌过多时,会直接损害胃粘膜,严重的会导致胃溃疡,也会使定居于胃粘膜的幽门螺旋杆菌大量繁殖,引起各类胃肠道疾病。奥美拉唑是治疗胃酸过多引起的各种消化系统疾病的常用药物。
1988年,奥美拉唑由瑞典Astra公司研发上市,是目前胃酸抑制剂中疗效最强的药物之一。奥美拉唑能使细胞壁内的
 无法转运到人体的胃液当中,从而有效抑制胃酸的分泌。但是奥美拉唑在酸性或者光照条件下极不稳定,在胃液中会迅速分解。将奥美拉唑制成肠溶片、肠溶胶囊或奥美拉唑和碳酸氢钠的包芯片,都能很好的解决该问题。
无法转运到人体的胃液当中,从而有效抑制胃酸的分泌。但是奥美拉唑在酸性或者光照条件下极不稳定,在胃液中会迅速分解。将奥美拉唑制成肠溶片、肠溶胶囊或奥美拉唑和碳酸氢钠的包芯片,都能很好的解决该问题。肠溶片:将奥美拉唑做制成肠溶片,肠溶膜衣在酸中不溶解,在肠液中溶解,这种工艺保护了奥美拉唑,但是包肠溶膜衣技术要求高,物料和人工成本增加。
肠溶胶囊:将奥美拉唑和碳酸氢钠直接混合灌装于胶囊,服用后,碳酸氢钠快速释放,在胃液中反应,同时给奥美拉唑提供稳定的碱性环境。但由于其工艺仅仅将奥美拉唑与碳酸氢钠及辅料简单混合,无法确保药物释放的先后顺序。
奥美拉唑包芯片:如图1所示结构,设计奥美拉唑和碳酸氢钠包芯片,其中碳酸氢钠为包芯片的外层,可迅速的崩解,避免奥美拉唑直接接触胃液,碳酸氢钠外层崩解后,奥美拉唑也能够迅速在胃内释放,有效提高了奥美拉唑的生物利用度。图2为包芯片和市面上的奥美拉唑普通片在胃酸中不同时间点pH值的变化趋势。

通过制剂工艺的改进,生产的复方奥美拉唑包芯片质量及效果优于原药,且制药成本及稳定性都有很大优势。因此,在药品研发的过程中,不宜盲目迷信其生产及制作工艺,需要增强自信,大胆创新,自主研发新药剂。
回答下列问题:
(1)奥美拉唑的化学式为
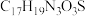 ,其中氮元素和硫元素的质量比为
,其中氮元素和硫元素的质量比为(2)碳酸氢钠俗称
(3)结合图1和图2,简述奥美拉唑包芯片质量及效果更优的原因
(4)下列关于奥美拉唑相关药品描述正确的是
a.幽门螺旋杆菌在胃酸过多的情况下会大量繁殖,影响人体健康
b.奥美拉唑胶囊和奥美拉唑包芯片一样,都加入了碳酸氢钠,效果一致
c.奥美拉唑药物中加入碳酸氢钠除了能够提供碱性环境外,还能中和胃酸
d.在药品研发过程中,不仅要考虑药效,还要综合考虑药物研发的工艺和成本
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】金属材料与人类的生产和生活密切相关。
(1)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是铁合金,铁合金的硬度比纯铁_______ (填“大”或“小”)。
(2)生铁和钢是两种常见的铁合金,下列说法错误的是 (填字母)。
(3)自行车车架表面喷漆不仅美观,而且可有效防止铁与空气中的___________ 接触而生锈。
(4)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序,某同学设计了如图所示的3个实验:

实验甲中铝丝会出现明显的现象,则实验甲中反应的化学方程式为________ 。另一位同学认为实验乙、丙中均无明显现象,对完整的实验结论没有作用,都可以省去。你的看法是_______ 。
(5)某化学兴趣小组将一定质量的Fe和Zn的混合粉末加入AgNO3溶液中,充分反应后过滤,得到滤渣和滤液:
①如果滤液中加入稀盐酸有白色沉淀,则滤液中的金属阳离子有_________ 种;
②如果滤液呈浅绿色,则关于该滤渣和滤液的下列说法中正确的是_________ (填字母)。
A.向滤渣中加入稀盐酸,一定有气泡产生
B.向滤液中加入稀盐酸,一定有白色沉淀产生
C.滤渣中一定含有Ag
D.滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Zn(NO3)2
(1)近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是铁合金,铁合金的硬度比纯铁
(2)生铁和钢是两种常见的铁合金,下列说法错误的是 (填字母)。
| A.生铁就是含杂质很多的铁的合金 |
| B.放入足量的稀盐酸中,一定有黑色的固体剩余 |
| C.它们放在稀盐酸中都会有气泡产生 |
| D.它们都是混合物 |
(3)自行车车架表面喷漆不仅美观,而且可有效防止铁与空气中的
(4)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序,某同学设计了如图所示的3个实验:

实验甲中铝丝会出现明显的现象,则实验甲中反应的化学方程式为
(5)某化学兴趣小组将一定质量的Fe和Zn的混合粉末加入AgNO3溶液中,充分反应后过滤,得到滤渣和滤液:
①如果滤液中加入稀盐酸有白色沉淀,则滤液中的金属阳离子有
②如果滤液呈浅绿色,则关于该滤渣和滤液的下列说法中正确的是
A.向滤渣中加入稀盐酸,一定有气泡产生
B.向滤液中加入稀盐酸,一定有白色沉淀产生
C.滤渣中一定含有Ag
D.滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Zn(NO3)2
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】某热电厂用脱硫得到的石膏(CaSO4•2H2O)生产K2SO4肥料的流程如下:

请回答下列问题:
(1)石膏中S的化合价是___ .脱硫过程的化学方程式2CaCO3+2SO2+O2+4H2O=2CaSO4•2H2O+2 ___ .
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是___ .
(3)实验室完成过滤操作所需要用到玻璃棒,玻璃棒的作用是___ .
(4)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体.此反应的基本类型是___ .
(5)该工艺可以循环利用的物质有___ ,副产品NH4Cl与NaOH溶液混合微热,产生的气体能使湿润的红色石蕊试纸变 ___ 色.

请回答下列问题:
(1)石膏中S的化合价是
(2)石膏与饱和(NH4)2CO3溶液相混合,发生反应Ⅰ时需不断搅拌,其目的是
(3)实验室完成过滤操作所需要用到玻璃棒,玻璃棒的作用是
(4)(NH4)2SO4与KCl溶液需在浓氨水中发生反应Ⅱ,析出K2SO4晶体.此反应的基本类型是
(5)该工艺可以循环利用的物质有
您最近一年使用:0次
【推荐1】阅读下面文章,回答下列问题。
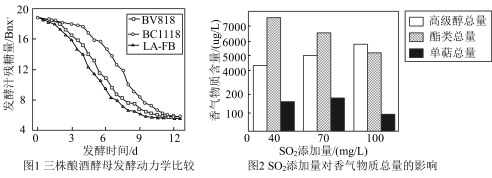
制造葡萄酒的原料葡萄中富含K、Ca、Na、Fe、Zn、Mg等元素。葡萄酒是以鲜葡萄或葡萄汁为原料,经酿酒酵母菌株将葡萄汁中的糖转化为酒精,同时生成了高级醇、酯类、单萜等香气化合物。葡萄酒香气主要受酿造菌种、酿造工艺、发酵条件等因素的影响。研究人员以发酵汁中残糖量为指标,研究不同种类的酿酒酵母的发酵动力(即发酵过程的速率),其测定结果如图1所示。
为防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,葡萄酒酿制中还会适量添加SO2,其添加量对主要香气物质总量影响如图2所示。
葡萄在栽种过程中容易产生病虫害,可通过定期施肥、中和酸性土壤、喷洒农药等方法来增强葡萄抗病能力。若发病,可用硫酸铜配制农药波尔多液进行喷洒。
人们发现二氧化硫可以完成上面所有的需求。在酵母发酵的过程中,会产生一定量的二氧化硫,不过这个量比较少,还需要额外添加。这里添加的并不一定是二氧化硫气体,可以是它的其他化合物——各种亚硫酸盐、焦亚硫酸盐、亚硫酸氢盐等。这些物质能够实现跟二氧化硫有类似的功能。部分国家葡萄酒中二氧化硫含量上限标准如表。
(1ppm=1mg/Kg,1ppm=1mg/L)
国际食品添加剂联合专家委员会(JECFA)制定的二氧化硫安全摄入限是每天每公斤体重0.7mg。“安全摄入限”的意思是,不超过这个含量的二氧化硫,即使长期食用,也不会带来可见的危害。
(1)在上述金属元素中,属于人体中微量元素的有_____ 。
(2)配制农药波尔多液时,不宜用___ 容器(填“铁制”或“铜制”)。
(3)在酿造葡萄酒的过程中,加入一定量SO2的作用是_____ 。
(4)对于一个体重62.5kg的成年人,每天二氧化硫安全摄入量是_____ g。
(5)下列说法正确的是_____ 。
制造葡萄酒的原料葡萄中富含K、Ca、Na、Fe、Zn、Mg等元素。葡萄酒是以鲜葡萄或葡萄汁为原料,经酿酒酵母菌株将葡萄汁中的糖转化为酒精,同时生成了高级醇、酯类、单萜等香气化合物。葡萄酒香气主要受酿造菌种、酿造工艺、发酵条件等因素的影响。研究人员以发酵汁中残糖量为指标,研究不同种类的酿酒酵母的发酵动力(即发酵过程的速率),其测定结果如图1所示。
为防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动,葡萄酒酿制中还会适量添加SO2,其添加量对主要香气物质总量影响如图2所示。

葡萄在栽种过程中容易产生病虫害,可通过定期施肥、中和酸性土壤、喷洒农药等方法来增强葡萄抗病能力。若发病,可用硫酸铜配制农药波尔多液进行喷洒。
人们发现二氧化硫可以完成上面所有的需求。在酵母发酵的过程中,会产生一定量的二氧化硫,不过这个量比较少,还需要额外添加。这里添加的并不一定是二氧化硫气体,可以是它的其他化合物——各种亚硫酸盐、焦亚硫酸盐、亚硫酸氢盐等。这些物质能够实现跟二氧化硫有类似的功能。部分国家葡萄酒中二氧化硫含量上限标准如表。
(1ppm=1mg/Kg,1ppm=1mg/L)
| 国家 | 干红 | 甜酒 |
| 澳洲 | 250ppm | 350ppm |
| 中国 | 250ppm | 400ppm |
| 国际葡萄栽培与酿酒组织 | 300ppm | 450ppm |
(1)在上述金属元素中,属于人体中微量元素的有
(2)配制农药波尔多液时,不宜用
(3)在酿造葡萄酒的过程中,加入一定量SO2的作用是
(4)对于一个体重62.5kg的成年人,每天二氧化硫安全摄入量是
(5)下列说法正确的是
| A.SO2添加量在100mg/L时,高级醇总量最高 |
| B.酯类总量随着SO2添加量的增大而增大 |
| C.单萜总量随着SO2添加量的增加,先增大后减小 |
| D.氯化钠能代替二氧化硫添加到葡萄酒中 |
| E.在其他条件相同时,发酵动力最好的酿酒酵母菌株是LA﹣FR |
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
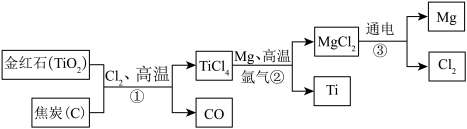
【推荐2】2022年8月1日,国产C919大飞机完成取证试飞,该飞机的制造中9%的用料为钛合金。如图是工业上以金红石(主要成分是TiO2)为原料生产金属(Ti)的流程图;
(1)金红石和焦炭要先粉碎处理,目的是_______ 。
(2)反应②要在氢气环境中进行,氩气能作保护气是利用了它的_______ 性质(“物理”或“化学”)。
(3)反应③的化学方程式为_______ ,该反应的基本反应类型是_______ 反应。
(4)该流程中可以循环利用的物质有_______ 。

(1)金红石和焦炭要先粉碎处理,目的是
(2)反应②要在氢气环境中进行,氩气能作保护气是利用了它的
(3)反应③的化学方程式为
(4)该流程中可以循环利用的物质有
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸铝【Al2(SO4)3】广泛用于造纸、处理工业用水等。铝土矿(主要成分为Al2O3和SiO2),生产硫酸铝的流程如图所示。
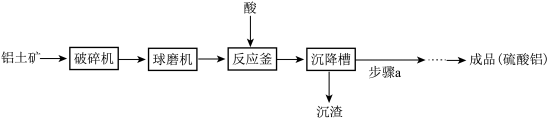
(1)将铝土矿粉碎的原因是___________ 。
(2)Al2(SO4)3属于___________ (填“酸”、“碱”或“盐”)。
(3)反应釜中加入的酸是___________ (填字母),反应釜中反应的化学方程式是___________ 。
A.HCl B.H2SO4 C.HNO3
(4)步骤a是从硫酸铝溶液中制备制备硫酸铝晶体需经过蒸发、___________ 、过滤、洗涤、干燥等。

(1)将铝土矿粉碎的原因是
(2)Al2(SO4)3属于
(3)反应釜中加入的酸是
A.HCl B.H2SO4 C.HNO3
(4)步骤a是从硫酸铝溶液中制备制备硫酸铝晶体需经过蒸发、
您最近一年使用:0次



