长期使用的水壶内会产生一层水垢(主要成分是碳酸钙和氢氧化镁),可用酸溶液清除。小明为测定水垢中碳酸钙的含量,向盛有不同质量水垢粉末的烧杯中均加入 等质量分数的稀盐酸,充分反应后测得的实验数据如下:
等质量分数的稀盐酸,充分反应后测得的实验数据如下:
请计算:
(1)第三组实验中所得二氧化碳的质量为_____ g。
(2)水垢中碳酸钙的质量分数。
 等质量分数的稀盐酸,充分反应后测得的实验数据如下:
等质量分数的稀盐酸,充分反应后测得的实验数据如下:| 实验组数 | 第一组 | 第一组 | 第三组 |
| 水垢的质量/g | 10 | 20 | 30 |
| 烧杯中剩余物质总质量/g | 106.7 | 113.4 | 122.3 |
(1)第三组实验中所得二氧化碳的质量为
(2)水垢中碳酸钙的质量分数。
2023·河北保定·二模 查看更多[4]
2023年河北省保定市高碑店市中考二模化学试题山东省泰安市岱岳区2023-2024学年九年级上学期期末化学试题(已下线)2024年中考风向标-河北-利用化学方程式的计算(已下线)黄金卷08(河北专用)-【赢在中考·黄金8卷】备战2024年中考化学模拟卷(河北专用)
更新时间:2023-06-29 23:02:32
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】取10g碳酸钙固体在高温反应炉内加热,一段时间后停止加热,测得剩余固体中钙元素的质量分数为50%,则生成二氧化碳的质量_____________ g.
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某化学兴趣小组欲测定某石灰石样品中CaCO3的质量分数,取12.5g样品和足量的稀盐酸混合,反应前容器内物质总质量为110.4g,充分反应后,容器内物质总质量为106g。请计算。
(1)生成二氧化碳气体的质量为_________ 。
(2)石灰石样品中CaCO3的质量分数______ 。(写出计算过程)
(1)生成二氧化碳气体的质量为
(2)石灰石样品中CaCO3的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
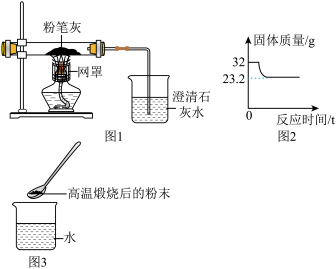
【推荐3】粉笔的主要成分为石灰石(含CaCO3)和石膏(CaSO4)。如图1所示煅烧32g粉笔末使CaCO3完全反应,玻璃管内固体质量随时间关系如图2所示。回答下列问题:
(1)反应时,图1烧杯中的现象是_____ 。
(2)由图2所知,生成CO2的质量为_____ g。
(3)反应结束,将煅烧后的粉末倒入足量水中,如图3,用手触摸烧杯外壁,感觉微热,主要原因是_____ 。
(4)计算该粉笔末中CaCO3的质量分数(根据化学方程式写出计算过程)。
(1)反应时,图1烧杯中的现象是
(2)由图2所知,生成CO2的质量为
(3)反应结束,将煅烧后的粉末倒入足量水中,如图3,用手触摸烧杯外壁,感觉微热,主要原因是
(4)计算该粉笔末中CaCO3的质量分数(根据化学方程式写出计算过程)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组做了如下实验:取25g石灰石样品(杂质不溶于酸也不与酸反应)放入烧杯中,向其中逐渐加入足量稀盐酸,反应时间与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
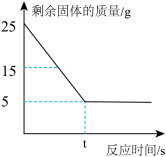
(1)25g石灰石样品中碳酸钙的质量分数为________ 。
(2)该反应共产生多少CO2________ ?(请根据化学方程式写出完整的计算步骤)

(1)25g石灰石样品中碳酸钙的质量分数为
(2)该反应共产生多少CO2
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】过氧化钙(CaO2)是一种环境友好型化工原料,工农业生产中用作漂白剂、种子消毒剂及鱼类运输时的制氧剂等。某同学把20g不纯的过氧化钙样品(杂质不与水反应)加入到盛有50g水(足量)的烧杯中,完全反应后,称量烧杯内物质的总质量为66.8g。
已知过氧化钙与水反应的化学方程式为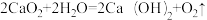 。请计算:
。请计算:
(1)生成氧气___________ g:
(2)该样品中过氧化钙的质量分数。(写出计算过程)
已知过氧化钙与水反应的化学方程式为
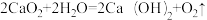 。请计算:
。请计算:(1)生成氧气
(2)该样品中过氧化钙的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】石灰石是生产水泥、玻璃、石灰等建筑材料的重要原料。我市石灰石资源丰富,某课外兴趣小组的同学通过测定某地石灰石中碳酸钙的质量分数,来判断是否有开采使用价值。他们称取该地石灰石样品8.0g于烧杯中,将80g稀盐酸分4次加入烧杯中,充分反应后(杂质不溶于水且不与稀盐酸反应),测得剩余固体的质量记录如下、
(1)表中m的值为______ 。
(2)该石灰石样品中碳酸钙的质量分数是______ 。
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
| 加入稀盐酸质量/g | 20 | 20 | 20 | 20 |
| 剩余固体质量/g | m | 4.0 | 2.0 | 1.2 |
(2)该石灰石样品中碳酸钙的质量分数是
(3)所用稀盐酸中溶质的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为了测定鸡蛋壳中碳酸钙的质量分数,某兴趣小组进行如下实验,将12g鸡蛋壳洗净、捣碎后,全部投入到盛有足量稀盐酸的烧杯中,电子秤的示数变化情况如图。(鸡蛋壳中的其他成分不溶于水,也不与稀盐酸反应)

请分析并计算:
(1)生成二氧化碳的质量为________ g。
(2)计算该鸡蛋壳中碳酸钙的质量分数(结果精确至0.1%)。

请分析并计算:
(1)生成二氧化碳的质量为
(2)计算该鸡蛋壳中碳酸钙的质量分数(结果精确至0.1%)。
您最近一年使用:0次




