水和溶液在生产生活中有着重要的作用。
(1)生活中可以用_____ 检验某水样是硬水还是软水。
(2)水可参与许多化学反应。一种家用环保型消毒液发生器的反应原理是:在通电条件下,氯化钠和水反应生成氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式是_____ 。
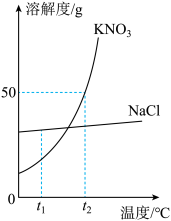
(3)如图为KNO3和NaCl两种物质的溶解度曲线。t1℃时,两种物质溶解度的大小关系:NaCl_____ KNO3(填“>”或“=”或“<”)。将饱和KNO3溶液变为不饱和KNO3溶液,可行的方法之一是添加溶剂(水),还可以是_____ 。

(1)生活中可以用
(2)水可参与许多化学反应。一种家用环保型消毒液发生器的反应原理是:在通电条件下,氯化钠和水反应生成氢氧化钠、氢气和氯气(Cl2),该反应的化学方程式是
(3)如图为KNO3和NaCl两种物质的溶解度曲线。t1℃时,两种物质溶解度的大小关系:NaCl
更新时间:2023-07-03 19:23:12
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下列短文,回答相关问题。
新型塑料—聚乳酸塑料
随着国内外禁塑令的颁发和升级,以聚乳酸(polylacticacid,PLA)为代表的生物基塑料成为传统石油基塑料市场的主要替代品,备受青睐。PLA来源于可再生的生物资源,并且具有优异的生物降解性和良好的力学性能,已发展为具有巨大增长潜力的行业。
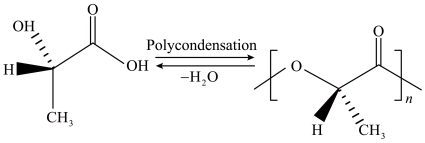
PLA是以生物发酵产生的乳酸(C3H6O3)为主要原料聚合得到的聚合物。单个的乳酸分子中有一个羟基和一个羧基,多个乳酸分子在一起,羟基与别的分子的羧基脱水缩合,羧基与别的分子的羟基脱水缩合,形成了聚乳酸。
生物降解通常指的是可以在一定生物活性环境下降解转化为二氧化碳和水的过程。目前已发现的能降解PLA塑料的微生物有细菌、放线菌和真菌,降解主要存在于堆肥、淡水、厌氧和土壤等多种自然环境中。
PLA作为一种生物基可降解塑料,只有在温度高于58℃和高湿度的密闭工业堆肥环境中,PLA才可以降解,在自然条件下分解选率依旧缓慢,较难实现彻底分解。尤其在海水中,PLA材料经过52周后其表面形态、重量、分子量以及机械性能几乎没有发生变化,随意丢弃到自然环境中同样会造成环境污染问题。
(1)人体在剧烈运动后会产生大量乳酸(C3H6O3),乳酸在酶的作用下最终氧化成二氧化碳和水,请写出乳酸氧化的化学方程式___________ 。
(2)根据乳酸直接缩聚法合成PLA,推测PLA由___________ (填元素符号)元素组成,该合成过程属于___________ 变化(填“物理”或“化学”)。
(3)为了促进细菌等微生物降解PLA塑料,可以控制的比较合适的条件是___________ 。
(4)下列说法错误的是___________。
新型塑料—聚乳酸塑料
随着国内外禁塑令的颁发和升级,以聚乳酸(polylacticacid,PLA)为代表的生物基塑料成为传统石油基塑料市场的主要替代品,备受青睐。PLA来源于可再生的生物资源,并且具有优异的生物降解性和良好的力学性能,已发展为具有巨大增长潜力的行业。
PLA是以生物发酵产生的乳酸(C3H6O3)为主要原料聚合得到的聚合物。单个的乳酸分子中有一个羟基和一个羧基,多个乳酸分子在一起,羟基与别的分子的羧基脱水缩合,羧基与别的分子的羟基脱水缩合,形成了聚乳酸。

生物降解通常指的是可以在一定生物活性环境下降解转化为二氧化碳和水的过程。目前已发现的能降解PLA塑料的微生物有细菌、放线菌和真菌,降解主要存在于堆肥、淡水、厌氧和土壤等多种自然环境中。
PLA作为一种生物基可降解塑料,只有在温度高于58℃和高湿度的密闭工业堆肥环境中,PLA才可以降解,在自然条件下分解选率依旧缓慢,较难实现彻底分解。尤其在海水中,PLA材料经过52周后其表面形态、重量、分子量以及机械性能几乎没有发生变化,随意丢弃到自然环境中同样会造成环境污染问题。
(1)人体在剧烈运动后会产生大量乳酸(C3H6O3),乳酸在酶的作用下最终氧化成二氧化碳和水,请写出乳酸氧化的化学方程式
(2)根据乳酸直接缩聚法合成PLA,推测PLA由
(3)为了促进细菌等微生物降解PLA塑料,可以控制的比较合适的条件是
(4)下列说法错误的是___________。
| A.用于合成PLA的乳酸属于有机高分子化合物 |
| B.利用微生物来降解PLA,温度越高越好 |
| C.PLA材料在海水中较难降解的原因,可能与海水的温度过低有关 |
| D.未来如果能用生物基塑料完全代替传统石油基塑料,就不可能产生“白色污染” |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知 32g 纯净物 X(相对分子质量为 32)在足量的氧气中充分燃烧,生成 44g 二氧化碳和 36g 水。则X 物质中碳、氢原子的个数比为___________ ,该反应的化学方程式为___________ 。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】2019年12月17日,舷号“17”的中国首艘国产002航母山东举行交接入列仪式,标志着我国在航海及军事领域取得重大突破。根据所学化学知识填空:
(1)建造航母用到了钛合金,构成金属钛的粒子是_____ 。
(2)TiC14在高温下与过量的镁反应可制得金属钛,同时生成氯化镁,写出此反应的化学方程式_____ 。
(3)航母外壳用涂料覆盖,是为了防止钢铁材料与_____ 接触而锈蚀。
(4)工业上冶炼2000t含杂质3%的生铁,需要含四氧化三铁90%的磁铁矿石的质量是_____ t(结果精确到0.1)。
(5)在硝酸亚铁和硝酸铜的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,则滤出的固体一定含有的物质_____ (填化学式)。
(1)建造航母用到了钛合金,构成金属钛的粒子是
(2)TiC14在高温下与过量的镁反应可制得金属钛,同时生成氯化镁,写出此反应的化学方程式
(3)航母外壳用涂料覆盖,是为了防止钢铁材料与
(4)工业上冶炼2000t含杂质3%的生铁,需要含四氧化三铁90%的磁铁矿石的质量是
(5)在硝酸亚铁和硝酸铜的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,则滤出的固体一定含有的物质
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】坚持“人与自然和谐共生”是新时代中国特色社会主义的基本方略之一,让“山更绿,水更清,空气更清新”是我们共同的追求。
(1)长期饮用硬水对健康不利,生活中常用_______________ 区分硬水和软水;小艳同学发现长时间烧煮水的水壶中有水垢,她用厨房里的_______________ (填标号)轻松将水垢除去。
A.食盐水
B.食醋
C.料酒
D.蚝油
(2)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的_______________ 操作;在盛有水的烧杯中加入以下某种物质,形成溶液过程中,温度没有明显变化的是_______________ (填字母)。
A.烧碱
B.硝酸铵
C.氯化钠
D.浓硫酸
(3)C1O2是饮用水常用的消毒剂,制取C1O2的化学方程式为: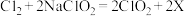 ,X的化学式
,X的化学式_______________ ;医用生理盐水中含有一定量的氯离子,请写出C1-的离子结构示意图___________ 。市售“自热米饭”的自热原理是:让饭盒夹层中的水与生石灰接触,反应并放出大量的热。该反应的化学方程式是______________________ 。
(1)长期饮用硬水对健康不利,生活中常用
A.食盐水
B.食醋
C.料酒
D.蚝油
(2)把磨好的豆浆倒在纱布袋中将渣和浆分离,相当于化学实验中的
A.烧碱
B.硝酸铵
C.氯化钠
D.浓硫酸
(3)C1O2是饮用水常用的消毒剂,制取C1O2的化学方程式为:
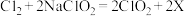 ,X的化学式
,X的化学式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】人类的日常生活和工农业生产离不开水。请回答:
(1)某地下水中含有较多可溶性钙、镁矿物质,该水属于____________ (填“软水”或“硬水”)。
(2)自然界中的水一般要净化后才能使用,在沉降、过滤、吸附、蒸馏等净水方法中,单一操作相对净化程度最高的是____________ 。
(3)下列关于水的说法中,不正确 的是 。
(4)生活中常用____________ 的方法降低水的硬度。
(1)某地下水中含有较多可溶性钙、镁矿物质,该水属于
(2)自然界中的水一般要净化后才能使用,在沉降、过滤、吸附、蒸馏等净水方法中,单一操作相对净化程度最高的是
(3)下列关于水的说法中,
| A.软水是纯净物 | B.水中某些杂质可用活性炭吸附除去 |
| C.洗菜、洗衣后的水用来冲洗厕所 | D.合理施用农药、化肥,以减少水体污染 |
您最近一年使用:0次
【推荐3】2022年6月5日,神舟十四号载人飞船与“天宫”空间站成功对接,“天宫”中水和氧气的最大化利用是生活保障的重要措施。图1是空间站资源再利用模拟图。

(1)“水净化系统”中活性炭可以除去色素和异味,是因为活性炭________ 。最终得到的饮用水为软水,生活中常用________ 区分硬水和软水。
(2)“萨巴蒂尔反应器”可除去二氧化碳。在300~400℃、催化剂条件下,将二氧化碳和氢气转化为甲烷(CH4)和水,请写出反应的符号表达式:________ 。
(3)宇航员一部分生活用氧可通过“水电解系统”制得。图2是电解水的实验室装置示意图,请回答下列问题:据图可知,a管与电源的________ (选填“正”或“负”)极端相连。该实验说明水是由________ 组成的,该变化中的最小微粒是________ 。
(4)反应一段时间后,切断上述装置中的电源,检验电解反应后a、b两管中得到的气体请完成下表:
(5)电解水的符号表达式:________ 。
(6)电解水时常加入一些NaOH,目的是:________ 。
(7)实验结束后,发现VH2:VO2>2:1,可能原因是:________ 。(任写一条即可)

(1)“水净化系统”中活性炭可以除去色素和异味,是因为活性炭
(2)“萨巴蒂尔反应器”可除去二氧化碳。在300~400℃、催化剂条件下,将二氧化碳和氢气转化为甲烷(CH4)和水,请写出反应的符号表达式:
(3)宇航员一部分生活用氧可通过“水电解系统”制得。图2是电解水的实验室装置示意图,请回答下列问题:据图可知,a管与电源的
(4)反应一段时间后,切断上述装置中的电源,检验电解反应后a、b两管中得到的气体请完成下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 依次打开a、b管活塞,分别用 | a管: | a管中得到的气体是 |
| b管:木条复燃 | b管中得到的气体是 |
(5)电解水的符号表达式:
(6)电解水时常加入一些NaOH,目的是:
(7)实验结束后,发现VH2:VO2>2:1,可能原因是:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题。
(1)面对依然严重的新冠肺炎疫情。我国全民战疫,众志成城,战疫工作成效显著,为构建人类命运共同体作出了重大贡献。配合防疫,养成室内定期消毒的习惯特别重要。84消毒液、75%的酒精溶液、过氧乙酸溶液、醋酸溶液等是常用消毒产品,我们要按照使用说明进行消毒操作。

①在使用84消毒液之前要先按照一定比例加水稀释,然后才能使用。市场上的84消毒液都是浓缩液,主要有效成分为NaClO,具有强氧化性,漂白性,不可直接用手触碰。在NaClO中,氯元素的化合价为___________ 。
②居家使用84消毒液时,切勿与洁厕灵等强酸类清洗剂混合使用。这是因为两者相遇会发生如下反应:2HCl + NaClO=NaCl+ R + Cl2↑,生成的氯气是有毒气体。请写出物质R的化学式:___________ 。
③过氧乙酸(CH3COOOH)也是很好的消毒剂。一个过氧乙酸分子中含有_________ 个原子,过氧乙酸中碳、氢元素的质量比为__________ (填最简整数比),过氧乙酸中质量分数最小的元素是________ (写元素符号)。
④在抗击疫情的过程中,下列认识,你认为符合 科学道理的是________ (填写序号字母)
A.家庭消毒时,消毒液越浓越好 B.勤洗手
C.应经常保持室内清洁卫生和通风 D.出门佩戴口罩
(2)侯氏制碱法是以食盐(NaC1)为主要原料制取纯碱,同时得到可用作化学肥料的物质氯化铵(NH4Cl)。NaCl和NH4Cl的溶解度曲线如图所示,请回答下列问题:

①如图所示,t2℃时,NH4C1的溶解度是_____ g。
②通过NaCl的溶解度曲线,可判断出海水“晒盐”是用________ 的方法从海水中得到NaCl(填写“蒸发结晶”“降温结晶”之一)。
③t1℃时,将相同质量的NH4Cl饱和溶液和NaCl饱和溶液均升温至t2℃,此时,NH4Cl溶液的溶质质量________ NaCl溶液的溶质质量(填写“大于”“等于”“小于”“无法判断”之一)。
(1)面对依然严重的新冠肺炎疫情。我国全民战疫,众志成城,战疫工作成效显著,为构建人类命运共同体作出了重大贡献。配合防疫,养成室内定期消毒的习惯特别重要。84消毒液、75%的酒精溶液、过氧乙酸溶液、醋酸溶液等是常用消毒产品,我们要按照使用说明进行消毒操作。

①在使用84消毒液之前要先按照一定比例加水稀释,然后才能使用。市场上的84消毒液都是浓缩液,主要有效成分为NaClO,具有强氧化性,漂白性,不可直接用手触碰。在NaClO中,氯元素的化合价为
②居家使用84消毒液时,切勿与洁厕灵等强酸类清洗剂混合使用。这是因为两者相遇会发生如下反应:2HCl + NaClO=NaCl+ R + Cl2↑,生成的氯气是有毒气体。请写出物质R的化学式:
③过氧乙酸(CH3COOOH)也是很好的消毒剂。一个过氧乙酸分子中含有
④在抗击疫情的过程中,下列认识,你认为
A.家庭消毒时,消毒液越浓越好 B.勤洗手
C.应经常保持室内清洁卫生和通风 D.出门佩戴口罩
(2)侯氏制碱法是以食盐(NaC1)为主要原料制取纯碱,同时得到可用作化学肥料的物质氯化铵(NH4Cl)。NaCl和NH4Cl的溶解度曲线如图所示,请回答下列问题:

①如图所示,t2℃时,NH4C1的溶解度是
②通过NaCl的溶解度曲线,可判断出海水“晒盐”是用
③t1℃时,将相同质量的NH4Cl饱和溶液和NaCl饱和溶液均升温至t2℃,此时,NH4Cl溶液的溶质质量
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐2】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是_________ (填A或B)。
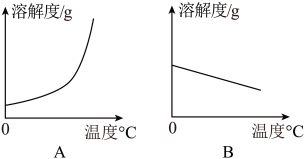
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。
其中措施正确的是____________ 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为___________ 。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙__________ 甲(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是___________________ 。
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的
pH___________ (填“偏大”、“偏小”或“不受影响”)。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是

(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。
其中措施正确的是
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的
pH
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】下图是A、B、C三种固体物质的溶解度曲线.据图回答下列问题。

(1)t2℃时,将60克A溶于50克水中得到溶液的质量为_____________ 克。
(2)将相同质量t2℃时的A.、B、C饱和溶液的温度降低到t1℃时,析出晶体最多的是____________ 。
(3)将t1℃时的A、 B、 C饱和溶液的温度升高到t2℃时,溶质质量分数最大的是___________ 。

(1)t2℃时,将60克A溶于50克水中得到溶液的质量为
(2)将相同质量t2℃时的A.、B、C饱和溶液的温度降低到t1℃时,析出晶体最多的是
(3)将t1℃时的A、 B、 C饱和溶液的温度升高到t2℃时,溶质质量分数最大的是
您最近一年使用:0次
【推荐2】溶解度是衡量物质溶解能力大小且能表达物质的固有属性。

(1)不同温度下,O2的溶解度随压强的变化如图1所示,图中t1对应的温度为40℃,则t2对应的温度______ 。(填序号,下同)
a.小于40℃ b.大于40℃ c.无法确定
(2)某学生在教师的指导下完成 溶解度的测定实验。
溶解度的测定实验。
步骤1:分别准确称取3.8g、1.2g。称量过程中,加入药品后发现托盘天平指针向右偏,则接下来的操作是______ 。
a.添加 直至天平平衡
直至天平平衡
b.改变砝码、游码,直至天平平衡
步骤2:将3.8g 放入大试管中,并用量筒量取10.0mL蒸馏水于试管内。(水的密度为1g/mL)
放入大试管中,并用量筒量取10.0mL蒸馏水于试管内。(水的密度为1g/mL)
步骤3:振荡大试管,发现有固体未溶解,于是用如图2所示方法进行水浴加热,使固体全部溶解,则此加热方法除受热均匀外,还具有的优点是______ 。
(3)图3为A物质的溶解度曲线M、N两点分别表示A物质的两种溶液。若要实现M→N的方法是(A从溶液中析出时不带结晶水)______ 。

(1)不同温度下,O2的溶解度随压强的变化如图1所示,图中t1对应的温度为40℃,则t2对应的温度
a.小于40℃ b.大于40℃ c.无法确定
(2)某学生在教师的指导下完成
 溶解度的测定实验。
溶解度的测定实验。步骤1:分别准确称取3.8g、1.2g。称量过程中,加入药品后发现托盘天平指针向右偏,则接下来的操作是
a.添加
 直至天平平衡
直至天平平衡 b.改变砝码、游码,直至天平平衡
步骤2:将3.8g
 放入大试管中,并用量筒量取10.0mL蒸馏水于试管内。(水的密度为1g/mL)
放入大试管中,并用量筒量取10.0mL蒸馏水于试管内。(水的密度为1g/mL)步骤3:振荡大试管,发现有固体未溶解,于是用如图2所示方法进行水浴加热,使固体全部溶解,则此加热方法除受热均匀外,还具有的优点是
(3)图3为A物质的溶解度曲线M、N两点分别表示A物质的两种溶液。若要实现M→N的方法是(A从溶液中析出时不带结晶水)
您最近一年使用:0次





