为测定某苏打样品中碳酸钠的含量,称取 20g 苏打样品(杂质不参加反应) 放入烧杯中,加入 200g 稀盐酸,二者恰好完全反应,反应后烧杯中剩余物质的总质量为 213.4g(气体的溶解忽略不计)。请计算:
(1)生成二氧化碳气体的质量为_____ g。
(2)写出反应的化学方程式_____ 。
(3)该样品中碳酸钠的质量分数_____ 。
(1)生成二氧化碳气体的质量为
(2)写出反应的化学方程式
(3)该样品中碳酸钠的质量分数
更新时间:2023/07/19 10:11:12
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
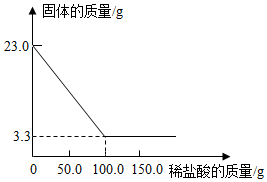
【推荐1】实验室有不纯的氯酸钾样品25.0 g,把该样品与少量二氧化锰混合加热制取氧气(杂质不参加反应),充分反应后,固体混合物质量变化如下所示:
(1)生成氧气的质量为______ g;
(2)不纯的氯酸钾在样品中氯酸钾的质量是多少?
| 反应前固体总质量 | 反应后固体总质量 |
| 26.0g | 16.4g |
(2)不纯的氯酸钾在样品中氯酸钾的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】在实验室加热32.5g二氧化锰和氯酸钾的固体混合物制取氧气时,剩余固体物质的质量变化如图所示。请回答:________ g。
(2)完全反应后,剩余的固体物质是________ 。
(3)成年人每分钟大约需装吸入8L氧气,则每分钟大致需要空气________ L。

(2)完全反应后,剩余的固体物质是
(3)成年人每分钟大约需装吸入8L氧气,则每分钟大致需要空气
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】一定质量的氯酸钾( )中加入
)中加入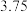 克二氧化锰(
克二氧化锰( ),充分混合加热,如图为加热过程中氧气质量随时间变化的曲线,根据图像分析并计算。
),充分混合加热,如图为加热过程中氧气质量随时间变化的曲线,根据图像分析并计算。___________ 克。
(2)原混合物中氯酸钾占整个混合物的质量分数。(写出计算过程)
 )中加入
)中加入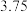 克二氧化锰(
克二氧化锰( ),充分混合加热,如图为加热过程中氧气质量随时间变化的曲线,根据图像分析并计算。
),充分混合加热,如图为加热过程中氧气质量随时间变化的曲线,根据图像分析并计算。
(2)原混合物中氯酸钾占整个混合物的质量分数。(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
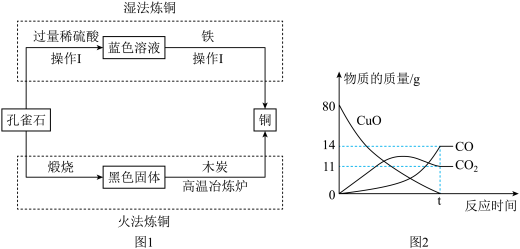
【推荐1】古籍《淮南万毕术》中记载了湿法炼铜技术,《大冶赋》中记载了火法炼铜技术。图1是以孔雀石【主要成分为Cu2(OH)2CO3,其他杂质不反应】为原料演绎古代两种炼铜技术。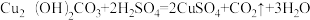
(1)“湿法炼铜”加入铁,利用了铁的金属活动性比铜的______ (选填“强”或“弱”)。蓝色溶液的pH______ 7(选填“>”、“<”或“=”)。
(2)用25g孔雀石与过量稀硫酸反应生成4.4g的CO2,孔雀石中Cu2(OH)2CO3的质量分数是多少?
(3)据“火法炼铜”原理,将9g炭粉和80g氧化铜混合物隔绝空气高温,部分物质的质量变化如图2,该实验发生的化学方程式______ 。
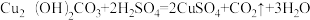
(1)“湿法炼铜”加入铁,利用了铁的金属活动性比铜的
(2)用25g孔雀石与过量稀硫酸反应生成4.4g的CO2,孔雀石中Cu2(OH)2CO3的质量分数是多少?
(3)据“火法炼铜”原理,将9g炭粉和80g氧化铜混合物隔绝空气高温,部分物质的质量变化如图2,该实验发生的化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
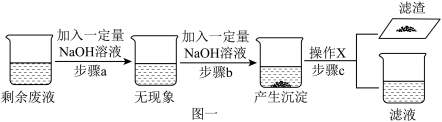
【推荐2】某化学兴趣小组欲探究实验室氧化铜和稀硫酸反应后某剩余废液的溶质成分,其实验步骤及对应实验现象如图一所示:______ 。
(2)实验中加入NaOH溶液的溶质质量分数均为 在上述实验过程中,产生沉淀的质量与加入NaOH溶液的质量关系如图二所示。试回答:
在上述实验过程中,产生沉淀的质量与加入NaOH溶液的质量关系如图二所示。试回答:______ (选填“a”“b”“c”之一)。
②当滴入 的
的 溶液
溶液 时(至图中
时(至图中 点),烧杯中溶液里一定大量存在的阴离子是
点),烧杯中溶液里一定大量存在的阴离子是______ (写离子符号)。
③当滴入 的
的 溶液
溶液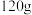 时(即图中B点),试通过计算,求生成沉淀的质量
时(即图中B点),试通过计算,求生成沉淀的质量______ 。(写出计算过程,计算结果精确到0.1)
(2)实验中加入NaOH溶液的溶质质量分数均为
 在上述实验过程中,产生沉淀的质量与加入NaOH溶液的质量关系如图二所示。试回答:
在上述实验过程中,产生沉淀的质量与加入NaOH溶液的质量关系如图二所示。试回答: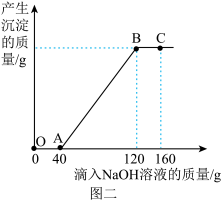
②当滴入
 的
的 溶液
溶液 时(至图中
时(至图中 点),烧杯中溶液里一定大量存在的阴离子是
点),烧杯中溶液里一定大量存在的阴离子是③当滴入
 的
的 溶液
溶液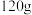 时(即图中B点),试通过计算,求生成沉淀的质量
时(即图中B点),试通过计算,求生成沉淀的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】纳米氧化亚铜(Cu2O)有优越的光催化性能被应用于废水处理,同时是制备传感器和高温超导材料。烧结法制备纳米氧化亚铜是以纯铜粉为原料,工艺流程如下:____________ 。
(2)反应①是在氧气中进行灼烧,其反应的化学方程式为________________ 。
(3)反应②是在密闭条件下进行烧结,反应的化学方程式为 CuO+Cu Cu2O。制备80kg含Cu2O 90%的纳米氧化亚铜,理论上需要CuO的质量是多少?(写出计算过程)
Cu2O。制备80kg含Cu2O 90%的纳米氧化亚铜,理论上需要CuO的质量是多少?(写出计算过程)
(4)经检测,80kg产品中含氧元素12%,则其中含CuO的质量_______ kg、Cu的质量_______ kg。
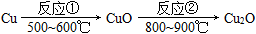
(2)反应①是在氧气中进行灼烧,其反应的化学方程式为
(3)反应②是在密闭条件下进行烧结,反应的化学方程式为 CuO+Cu
 Cu2O。制备80kg含Cu2O 90%的纳米氧化亚铜,理论上需要CuO的质量是多少?(写出计算过程)
Cu2O。制备80kg含Cu2O 90%的纳米氧化亚铜,理论上需要CuO的质量是多少?(写出计算过程)(4)经检测,80kg产品中含氧元素12%,则其中含CuO的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】工业上常用氢氧化钠溶液处理铝土矿(主要成分Al2O3),反应的化学方程式:Al2O3 + 2NaOH = 2NaAlO2 +H2O。现欲对204 t含Al2O3 为10%的铝土矿进行处理(杂质不参与反应)。求:
(1)204t铝土矿中 Al2O3 的质量为______ t,Al2O3中铝元素的质量为______ t;
(2)如要全部处理完上述铝土矿,理论上需要消耗NaOH的质量为多少?_____
(1)204t铝土矿中 Al2O3 的质量为
(2)如要全部处理完上述铝土矿,理论上需要消耗NaOH的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】为测定某纯碱样品中Na2CO3的质量分数,取20g该样品于烧杯中,滴加稀硫酸至不再产生气泡为止,加入稀硫酸的质量与产生气体的质量关系如图所示。(反应的化学方程式为: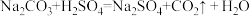 ;杂质不参加反应)
;杂质不参加反应)_______________ 。
(2)列式计算该纯碱样品中Na2CO3的质量分数。
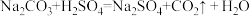 ;杂质不参加反应)
;杂质不参加反应)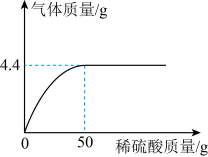
(2)列式计算该纯碱样品中Na2CO3的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上用高温煅烧石灰石的方法制备大量二氧化碳。为了测定某石灰石中碳酸钙的质量分数,称取6.25g石灰石样品研碎成粉末加热至高温(杂质不参加反应),冷却,每次称得剩余固体质量如下表:
计算:
(1)完全反应后生成二氧化碳多少克?
(2)石灰石中碳酸钙的质量分数多少?
| 操作次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 剩余固体质量(g) | 4.25 | 4.15 | 4.05 | 4.05 |
(1)完全反应后生成二氧化碳多少克?
(2)石灰石中碳酸钙的质量分数多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】化学兴趣小组同学为了测定烧碱的变质情况,取烧碱样品13g进行下列实验:
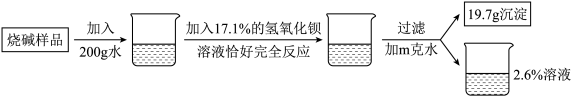
(1)写出上述反应的化学方程式_____________________________;
(2)列出求解混合物中参加反应的物质质量(X)的比例式________________________;
(3)未变质前氢氧化钠的质量是________________________;
(4)加入水的质量m的值是________________________;
(5)用这种方法制取20.8g的氢氧化钠,需要此烧碱样品的质量为________________________。

(1)写出上述反应的化学方程式_____________________________;
(2)列出求解混合物中参加反应的物质质量(X)的比例式________________________;
(3)未变质前氢氧化钠的质量是________________________;
(4)加入水的质量m的值是________________________;
(5)用这种方法制取20.8g的氢氧化钠,需要此烧碱样品的质量为________________________。
您最近一年使用:0次