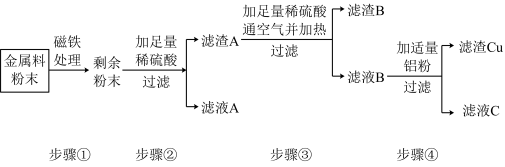
某化学兴趣小组拟从一种由铝、铁、铜、银四种金属粉末组成的混合物中回收铁、铜和银并得到硫酸铝,他们设计了如图所示的流程并进行操作。请回答:
已知: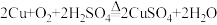 ,银在该条件下不发生反应。
,银在该条件下不发生反应。
(1)过滤操作需要的玻璃仪器有烧杯、玻璃棒和______ ,玻璃棒的作用是______ 。
(2)步骤①“磁铁处理”的目的是______ 。
(3)步骤③能观察到的现象是:固体部分溶解,溶液______ ,所得滤渣B的成分是______ 。
(4)步骤 中发生反应的化学方程式是:
中发生反应的化学方程式是:______ 。
(5)硫酸铝可代替明矾净水,说明硫酸铝溶于水后也能生成胶状物______ 水中的悬浮物。

已知:
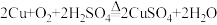 ,银在该条件下不发生反应。
,银在该条件下不发生反应。(1)过滤操作需要的玻璃仪器有烧杯、玻璃棒和
(2)步骤①“磁铁处理”的目的是
(3)步骤③能观察到的现象是:固体部分溶解,溶液
(4)步骤
 中发生反应的化学方程式是:
中发生反应的化学方程式是:(5)硫酸铝可代替明矾净水,说明硫酸铝溶于水后也能生成胶状物
更新时间:2023-07-04 18:25:57
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】某废旧电子产品中含有Fe、Cu、Au、Ni(镍)等金属,某工厂回收部分金属的流程图如下、已知:硫酸镍的化学式为NiSO4; 2Cu+O2+2H2SO4 2CuSO4+2H2O
2CuSO4+2H2O

(1)操作I、II、III中都需要用到玻璃棒,其作用是______ 。
(2)初产品中加入稀硫酸发生反应的化学方程式______ (任写一个),其反应的基本类型是______ 。
(3)固体A的成分是______ (写化学式)。
(4)Cu、Fe、Ni的活动性由强到弱的顺序依次是______ 。
 2CuSO4+2H2O
2CuSO4+2H2O
(1)操作I、II、III中都需要用到玻璃棒,其作用是
(2)初产品中加入稀硫酸发生反应的化学方程式
(3)固体A的成分是
(4)Cu、Fe、Ni的活动性由强到弱的顺序依次是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
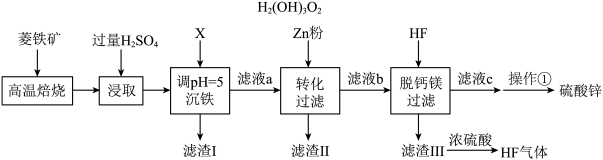
【推荐2】硫酸锌(ZnSO4)在防腐、电镀、医学上有诸多应用。硫酸锌可由菱锌矿制备,菱锌矿的主要成分为ZnCO3,杂质为SiO2以及Ca、Mg、Fe、Cu等元素的化合物。其制备流程如下:
资料:1.SiO2不能与硫酸发生化学反应,也不溶于水。
2.沉铁目的是将溶液中铁元素转为氢氧化铁沉淀。
(1)菱锌矿高温焙烧,ZnCO3分解生成ZnO和_________ 。
(2)为了提高锌的浸取效果,可采取的措施有__________ 。
(3)从降低成本、提高纯度等角度分析,加入的物质X最适宜的是___________。
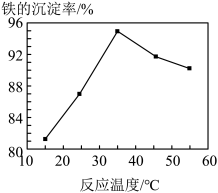
(4)由图可知,“沉铁”过程中适宜的温度是______ ℃。滤渣I的成分是__________ 。______ 和_______ ,最终溶液呈无色。比较Zn2+浓度:滤液a___________ (填“>”、“<”、“=”)滤液b。
(6)写出滤渣Ⅲ中的氟化钙(CaF2)或氟化镁(MgF2)与浓硫酸发生复分解反应的化学方程式:________ 。
(7)上述流程中可以回收再用的物质是___________ 。
资料:1.SiO2不能与硫酸发生化学反应,也不溶于水。
2.沉铁目的是将溶液中铁元素转为氢氧化铁沉淀。
(1)菱锌矿高温焙烧,ZnCO3分解生成ZnO和
(2)为了提高锌的浸取效果,可采取的措施有
(3)从降低成本、提高纯度等角度分析,加入的物质X最适宜的是___________。
| A.Cu | B.Ca(OH)2 | C.Na2CO3 | D.HCl |
(4)由图可知,“沉铁”过程中适宜的温度是
(6)写出滤渣Ⅲ中的氟化钙(CaF2)或氟化镁(MgF2)与浓硫酸发生复分解反应的化学方程式:
(7)上述流程中可以回收再用的物质是
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】某油脂厂废弃的镍催化剂主要含金属Ni、Al、Fe 及 Fe2O3等,还有少量其他不溶性物质。图 1 是回收镍制备硫酸镍晶体的工艺流程,图 2 是Fe 3+,Ni 2+从开始沉淀至沉淀完全时溶液 pH 的变化。请回答下列问题:

(1)“碱浸”的目的是______ 。
(2)“酸浸”时发生反应的化学方程式是______ (写一个)。
(3)生成滤渣③的化学方程式是______ 。
(4)“调 pH”时,为使溶液中的Fe 3+全部沉淀,而Ni 2+仍在溶液中,溶液 pH 的范围应是______ 。
(5)“浓缩结晶”获得硫酸镍晶体(NiSO4·7H2O)采用的方法是浓缩溶液、______ 结晶(填“降温”或“蒸发”)。

(1)“碱浸”的目的是
(2)“酸浸”时发生反应的化学方程式是
(3)生成滤渣③的化学方程式是
(4)“调 pH”时,为使溶液中的Fe 3+全部沉淀,而Ni 2+仍在溶液中,溶液 pH 的范围应是
(5)“浓缩结晶”获得硫酸镍晶体(NiSO4·7H2O)采用的方法是浓缩溶液、
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】水是生命的源泉,为了人类社会的可持续发展,我们应该了解水的有关知识。

(1)天然水中含有许多杂质,自来水厂通常对天然水进行、______ 、等几步处理,使之达到饮用水标准,在实验室里,若要得到净化程度最高的水,可用_____ 的方法。如下图所示的两个实验中,发生物理变化的是实验_____ ;实验B中没有发生改变的微粒是_____ ,试管2中得到的气体是_____ 。所以,你认为保持水化学性质的最小粒子_____ 。
(2)节约用水是每个公民的义务,我们应该提倡以下方式中的_____ (填字母序号)。
A 用淘米水、洗菜水浇花、冲厕所
B 不间断地放水洗衣服
C 不间断地放水刷牙
D 用喷灌、滴灌的方法浇灌农田和园林
(3)实验室中有一杯含有MgCl2和CaCl2的硬水,下表是某兴趣小组设计软化硬水的实验方案,请你一起来完成下表。可供选用的药品有Ca(OH)2溶液、NaOH溶液、Na2CO3溶液、肥皂水。

(1)天然水中含有许多杂质,自来水厂通常对天然水进行、
(2)节约用水是每个公民的义务,我们应该提倡以下方式中的
A 用淘米水、洗菜水浇花、冲厕所
B 不间断地放水洗衣服
C 不间断地放水刷牙
D 用喷灌、滴灌的方法浇灌农田和园林
(3)实验室中有一杯含有MgCl2和CaCl2的硬水,下表是某兴趣小组设计软化硬水的实验方案,请你一起来完成下表。可供选用的药品有Ca(OH)2溶液、NaOH溶液、Na2CO3溶液、肥皂水。
| 实验操作 | 现象 | 结论或化学方程式 |
| ①取少量硬水样品于试管中,向其滴加Ca(OH)2溶液,直到不再产生沉淀 | 有白色沉淀产生 | 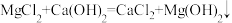 |
| ②再向上述试管中滴加 | 有白色沉淀产生 | 化学方程式: |
| ③过滤 | 滤出沉淀 | 得到澄清滤液 |
| ④用两试管分别取等量的上述滤液和原硬水样品,分别滴加 | 盛有滤液的试管中 | 证明硬水已软化 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】天然水净化为自来水的主要流程如下:

(1)下列说法不正确的是____________ (填字母)。
a.过滤池可以除去难溶性杂质
b.活性炭吸附池可以除去水中的色素和臭味
c.清水池中一定是软水
(2)明矾【KAl(SO4)m﹒12H2O】能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m=_____ 。
(3)下列实验能证明水是由氢元素和氧元素组成的是_______ (填字母序号)。
a.氢气在氧气中燃烧b.水的蒸发
c.水的电解d.水的净化
(4)目前不少自来水用液氯(Cl2)作为消毒剂,液氯注入水后发生反应的示意图如下:

其中“ ”、“
”、“ ”、“
”、“ ”代表不同原子,产物D为次氯酸(HClO),有杀菌作用。液氯与水反应的化学方程式是
”代表不同原子,产物D为次氯酸(HClO),有杀菌作用。液氯与水反应的化学方程式是__________ 。
(5)天然水中微生物使有机物(以C6H10O5表示)转化为CO2和H2O的过程中所需O2的量做生化需氧量(BOD,单位为mg﹒L-1),反应的化学方程式为: 测得20℃时1L某天然水样中含有有机物(C6H10O5)的质量为10.8mg,则该水样的BOD值是
测得20℃时1L某天然水样中含有有机物(C6H10O5)的质量为10.8mg,则该水样的BOD值是______ 。

(1)下列说法不正确的是
a.过滤池可以除去难溶性杂质
b.活性炭吸附池可以除去水中的色素和臭味
c.清水池中一定是软水
(2)明矾【KAl(SO4)m﹒12H2O】能作絮凝剂,是因为明矾溶于水后生成具有吸附作用的胶状物氢氧化铝。m=
(3)下列实验能证明水是由氢元素和氧元素组成的是
a.氢气在氧气中燃烧b.水的蒸发
c.水的电解d.水的净化
(4)目前不少自来水用液氯(Cl2)作为消毒剂,液氯注入水后发生反应的示意图如下:

其中“
 ”、“
”、“ ”、“
”、“ ”代表不同原子,产物D为次氯酸(HClO),有杀菌作用。液氯与水反应的化学方程式是
”代表不同原子,产物D为次氯酸(HClO),有杀菌作用。液氯与水反应的化学方程式是(5)天然水中微生物使有机物(以C6H10O5表示)转化为CO2和H2O的过程中所需O2的量做生化需氧量(BOD,单位为mg﹒L-1),反应的化学方程式为:
 测得20℃时1L某天然水样中含有有机物(C6H10O5)的质量为10.8mg,则该水样的BOD值是
测得20℃时1L某天然水样中含有有机物(C6H10O5)的质量为10.8mg,则该水样的BOD值是
您最近一年使用:0次
【推荐3】化学与生活息息相关。请回答下列问题:
(1)水是生命之源。如图是实验室电解水示意图。

①电解水的化学方程式为______ ,该反应属于______ (填基本反应类型);
②a、b两管中气体的体积比为______ ,请写出检验b管中气体的方法:______ (包括操作、现象)。
③我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,“—”表示催化剂)。
”表示氧原子,“—”表示催化剂)。

该分解微观过程的正确顺序是①→______ →______ →______ →③(填序号)。与电解水相比,该制氢方法的优点是______ 。
(2)某家用净水机工作原理如图所示:

①净水机中,活性炭的作用是______ 。
②经过净水机处理后的水是硬水还是软水,其检验方法为:______ (包括操作、现象、结论)。
③日常生活中常用______ 方法降低水的硬度。
(3)“见著知微”是化学学习者应该具备的基本素养,也是学习化学的重要思想方法。如图,是两种不同状态下的水分子模型图。

①在如图中你能获得的信息是______ 。(答一点即可)
②请从你所获得的信息中设计实验加以证明______ 。
(1)水是生命之源。如图是实验室电解水示意图。

①电解水的化学方程式为
②a、b两管中气体的体积比为
③我国科学家已研制出在新型高效光催化剂作用下,利用太阳能分解水制氢气。水在通过并接触催化剂表面时,分解的微观过程用示意图表示如下:(“
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,“—”表示催化剂)。
”表示氧原子,“—”表示催化剂)。
该分解微观过程的正确顺序是①→
(2)某家用净水机工作原理如图所示:

①净水机中,活性炭的作用是
②经过净水机处理后的水是硬水还是软水,其检验方法为:
③日常生活中常用
(3)“见著知微”是化学学习者应该具备的基本素养,也是学习化学的重要思想方法。如图,是两种不同状态下的水分子模型图。

①在如图中你能获得的信息是
②请从你所获得的信息中设计实验加以证明
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】某食盐样品中含有少量的氯化钙杂质,为了将杂质除去,并测定食盐中氯化钠的质量分数,某工厂实验员设计了如图实验流程进行实验:

根据如图流程图回答下列问题:
(1)操作I的名称是___ ,沉淀A化学式是___ ;
(2)滤液B中溶质成分有___ ,试剂甲是____ ;
(3)实验得到NaCl固体中还含有少量杂质,为了除去杂质.实验员对流程作出如下改进:在滤液B蒸发结晶之前,先滴加盐酸至不再产生气泡为止,该反应的化学方程式为___ ;改进流程中加入的盐酸稍过量也不会在NaCl固体中产生新的杂质,其原因是____ .
(4)实验员提出了两个数据测定方案.测定粗盐中氯化钠的质量分数.
方案一:称量食盐样品的质量和经洗涤、干燥的沉淀A或CaCl2固体的质量,并进行计算.
方案二:称量食盐样品的质量和实验改进后所得NaCl固体的质量,并进行计算.
请你判断:上述所选称量数据不合理的是方案____ ,理由是____ .

根据如图流程图回答下列问题:
(1)操作I的名称是
(2)滤液B中溶质成分有
(3)实验得到NaCl固体中还含有少量杂质,为了除去杂质.实验员对流程作出如下改进:在滤液B蒸发结晶之前,先滴加盐酸至不再产生气泡为止,该反应的化学方程式为
(4)实验员提出了两个数据测定方案.测定粗盐中氯化钠的质量分数.
方案一:称量食盐样品的质量和经洗涤、干燥的沉淀A或CaCl2固体的质量,并进行计算.
方案二:称量食盐样品的质量和实验改进后所得NaCl固体的质量,并进行计算.
请你判断:上述所选称量数据不合理的是方案
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐2】四氧化三铁是一种常用的磁性材料,由工业废料铁泥(含Fe、Fe2O3、FeO和杂质,杂质不参与反应)制取 的一种流程如下:
的一种流程如下:

(1)操作Ⅱ的名称是________________ 。
(2)Fe2O3与稀硫酸反应的化学方程式为____________ ,为使铁泥与稀硫酸充分反应,可采取的措施是_____________ (答出一点即可)。
(3)向溶液X中加入过量铁粉的作用是____________ 。
(4)FeOOH与FeSO3溶液在一定条件下反应生成 和
和___________ (填化学式)。
 的一种流程如下:
的一种流程如下:
(1)操作Ⅱ的名称是
(2)Fe2O3与稀硫酸反应的化学方程式为
(3)向溶液X中加入过量铁粉的作用是
(4)FeOOH与FeSO3溶液在一定条件下反应生成
 和
和
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
【推荐1】碳酸亚铁(FeCO3)是制取补血剂的原料,以下是用黄铜矿废液[溶质成份为Fe2(SO4)3、CuSO4及H2SO4]为原料,制备碳酸亚铁并回收铜的生产流程示意图:

已知:①Fe与Fe2(SO4)3溶液能发生反应生成FeSO4②溶液B中只有一种溶质。
(1)步骤1中,试剂A为_____ ,加入过量A的目的是使废液中Fe2(SO4)3、CuSO4及H2SO4全部转化为 _____ ;反应过程中观察到的现象之一是有红色固体析出,写出该反应的化学方程式 _____ 。
(2)操作a的名称:_____ 。
(3)步骤Ⅱ中,试剂C的化学式可能为_____ 等可溶性碳酸盐。
(4)步骤Ⅲ的目的是:除去“不溶物”中的另一种金属,回收得到纯净、干燥的铜。用化学方法回收铜的操作步骤为:加入过量的稀盐酸等酸、过滤、洗涤、干燥;回收铜的物理方法为_____ 。

已知:①Fe与Fe2(SO4)3溶液能发生反应生成FeSO4②溶液B中只有一种溶质。
(1)步骤1中,试剂A为
(2)操作a的名称:
(3)步骤Ⅱ中,试剂C的化学式可能为
(4)步骤Ⅲ的目的是:除去“不溶物”中的另一种金属,回收得到纯净、干燥的铜。用化学方法回收铜的操作步骤为:加入过量的稀盐酸等酸、过滤、洗涤、干燥;回收铜的物理方法为
您最近一年使用:0次




