钙是人体所需的重要元素之一,某化学小组用主要成分为碳酸钙的补钙剂进行如下实验。
【查阅资料】
①白醋的主要成分是醋酸(CH3COOH),可与碳酸钙反应,不与补钙剂中的其他成分反应。
②ppm常用来表示气体的浓度,数值越大,说明气体的浓度越高。
③碳酸钙与醋酸反应的化学方程式:
④实验过程中暂不考虑醋酸挥发。
I.验证补钙剂能与白醋反应。
【进行实验】
【解释与结论】
(1)补全实验中的现象_____ 。
【小组交流】
分组实验中,同学们发现产生气泡的速率不同,于是进行了如下探究。
Ⅱ.探究影响补钙剂与白醋反应速率的因素
【进行实验】
室温条件下进行实验,记录如下:
【解释与结论】
(2)上述实验中,反应速率最快的是_____ (填实验序号)。
(3)设计第1组实验的目的是_____ 。
(4)对比①③可得到的结论是_____ 。
【反思与评价】
(5)实验过程中,发现温度对该反应速率有影响。同学们再进行实验探究温度对反应速率的影响时,不需要控制相同的_____(填序号)。
(6)某产品包装注明,每片补钙剂中含钙元素600mg(补钙剂中的其他成分不含钙元素),则每片补钙剂中碳酸钙的质量为_____ mg。
【查阅资料】
①白醋的主要成分是醋酸(CH3COOH),可与碳酸钙反应,不与补钙剂中的其他成分反应。
②ppm常用来表示气体的浓度,数值越大,说明气体的浓度越高。
③碳酸钙与醋酸反应的化学方程式:

④实验过程中暂不考虑醋酸挥发。
I.验证补钙剂能与白醋反应。
【进行实验】
| 装置 | 现象 |
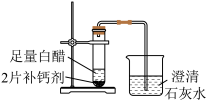 | 试管中的固体逐渐减少,有气泡产生,烧杯中_____。 |
(1)补全实验中的现象
【小组交流】
分组实验中,同学们发现产生气泡的速率不同,于是进行了如下探究。
Ⅱ.探究影响补钙剂与白醋反应速率的因素
【进行实验】
室温条件下进行实验,记录如下:
| 实验操作 | 组别 | 实验序号 | 补钙剂形态 | 白醋中酸浓度(g/100mL) | 二氧化碳浓度随时间的变化曲线 |
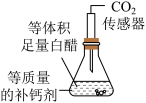 | 第1组 | ① | 片状 | 6 | 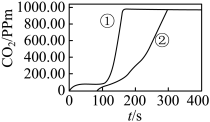 |
| ② | 片状 | 3 | |||
| 第2组 | ③ | 粉末 | 6 | 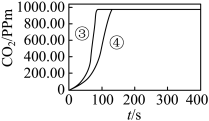 | |
| ④ | 粉末 | 3 |
(2)上述实验中,反应速率最快的是
(3)设计第1组实验的目的是
(4)对比①③可得到的结论是
【反思与评价】
(5)实验过程中,发现温度对该反应速率有影响。同学们再进行实验探究温度对反应速率的影响时,不需要控制相同的_____(填序号)。
| A.补钙剂的质量 |
| B.温度 |
| C.白醋中醋酸浓度 |
| D.白醋的体积 |
| E.补钙剂形态 |
更新时间:2023-07-02 20:56:23
|
相似题推荐
【推荐1】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学探究该气体的成分。
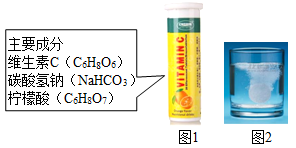
【猜想与假设】
小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_______ 。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO______ 。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
【得出结论】
(1)由实验A可知,该气体中肯定含有__________ ,写出该反应的化学方程式__________ 。
(2)由实验B_________ (填“能”或“不能”)确定该气体中不含氧气,理由是________ 。
【拓展延伸】关于维生素C(C6H8O6)和柠檬酸(C6H8O7)的下列说法错误的是__________ 。
A.均由碳、氢、氧三种元素组成的化合物
B.由于维生素C和柠檬酸的分子构成不同,因此性质差异很大
C.维生素C和柠檬酸中碳元素的质量分数相同
D.维生素C和柠檬酸中碳元素、氢元素和氧元素的质量比不同

【猜想与假设】
小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| A | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| B | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验A可知,该气体中肯定含有
(2)由实验B
【拓展延伸】关于维生素C(C6H8O6)和柠檬酸(C6H8O7)的下列说法错误的是
A.均由碳、氢、氧三种元素组成的化合物
B.由于维生素C和柠檬酸的分子构成不同,因此性质差异很大
C.维生素C和柠檬酸中碳元素的质量分数相同
D.维生素C和柠檬酸中碳元素、氢元素和氧元素的质量比不同
您最近一年使用:0次
【推荐2】金属的锈蚀与保护是初中化学的核心知识,某兴趣小组关于铜锈蚀和铁除锈、冶炼等进行如下实验探究。
【任务一】铜的锈蚀
某同学设计实验探究铜锈蚀产生铜绿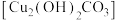 的条件(如图所示)。一段时间后,在A和B、D中没有观察到明显现象,C中铜片表面有铜绿。
的条件(如图所示)。一段时间后,在A和B、D中没有观察到明显现象,C中铜片表面有铜绿。
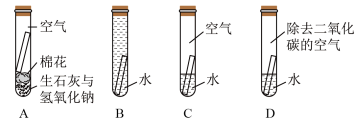
(1)实验中用的蒸馏水事先煮沸再冷却,目的是_____ 。
(2)A中生石灰与氢氧化钠的作用是_____ 。
(3)A、B、D与C对比,说明铜片锈蚀需要的物质是_____ 。
【任务二】铁的除锈
(4)写出一条生活中常见防止铁生锈的方法:_____ 。
(5)写出用稀盐酸除铁锈的化学方程式:_____ 。
(6)工业上用 还原
还原 。如图是48g氧化铁与过量的
。如图是48g氧化铁与过量的 反应,在不同温度下所得固体的质量和固体成分的图象。请回答问题。
反应,在不同温度下所得固体的质量和固体成分的图象。请回答问题。
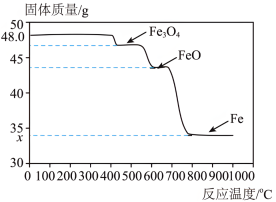
①获得铁的温度应不低于_____ ℃。(选填“400”“600”或“800”)
②图中
_____ 。
③为防止生成的铁在高温下氧化,可以进行的操作是_____ 。
【任务一】铜的锈蚀
某同学设计实验探究铜锈蚀产生铜绿
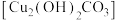 的条件(如图所示)。一段时间后,在A和B、D中没有观察到明显现象,C中铜片表面有铜绿。
的条件(如图所示)。一段时间后,在A和B、D中没有观察到明显现象,C中铜片表面有铜绿。
(1)实验中用的蒸馏水事先煮沸再冷却,目的是
(2)A中生石灰与氢氧化钠的作用是
(3)A、B、D与C对比,说明铜片锈蚀需要的物质是
【任务二】铁的除锈
(4)写出一条生活中常见防止铁生锈的方法:
(5)写出用稀盐酸除铁锈的化学方程式:
(6)工业上用
 还原
还原 。如图是48g氧化铁与过量的
。如图是48g氧化铁与过量的 反应,在不同温度下所得固体的质量和固体成分的图象。请回答问题。
反应,在不同温度下所得固体的质量和固体成分的图象。请回答问题。
①获得铁的温度应不低于
②图中

③为防止生成的铁在高温下氧化,可以进行的操作是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2)。该小组同学进行如下探究。
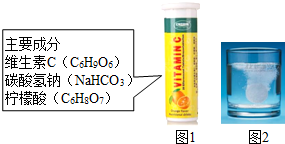
探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为_____ 。
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
【得出结论】(1)由实验①可知,该气体中肯定含有______ 。
(2)由实验②_____ (填“能”或“不能”)确定该气体中不含氧气,理由是_____ 。
探究二:泡腾片中碳酸氢钠的含量。
经测定维C泡腾片中钠元素的质量分数是6.9%,则该泡腾片中碳酸氢钠的质量分数是_____ %。

探究一:该气体的成分。
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2。
小明说:不可能含有N2,因为
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(2)由实验②
探究二:泡腾片中碳酸氢钠的含量。
经测定维C泡腾片中钠元素的质量分数是6.9%,则该泡腾片中碳酸氢钠的质量分数是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
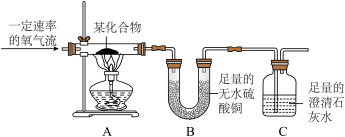
【推荐1】己知某化合物在氧气中完全燃烧只能生成二氧化碳和水,同学们利用如下装置探究该化合物的元素组成。
【查阅资料】无水硫酸铜遇水变蓝色。
【实验步骤】
①组装好装置后,装入药品前需要进行的实验操作是_______ 。
②缓缓通入一定速率的氧气流。
③分别称量装置B和装置C的质量。
④点燃酒精灯,使燃料充分燃烧。
⑤继续通入一段时间的氧气后,再次称量装置B和C的质量。
【实验现象】A中固体燃烧无剩余,B、C装置中的现象分别是_______ 。请写出C装置中反应的化学方程式_______ 。
【实验数据】该化合物起始质量为0.9g,B装置增重0.54g,C装置增重1.32g。
【实验结论】该化合物由_______ 元素组成且各元素的质量比为_______ 。
【实验反思】化合物充分燃烧后,仍然需要通入一段时间的氧气,其目的是_______ 。

【查阅资料】无水硫酸铜遇水变蓝色。
【实验步骤】
①组装好装置后,装入药品前需要进行的实验操作是
②缓缓通入一定速率的氧气流。
③分别称量装置B和装置C的质量。
④点燃酒精灯,使燃料充分燃烧。
⑤继续通入一段时间的氧气后,再次称量装置B和C的质量。
【实验现象】A中固体燃烧无剩余,B、C装置中的现象分别是
【实验数据】该化合物起始质量为0.9g,B装置增重0.54g,C装置增重1.32g。
【实验结论】该化合物由
【实验反思】化合物充分燃烧后,仍然需要通入一段时间的氧气,其目的是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】科学探究是学习化学最重要的方法,下面是对二氧化碳有关问题的研究,请回答有关问题:
(1)用一个空的软塑料瓶收集一瓶二氧化碳气体,在瓶中倒入 容积的水,立即盖紧瓶振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是
容积的水,立即盖紧瓶振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是_______________ 。
(2)如下图,从烧杯的一侧倾倒二氧化碳,观察到的现象是_______________________________ ,该实验说明二氧化碳_____________________________ 的物理性质和_____________________ 的化学性质。
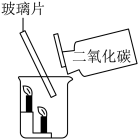
若没有玻璃片,可能产生的现象:____________________________________ 。
(3)如下图,准备好双孔塞(插有带小气球的短玻璃管和盛有澄清石灰水的分液漏斗)取装满二氧化碳的集气瓶,用双孔塞将集气瓶塞紧。把澄清石灰水放入集气瓶振荡,可观察到的现象是______________________________________ ;___________________________________________ 。其原因是____________________________________________ (用文字表达式表示)。
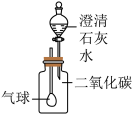
(4)某同学用石蕊试液染成紫色的干燥的小花做了两个实验:
实验一:把干燥的小花直接放到干燥二氧化碳的集气瓶中,无现象产生。说明:__________________________________ 。
实验二:用水喷湿后放入装有二氧化碳的集气瓶里(如图示)可观察到的现象______________________________ ,其原因是______________________ (用文字表达式表示)
(1)用一个空的软塑料瓶收集一瓶二氧化碳气体,在瓶中倒入
 容积的水,立即盖紧瓶振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是
容积的水,立即盖紧瓶振荡,观察到塑料瓶变瘪了,该现象说明二氧化碳具有的性质是(2)如下图,从烧杯的一侧倾倒二氧化碳,观察到的现象是

若没有玻璃片,可能产生的现象:
(3)如下图,准备好双孔塞(插有带小气球的短玻璃管和盛有澄清石灰水的分液漏斗)取装满二氧化碳的集气瓶,用双孔塞将集气瓶塞紧。把澄清石灰水放入集气瓶振荡,可观察到的现象是

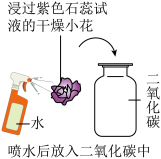
(4)某同学用石蕊试液染成紫色的干燥的小花做了两个实验:
实验一:把干燥的小花直接放到干燥二氧化碳的集气瓶中,无现象产生。说明:
实验二:用水喷湿后放入装有二氧化碳的集气瓶里(如图示)可观察到的现象

您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】小明在实验室进行了如下两个实验,回答下列问题。
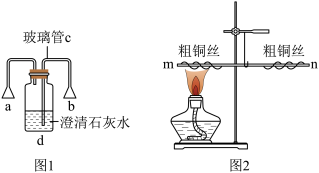
(1)用图1装置对人体吸入的空气和呼出的气体进行探究。实验操作及现象如表。
①吸气、呼气时,c处现象不同的原因是______ 。
②吸气、呼气时,d处现象不同,说明呼出气体中二氧化碳含量______ (填“高于”或“低于”)吸入空气中的二氧化碳含量。
(2)利用图2装置探究铜和氧气在加热条件下是否生成了新物质。
在一根用细铜丝吊着的玻璃棒两端分别绕上10cm长的粗铜丝,并使玻璃棒保持水平。然后用酒精灯给m端的粗铜丝加热1~2min。
①冷却后,观察到的现象是:m端铜丝变为______ 色,玻璃棒n端上升。
②取下m端加热后的粗铜丝,将其浸没于盛有稀盐酸的试管中,加热,一段时间后,可观察到试管中的液体变为______ 色。(已知铜与稀盐酸不发生化学反应)
由此说明:加热条件下,铜和氧气反应生成了新物质。

(1)用图1装置对人体吸入的空气和呼出的气体进行探究。实验操作及现象如表。
| 操作 | c处现象 | d处现象 |
| A.从a处缓缓吸气5次 | 无明显现象 | 石灰水不浑浊 |
| B.从b处缓缓呼气5次 | 出现无色液滴 | 石灰水变浑浊 |
②吸气、呼气时,d处现象不同,说明呼出气体中二氧化碳含量
(2)利用图2装置探究铜和氧气在加热条件下是否生成了新物质。
在一根用细铜丝吊着的玻璃棒两端分别绕上10cm长的粗铜丝,并使玻璃棒保持水平。然后用酒精灯给m端的粗铜丝加热1~2min。
①冷却后,观察到的现象是:m端铜丝变为
②取下m端加热后的粗铜丝,将其浸没于盛有稀盐酸的试管中,加热,一段时间后,可观察到试管中的液体变为
由此说明:加热条件下,铜和氧气反应生成了新物质。
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】某学习小组的同学对过氧化氢分解进行探究。
I.【探究一】影响过氧化氢分解快慢的因素
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
(1)对比①②可知,其他条件相同时,温度越高,过氧化氢分解越快,则t1_____ t2(填“>”“二”或“<”)。
(2)能说明过氧化氢分解快慢与溶质质量分数有关的实验是_________ (填实验序号),合理的结论是______ 。
【交流探讨】MnO2属于金属氧化物,其他金属氧化物能否起到类似MnO2的催化作用?
II.[探究二]探究FerOs是否对过氧化氢分解起催化作用。
【得出结论】Fe2O3能对过氧化氢的分解起催化作用。
I.【探究一】影响过氧化氢分解快慢的因素
分别取5mLH2O2溶液进行实验,测定产生4mLO2所需时间,实验结果记录如下:
| 实验序号 | H2O2溶液的溶质质量分数% | 温度℃ | MnO2粉末用量 | 反应时间 |
| ① | 30 | 35 | 0 | t1 |
| ② | 30 | 55 | 0 | t2 |
| ③ | 5 | 20 | 0.1 | 3s |
| ④ | 15 | 20 | 0.1 | 1s |
(2)能说明过氧化氢分解快慢与溶质质量分数有关的实验是
【交流探讨】MnO2属于金属氧化物,其他金属氧化物能否起到类似MnO2的催化作用?
II.[探究二]探究FerOs是否对过氧化氢分解起催化作用。
| 操作步骤 | 实验情况记录 | 结论 | |
| (1) |  | A试管上方带火星的木条未复燃,B中出现气泡快,带火星的木条复燃现象 | Fe2O3 |
| (2) | 将B试管中的混合物 | 固体质量为0.2 g | Fe2O3质量未变 |
| (3) | 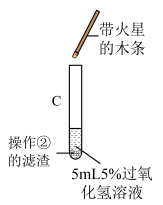 | C试管上方带火星的木条 | Fe2O3化学性质未变 |
您最近一年使用:0次
【推荐2】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
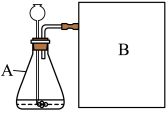
【进行实验】如图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是______ 。
【实验记录】
【结论】该探究过程得到的结论是______ 。
【反思】
(1)H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的化学性质和______ 是否改变。
(2)请你设计实验探究MnO2的化学性质在反应前后是否改变,简述:
实验操作:______ 。
现象及结论:______ 。
【假设】H2O2生成O2的快慢与催化剂种类有关
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
【进行实验】如图是他们进行实验的装置图,此实验中B处宜采用的气体收集方法是

【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2溶液 | 5%H2O2溶液 |
| 催化剂 | 1g水泥块 | 1g MnO2 |
| 时间 | 165秒 | 46秒 |
【反思】
(1)H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的化学性质和
(2)请你设计实验探究MnO2的化学性质在反应前后是否改变,简述:
实验操作:
现象及结论:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】以下是某研究小组用5mL的H2O2溶液,探究影响反应速率部分因素的相关实验数据。
(1)根据以上实验,写出过氧化氢溶液分解的符号表达式_________ 。
(2)通过实验①和②对比可知,化学反应速率与________ 有关;从实验________ 和_____ 对比可知,化学反应速率与温度的关系是________ 。
(3)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的碰撞概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是_______ 。
(4)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量_______ (选填“减小”或“不变”或“增大”)。
| 实验序号 | H2O2溶液浓度 | 温度℃ | MnO2的用量(g) | 收集氧气的体积(mL) | 反应所需的时间/s |
| ① | 5% | 20 | 0.1 | 4 | 16.75 |
| ② | 15% | 20 | 0.1 | 4 | 6.04 |
| ③ | 30% | 25 | 0 | 2 | 49.21 |
| ④ | 30% | 35 | 0 | 2 | 10.76 |
(1)根据以上实验,写出过氧化氢溶液分解的符号表达式
(2)通过实验①和②对比可知,化学反应速率与
(3)化学反应的实质是微观粒子相互接触、碰撞的结果,化学反应速率与微观粒子的碰撞概率有关。试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是
(4)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,产生氧气的总质量
您最近一年使用:0次



