《天工开物》中记载了一种“绿青”的宝石,是孔雀石的一种,其主要成分为碱式碳酸铜【Cu2(OH)2CO3】。在现代生产中被用于制造油漆、颜料等。某兴趣小组欲在实验室中制备碱式碳酸铜。
活动一:探究制备碱式碳酸铜的条件。
【查阅资料】碱式碳酸铜是翠绿色、难溶于水的固体,酸性条件下不稳定。
【进行实验】按下表中的数据进行图示实验,记录实验结果。
(1)操作一为:______ 。
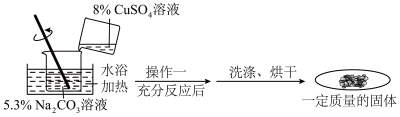
【解释与结论】
(2)为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH______ 7;
(3)分析步骤Ⅱ、IV、V的数据可知CuSO4溶液与Na2CO3溶液最佳配比,则x为______ ;
(4)分析步骤I、Ⅱ、Ⅲ的数据,实验的最佳温度为______ ℃;
活动二:探究步骤Ⅲ中所得固体颜色偏暗的原因。
【查阅资料】碱式碳酸铜受热分解会生成的CuO为黑色。
【猜想与假设】固体颜色偏暗是因为实验过程中生成了CuO。
【进行实验】
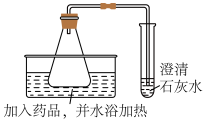
(5)如图所示,锥形瓶中加入的药品为50 mL CuSO4溶液和Na2CO3溶液,水浴温度为______ ,观察到固体变为暗绿色,澄清的石灰水变浑浊。
(6)【结论】碱式碳酸铜反应的方程式:
______ 。
活动一:探究制备碱式碳酸铜的条件。
【查阅资料】碱式碳酸铜是翠绿色、难溶于水的固体,酸性条件下不稳定。
【进行实验】按下表中的数据进行图示实验,记录实验结果。
(1)操作一为:

序号 | CuSO4溶液体积/mL | Na2CO3溶液体积/mL | 水浴温度/℃ | 固体颜色 |
I | 50 | 60 | 60 | 蓝绿 |
II | 50 | 60 | 70 | 翠绿 |
Ⅲ | 50 | 60 | 80 | 暗绿 |
IV | 50 | 70 | 70 | 蓝绿 |
V | 50 | 50 | x | 蓝绿 |
(2)为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH
(3)分析步骤Ⅱ、IV、V的数据可知CuSO4溶液与Na2CO3溶液最佳配比,则x为
(4)分析步骤I、Ⅱ、Ⅲ的数据,实验的最佳温度为
活动二:探究步骤Ⅲ中所得固体颜色偏暗的原因。
【查阅资料】碱式碳酸铜受热分解会生成的CuO为黑色。
【猜想与假设】固体颜色偏暗是因为实验过程中生成了CuO。
【进行实验】

(5)如图所示,锥形瓶中加入的药品为50 mL CuSO4溶液和Na2CO3溶液,水浴温度为
(6)【结论】碱式碳酸铜反应的方程式:

更新时间:2023-07-11 19:42:03
|
相似题推荐
科学探究题
|
适中
(0.65)
【推荐1】兴趣小组以“土壤酸碱性形成原因以及对植物生长的影响”为主题开展了项目式研究。
【任务一】测定土壤的酸碱度及对作物的影响
取我市3份不同地方土样,干燥后分别与自来水按2∶5的质量比混合,操作如下图所示。测得三个土样的pH分别为5.1、5.2、5.3

(1)我市的土壤呈_____ (填“酸性”“碱性”或“中性)。
(2)纱布相当于过滤器中的_____ (填实验材料名称)。请指出该实验中不够严密的操作_____ (写一点)。
(3)不同农作物生长适应pH范围如下表,其中不适合在我市种植的农作物是_____ 。
(4)模拟不同酸碱度土壤对植物生长的影响:项目小组分别在5个烧杯中倒入不同pH溶液50mL,保持其他条件一致,放入8粒大小一样的绿豆,观察记录,数据如图。由图可知,土壤pH=_____ 时,绿豆生长状况最好。

【任务二】酸性土壤形成的原因及改良
(5)长期施用一些化肥会造成土壤酸化,以 为例:
为例: ,则R的化学式是
,则R的化学式是_____ 。
(6)用适量的石灰石粉末( )改良上述土壤的原理如下图
)改良上述土壤的原理如下图

说明石灰石中的 把土壤颗粒上吸附的
把土壤颗粒上吸附的_____ (填离子符号)交换下来。
(7)假设土壤浸出液的酸只有 ,写出用石灰水中和
,写出用石灰水中和 的化学方程式
的化学方程式_____ 。取100mL该浸出液(硫酸的浓度约为0.0196%),需要_____ mL0.148%石灰水将其恰好中和(上述溶液的密度均为1.0g/mL)。
【任务一】测定土壤的酸碱度及对作物的影响
取我市3份不同地方土样,干燥后分别与自来水按2∶5的质量比混合,操作如下图所示。测得三个土样的pH分别为5.1、5.2、5.3

(1)我市的土壤呈
(2)纱布相当于过滤器中的
(3)不同农作物生长适应pH范围如下表,其中不适合在我市种植的农作物是
| 农作物名称 | 水稻 | 花生 | 大豆 | 地瓜 | 土豆 | 棉花 |
| 适应范围(pH) | 4.0-9.0 | 4.8-8.0 | 5.0-8.0 | 5.0-8.0 | 5.0-6.5 | 5.5-9.0 |

【任务二】酸性土壤形成的原因及改良
(5)长期施用一些化肥会造成土壤酸化,以
 为例:
为例: ,则R的化学式是
,则R的化学式是(6)用适量的石灰石粉末(
 )改良上述土壤的原理如下图
)改良上述土壤的原理如下图
说明石灰石中的
 把土壤颗粒上吸附的
把土壤颗粒上吸附的(7)假设土壤浸出液的酸只有
 ,写出用石灰水中和
,写出用石灰水中和 的化学方程式
的化学方程式
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】如图几种物资在新冠疫情中起到了重要的作用。

(1)一次性医用三层口罩是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到_______ (填实验操作名称)作用。
(2)84消毒液的有效成分为次氯酸钠(NaClO),其中氯元素的化合价为_____ ;工业上可用氯气(C12)和NaOH溶液反应来制取NaClO,同时生成一种重要的调味品和水,该反应的化学方程式为_____ 。
(3)某兴趣小组对84消毒液和过氧化氢消毒剂进行如下探究:
【实验1】取少量84消毒液于试管中,滴加过氧化氢消毒剂,发现大量气泡产生并能使带火星的木条复燃,说明该气泡是_______ (写化学式)。
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】猜想一:作反应物,NaClO与过氧化氢消毒剂发生化学反应;
猜想二:作_______ ,与过氧化氢分解产生氧气时起类似MnO2的作用。
【实验2】
①按图所示组装实验装置,并检查装置气密性。

②向锥形瓶中加入30mL84消毒液,注射器中吸入25mL过氧化氢溶液。
③把注射器中的过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他误差)见下表:
分析表中数据得出“猜想_______ 正确”,其依据是_______ 。
【拓展反思】
①生活中使用各种消毒剂时,要考虑它们的性质,切记“科学使用,注意安全!”下列使用消毒剂的做法正确的是_______ 。
A 消毒剂均应密封保存 B 使用84消毒液的浓度越高越好
C 不同的消毒剂可混合使用 D 使用医用酒精消毒应远离明火
②“洁厕灵”的有效成分是稀盐酸,若与“84消毒液”混用,会产生一种有毒气体,其反应的化学方程式为 ,则的化学式为
,则的化学式为_______ 。

(1)一次性医用三层口罩是由专业两层纤维无纺布和中间一层熔喷布,经超声波焊接而成,能像滤纸一样起到
(2)84消毒液的有效成分为次氯酸钠(NaClO),其中氯元素的化合价为
(3)某兴趣小组对84消毒液和过氧化氢消毒剂进行如下探究:
【实验1】取少量84消毒液于试管中,滴加过氧化氢消毒剂,发现大量气泡产生并能使带火星的木条复燃,说明该气泡是
【提出问题】在上述反应中,NaClO的作用是什么?
【作出猜想】猜想一:作反应物,NaClO与过氧化氢消毒剂发生化学反应;
猜想二:作
【实验2】
①按图所示组装实验装置,并检查装置气密性。

②向锥形瓶中加入30mL84消毒液,注射器中吸入25mL过氧化氢溶液。
③把注射器中的过氧化氢溶液平均分5次推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他误差)见下表:
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 收集气体的总体积/mL | 140 | 280 | 365 | 370 | 375 |
【拓展反思】
①生活中使用各种消毒剂时,要考虑它们的性质,切记“科学使用,注意安全!”下列使用消毒剂的做法正确的是
A 消毒剂均应密封保存 B 使用84消毒液的浓度越高越好
C 不同的消毒剂可混合使用 D 使用医用酒精消毒应远离明火
②“洁厕灵”的有效成分是稀盐酸,若与“84消毒液”混用,会产生一种有毒气体,其反应的化学方程式为
 ,则的化学式为
,则的化学式为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】戴口罩是新冠肺炎疫情常态化防控的措施之一。一次性医用口罩绒布的主要成分是聚丙烯[(C3H6)n],随意丢弃易引起白色污染。某兴趣小组尝试用焚烧法对口罩绒布进行处理,并将燃烧产物用氢氧化钠溶液吸收。
(1)聚丙烯完全燃烧的化学方程式为:2(C3H6)n+9nO2 6nCO2+6nX,X的化学式为
6nCO2+6nX,X的化学式为______ 。
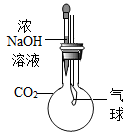
(2)为“看见”CO2与NaOH的反应,甲同学设计了如图所示的实验方案,当观察到______ 现象时,说明两者发生反应。
(3)将完全燃烧后的产物全部通入一定量的氢氧化钠溶液中,得到吸收液。乙同学对吸收液的成分产生兴趣,进行如下探究:
【提出问题】
吸收液中溶质的成分是什么?
【查阅资料】
①Na2CO3、NaHCO3的溶液均呈碱性;CaCl2溶液呈中性。
②NaOH与NaHCO3能反应。
③Na2CO3+CaCl2═CaCO3↓+2NaCl;2NaHCO3+CaCl2═CaCO3↓+2NaCl+H2O+CO2↑
【猜想假设】
猜想一:NaOH、Na2CO3
猜想二:______
猜想三:Na2CO3、NaHCO3
猜想四:NaHCO3
【实验探究】
【交流反思】
实验结束后,为了对吸收液进行无害化处理,丙同学向吸收液中加入稀盐酸至不再产生气泡为止。写出其中一个反应的化学方程式:______ 。

(1)聚丙烯完全燃烧的化学方程式为:2(C3H6)n+9nO2
 6nCO2+6nX,X的化学式为
6nCO2+6nX,X的化学式为(2)为“看见”CO2与NaOH的反应,甲同学设计了如图所示的实验方案,当观察到
(3)将完全燃烧后的产物全部通入一定量的氢氧化钠溶液中,得到吸收液。乙同学对吸收液的成分产生兴趣,进行如下探究:
【提出问题】
吸收液中溶质的成分是什么?
【查阅资料】
①Na2CO3、NaHCO3的溶液均呈碱性;CaCl2溶液呈中性。
②NaOH与NaHCO3能反应。
③Na2CO3+CaCl2═CaCO3↓+2NaCl;2NaHCO3+CaCl2═CaCO3↓+2NaCl+H2O+CO2↑
【猜想假设】
猜想一:NaOH、Na2CO3
猜想二:
猜想三:Na2CO3、NaHCO3
猜想四:NaHCO3
【实验探究】
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 取吸收液少许于试管中,滴加2~3滴无色酚酞溶液 | 溶液呈碱性 | |
| 2 | 向步骤1所得溶液中加入过量的CaCl2溶液 | 产生白色沉淀,溶液为红色 | 猜想 |
【交流反思】
实验结束后,为了对吸收液进行无害化处理,丙同学向吸收液中加入稀盐酸至不再产生气泡为止。写出其中一个反应的化学方程式:
您最近一年使用:0次
【推荐1】氢氧化钠溶液和稀盐酸混合没有明显现象,它们是否发生了反应呢?某化学兴趣小组的同学设计如图甲所示实验进行探究。他们在盛有一定量 溶液的烧杯中放置
溶液的烧杯中放置 传感器和温度传感器,然后开启电磁搅拌器,从滴定管中逐滴加入
传感器和温度传感器,然后开启电磁搅拌器,从滴定管中逐滴加入 溶液;计算机显示两种传感器所得的数据曲线如图乙和图丙。
溶液;计算机显示两种传感器所得的数据曲线如图乙和图丙。

【实验分析】
(1)写出稀盐酸和氢氧化钠溶液反应的化学方程式______ ,该反应的基本反应类型是______ 。
(2)由图乙可知,图甲滴定管中的 溶液是
溶液是______ (选填“ 溶液”或“稀盐酸”)。
溶液”或“稀盐酸”)。
(3)关于图乙、图丙的说法正确的是______(填字母)。
(4)图丁是图甲中 溶液和稀盐酸反应的微观示意图,则反应前的“●”表示的微粒是
溶液和稀盐酸反应的微观示意图,则反应前的“●”表示的微粒是______ (填微粒符号)。

【拓展迁移】
(5)将 的
的 溶液与
溶液与 的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显
的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显______ 色。
 溶液的烧杯中放置
溶液的烧杯中放置 传感器和温度传感器,然后开启电磁搅拌器,从滴定管中逐滴加入
传感器和温度传感器,然后开启电磁搅拌器,从滴定管中逐滴加入 溶液;计算机显示两种传感器所得的数据曲线如图乙和图丙。
溶液;计算机显示两种传感器所得的数据曲线如图乙和图丙。
【实验分析】
(1)写出稀盐酸和氢氧化钠溶液反应的化学方程式
(2)由图乙可知,图甲滴定管中的
 溶液是
溶液是 溶液”或“稀盐酸”)。
溶液”或“稀盐酸”)。(3)关于图乙、图丙的说法正确的是______(填字母)。
A.图乙中 点表示的溶液中 点表示的溶液中 和 和 微粒数目相同 微粒数目相同 |
B.取图丙中 点的溶液,加入碳酸钠溶液,会产生气泡 点的溶液,加入碳酸钠溶液,会产生气泡 |
C.取图乙 点的溶液,进行蒸发结晶,再将所得固体溶于水,测得溶液的 点的溶液,进行蒸发结晶,再将所得固体溶于水,测得溶液的 ,可以得出稀盐酸和 ,可以得出稀盐酸和 溶液发生了反应 溶液发生了反应 |
(4)图丁是图甲中
 溶液和稀盐酸反应的微观示意图,则反应前的“●”表示的微粒是
溶液和稀盐酸反应的微观示意图,则反应前的“●”表示的微粒是
【拓展迁移】
(5)将
 的
的 溶液与
溶液与 的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显
的稀盐酸混合,充分反应后,滴入紫色石蕊溶液显
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室有一瓶标签被腐蚀的无色溶液,是稀硫酸和氢氧化钠溶液中的一种。在老师的指导下,小红和小明用不同方法鉴定。
实验一:
小红和小明操作均无误。
【提出问题】
该溶液到底是稀硫酸还是氢氧化钠溶液?
【查阅资料】
铝、氧化铝既能与酸反应,又可与强碱溶液反应,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,氧化铝与氢氧化钠溶液反应生成偏铝酸钠( NaAlO2)和一种氧化物。NaAlO2易溶于水,其水溶液呈碱性,NaAlO2与铝、氧化铝均不反应。
【分析实验得出结论】该溶液为_____ 溶液。
【交流反思】实验一中,小红所做实验开始无明显现象的原因是_____ (用化学方程式表示)。
【拓展应用】有一种管道疏通剂,主要成分为铝粉和氢氧化钠粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对油脂和毛发等淤积物的腐蚀,同时产生氢气增加管道内气压,利于疏通。
实验二:小明用如图所示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明从左端管口加入管道疏通剂,并用胶塞堵住弯管左端上口,可能出现的现象为_____ (填字母序号)。

A 产生大量气体
B 弯管内温度升高
C 堵塞物变软被气体赶出,落入烧杯中
实验一:
| 实验步骤 | 实验现象 | 实验结论 |
| 小红取少量该溶液于试管中,向其中插入没有打磨的铝片 | 开始无明显现象,后产生 | 小红认为该溶液为稀硫酸 |
| 小明用pH试纸测定其pH | pH=13 | 小明认为该溶液为氢氧化钠溶液 |
【提出问题】
该溶液到底是稀硫酸还是氢氧化钠溶液?
【查阅资料】
铝、氧化铝既能与酸反应,又可与强碱溶液反应,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,氧化铝与氢氧化钠溶液反应生成偏铝酸钠( NaAlO2)和一种氧化物。NaAlO2易溶于水,其水溶液呈碱性,NaAlO2与铝、氧化铝均不反应。
【分析实验得出结论】该溶液为
【交流反思】实验一中,小红所做实验开始无明显现象的原因是
【拓展应用】有一种管道疏通剂,主要成分为铝粉和氢氧化钠粉末。工作原理是:利用铝和氢氧化钠遇水反应放出大量的热,加快氢氧化钠对油脂和毛发等淤积物的腐蚀,同时产生氢气增加管道内气压,利于疏通。
实验二:小明用如图所示的玻璃弯管模拟家庭下水道,并用动物脂肪和毛发堵在弯管处,他按照使用说明从左端管口加入管道疏通剂,并用胶塞堵住弯管左端上口,可能出现的现象为

A 产生大量气体
B 弯管内温度升高
C 堵塞物变软被气体赶出,落入烧杯中
您最近一年使用:0次
科学探究题
|
适中
(0.65)
【推荐3】在学习了常见的酸和碱后,某化学兴趣小组的同学围绕“酸碱中和反应”,在老师引导下开展实验探究活动,请你参与下列活动。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。

(1)测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将___________ (填字母序号)。
a.氢氧化钾溶液滴入稀硫酸中
b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化
乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是___________ (填“放热”或“吸热”)反应。图2中B点表示的含义是___________ 。
(3)借助于酸碱指示剂
丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为___________ 。
【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。
【猜想与假设】
(4)猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有___________ ;
【进行实验】
(5)为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(6)丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是___________ 。
(7)同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用下列的某些物质代替,也能得到同样的实验结论,请你选出可用药品的字母序号___________。
【实验探究】将氢氧化钾溶液与稀硫酸混合,观察不到明显现象,为证明氢氧化钾溶液与稀硫酸发生了反应,三位同学进行了以下实验。

(1)测定溶液pH变化的方法
甲同学在实验过程中测得pH变化如图1所示,则该同学是将
a.氢氧化钾溶液滴入稀硫酸中
b.稀硫酸滴入氢氧化钾溶液中
(2)测混合过程中的温度变化
乙同学在实验过程中测得反应混合溶液的温度变化如图2所示,说明稀硫酸与氢氧化钾溶液发生的反应是
(3)借助于酸碱指示剂
丙同学通过图3所示实验,他观察到溶液由红色变成无色,也证明氢氧化钾溶液与稀硫酸发生了化学反应,反应的化学方程式为
【提出问题】针对反应后溶液中溶质的成分,大家纷纷提出了猜想。
【猜想与假设】
(4)猜想一:只有K2SO4;猜想二:有K2SO4和H2SO4;猜想三:有
【进行实验】
(5)为了验证猜想,学习小组选用Fe2O3粉末、BaCl2溶液,进行如下探究:
| 实验方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 取少量反应后的溶液于试管 中,加入Fe2O3粉末 | 溶液中有H2SO4,猜想二正确 | |
| 方案二 | 取少量反应后的溶液于试管中,滴加BaCl2溶液 | ②产生白色沉淀 | 溶液中有H2SO4,猜想二正确 |
【实验结论】通过探究,同学们一致确定猜想二是正确的。
【评价与反思】
(6)丁同学针对上述方案提出疑问,认为方案二是不合理的,理由是
(7)同学们经过反思与讨论,最后认为方案一中的Fe2O3粉末可以用下列的某些物质代替,也能得到同样的实验结论,请你选出可用药品的字母序号___________。
| A.Mg | B.CuO | C.KCl | D.Na2CO3 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】柠檬的果皮、籽、果肉中均含有大量的柚皮苷(C27H32O14)和柠檬苦素类似物等苦味物质,在榨汁过程中常出现苦味,为了寻求去除苦味的方法,化学小组进行了实验,探究树脂添加量、脱苦时间、温度对其脱苦率的影响。
资料:柠檬的不同部位中,柠檬籽中柚皮苷的含量最高,果皮次之,再次是果肉。
【进行实验】
实验一:室温下,分别取20 mL鲜榨柠檬汁进行实验,探究树脂添加量、脱苦时间与脱苦率的关系。记录如下:
实验二:分别在20 mL鲜榨柠檬汁中加入一定质量的树脂,脱苦时间相同,探究温度与脱苦率的关系。记录如下:
【解释与结论】
(1)实验一中①②③的目的是_________ 。
(2)实验一由②④⑤可以得到的结论是_________ 。
(3)实验一①中,若将脱苦时间改为10min,则脱苦率_________ (填“>”或“<”)20.4%。
(4)实验二中探究温度与脱苦率的关系,可选做的实验是_________ (任选一组,填实验序号) 。
(5)下列说法正确的是 (填序号)。
【反思与评价】
(6)小组同学查阅资料发现,添加柚苷酶也可降低柠檬汁的苦味,设计实验比较在柠檬汁中添加树脂与添加柚苷酶的脱苦效果:室温下,分别取20 mL鲜榨柠檬汁于两个烧杯中,_________ ,取样测量柠檬汁的脱苦率。
资料:柠檬的不同部位中,柠檬籽中柚皮苷的含量最高,果皮次之,再次是果肉。
【进行实验】
实验一:室温下,分别取20 mL鲜榨柠檬汁进行实验,探究树脂添加量、脱苦时间与脱苦率的关系。记录如下:
| 序号 | 树脂添加量/g | 脱苦时间/min | 脱苦率(%) |
| ① | 0.04 | 20 | 20.4 |
| ② | 0.04 | 25 | 28.5 |
| ③ | 0.04 | 30 | 36.8 |
| ④ | 0.06 | 25 | 30.1 |
| ⑤ | 0.08 | 25 | 34.7 |
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
| 树脂添加量/g | 0.04 | 0.06 | 0.08 | 0.04 | 0.06 | 0.08 | 0.04 | 0.06 | 0.08 |
| 温度/℃ | 20 | 20 | 20 | 30 | 30 | 30 | 40 | 40 | 40 |
| 脱苦率(%) | 22.4 | 39.2 | 48.7 | 23.7 | 44.7 | 49.6 | 22.5 | 42.1 | 49.0 |
(1)实验一中①②③的目的是
(2)实验一由②④⑤可以得到的结论是
(3)实验一①中,若将脱苦时间改为10min,则脱苦率
(4)实验二中探究温度与脱苦率的关系,可选做的实验是
(5)下列说法正确的是 (填序号)。
| A.当加入树脂质量和脱苦时间相同时,脱苦温度越高,脱苦效果越好 |
| B.根据以上实验数据分析,当树脂添加量为0.08g时柠檬汁脱苦效果最好 |
| C.用柠檬鲜果榨汁时,可以采用去皮、去籽的方法减少柠檬汁的苦味 |
【反思与评价】
(6)小组同学查阅资料发现,添加柚苷酶也可降低柠檬汁的苦味,设计实验比较在柠檬汁中添加树脂与添加柚苷酶的脱苦效果:室温下,分别取20 mL鲜榨柠檬汁于两个烧杯中,
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某品牌“贴身暖宝宝”袋内主要成分:铁粉、水、活性炭、食盐等,化学兴趣小组围绕这些成分展开探究。
【活动一】探究袋内是否含有铁粉?
【进行实验】①取出袋内粉末于滤纸上,与磁铁充分接触。②将少量磁铁吸出的粉末加入足量稀硫酸中。
【收集证据】
(1)磁铁吸出的粉末与稀硫酸剧烈反应得到浅绿色溶液,同时_______ 。
【得出结论】袋内含有铁粉。
【做出猜想】被磁铁吸出的铁粉能在空气中燃烧。
【获取事实】将少许铁粉撒在酒精灯火焰上,铁粉立即剧烈燃烧、火星四射。
【反思交流】
(2)铁粉燃烧反应的化学方程式为_______ 。铁丝不能而铁粉能在空气中燃烧的原因是_______ 。
【活动二】暖宝宝中食盐和活性炭的作用是什么?
【进行实验】在盛有干燥空气的锥形瓶中分别放入①~④组物质,用温度传感器分别测量相同时间内的温度变化,装置如图1所示,传感器测得的相应数据如图2。
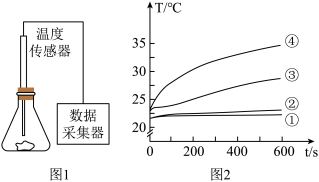
【解释与结论】
(3)④中x为_______ 。
(4)依据实验_______ (填序号)可得出“活性炭能加快反应速率”的结论。
(5)欲探究“活性炭用量对反应的影响”,应再设计1个实验:_______ 。
【活动三】测定“暖宝宝”中的含铁量
取一片包装完好的“暖宝宝”,取样品mg利用如图3所示装置与药品,测反应后生成气体的体积。将“暖宝宝”样品装入烧瓶中。打开分液漏斗活塞,加入稀硫酸至不再有气泡冒出。待恢复至室温,测得注射器活塞向右移动vmL(忽略稀硫酸占有的体积)。
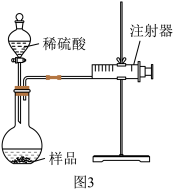
(6)若实验条件下,氢气的密度为dg/mL。则该“暖宝宝”中铁粉的质量分数的表达式为_______ 。(用含d、v、m的字母表示)
(7)利用图3装置,测量结果偏小,原因是_______ 、_______ (写两点即可)。
【活动一】探究袋内是否含有铁粉?
【进行实验】①取出袋内粉末于滤纸上,与磁铁充分接触。②将少量磁铁吸出的粉末加入足量稀硫酸中。
【收集证据】
(1)磁铁吸出的粉末与稀硫酸剧烈反应得到浅绿色溶液,同时
【得出结论】袋内含有铁粉。
【做出猜想】被磁铁吸出的铁粉能在空气中燃烧。
【获取事实】将少许铁粉撒在酒精灯火焰上,铁粉立即剧烈燃烧、火星四射。
【反思交流】
(2)铁粉燃烧反应的化学方程式为
【活动二】暖宝宝中食盐和活性炭的作用是什么?
【进行实验】在盛有干燥空气的锥形瓶中分别放入①~④组物质,用温度传感器分别测量相同时间内的温度变化,装置如图1所示,传感器测得的相应数据如图2。
| 物质序号 | 铁粉/g | 水/mL | 氯化钠/g | 活性炭/g |
| ① | 9 | 6 | 0 | 0 |
| ② | 9 | 6 | 3 | 0 |
| ③ | 9 | 6 | 0 | 6 |
| ④ | x | 6 | 3 | 6 |

【解释与结论】
(3)④中x为
(4)依据实验
(5)欲探究“活性炭用量对反应的影响”,应再设计1个实验:
【活动三】测定“暖宝宝”中的含铁量
取一片包装完好的“暖宝宝”,取样品mg利用如图3所示装置与药品,测反应后生成气体的体积。将“暖宝宝”样品装入烧瓶中。打开分液漏斗活塞,加入稀硫酸至不再有气泡冒出。待恢复至室温,测得注射器活塞向右移动vmL(忽略稀硫酸占有的体积)。

(6)若实验条件下,氢气的密度为dg/mL。则该“暖宝宝”中铁粉的质量分数的表达式为
(7)利用图3装置,测量结果偏小,原因是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在做氧化铜与木炭反应的实验时,往往会发现反应后试管中仍有黑色固体。小明对此进行了探究,并邀请你一起参与。
请写出反应的化学方程式_________________ 。
【提出问题】氧化铜与木炭充分反应结束后,试管中的黑色固体是什么?
【猜想或假设】可能是①木炭;②_______________ ;③____________________ 。
【查阅资料】铜、木炭都不与稀硫酸反应,而氧化铜能与稀硫酸反应形成蓝色溶液
【实验与结论】请设计实验验证小明的猜想
【实验反思】科学探究的方法有多种,请你再设计两种方法来证明小明的猜想。
方案一:_______________________ 。
方案二:____________________ 。
请写出反应的化学方程式
【提出问题】氧化铜与木炭充分反应结束后,试管中的黑色固体是什么?
【猜想或假设】可能是①木炭;②
【查阅资料】铜、木炭都不与稀硫酸反应,而氧化铜能与稀硫酸反应形成蓝色溶液
【实验与结论】请设计实验验证小明的猜想
| 实验步骤 | 实验现象 | 实验结论 |
【实验反思】科学探究的方法有多种,请你再设计两种方法来证明小明的猜想。
方案一:
方案二:
您最近一年使用:0次
【推荐1】某化学兴趣小组用图所示的实验装置,探究影响过氧化氢分解速率的因素。

(1)装置中使用注射器的优点是___________________ , 锥形瓶中反应的化学方程式为__________________ 。
(2)下面是用上述装置实验时,收集的相关数据:
(3)从实验①和②对比可知,化学反应速率与__________________ 有关;从实验__________________ 对比可知,化学反应速率与是否加MnO2有关。表格中的待测数据那一栏应该是___________________ 。
(4)发现问题:实验温度最难控制,反应一段时间后溶液的温度总是比起始温度高,说明反应__________________ (填“放出”或“吸收”)热量
(5)继续探究:除了该实验小组探究过的因素以外,你若还有其他影响反应速率的因素及探究方法,请写在下面_________________ 。

(1)装置中使用注射器的优点是
(2)下面是用上述装置实验时,收集的相关数据:
| 实验序号 | H2O2溶液浓度% | 体积ml | MnO2的量/g | 温度/°C | 待测数据 | 反应所需的时间/s |
| ① | 5 | 2 | 0.1 | 20 | 18 | |
| ② | 10 | 2 | 0.1 | 20 | 6 | |
| ③ | 5 | 2 | / | 20 | 64 | |
| ④ | 5 | 2 | / | 60 | 25 |
(3)从实验①和②对比可知,化学反应速率与
(4)发现问题:实验温度最难控制,反应一段时间后溶液的温度总是比起始温度高,说明反应
(5)继续探究:除了该实验小组探究过的因素以外,你若还有其他影响反应速率的因素及探究方法,请写在下面
您最近一年使用:0次
科学探究题
|
适中
(0.65)
真题
解题方法
【推荐2】科学探究
维生素C广泛存在于新鲜的果蔬中,对人体健康有多种益处。人体不能合成维生素C,需要从食物中获得。哪些果蔬维生素C含量较高?某兴趣小组选取猕猴桃、梨、紫甘蓝和黄瓜探究其维生素C含量高低。
【实验原理】维生素C能使酸性高锰酸钾溶液褪色。
(1)维生素C越多,消耗的高锰酸钾越______ (填“多”或“少”);
【实验方案】步骤一:配制0.02%酸性高锰酸钾溶液
(2)配制溶液时,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、试剂瓶和_____ 。
步骤二:制作新鲜果蔬汁
分别取等质量的猕猴桃、梨、紫甘蓝、黄瓜(可食用部分),切碎,加入等体积的水(果蔬中可食用部分和水的质量比均为 ),分别放入榨汁机榨出四种果蔬汁,用纱布过滤,滤液放入滴瓶备用。
),分别放入榨汁机榨出四种果蔬汁,用纱布过滤,滤液放入滴瓶备用。
步骤三:果蔬汁与0.02%酸性高锰酸钾溶液反应
(3)______ (填操作和现象),记录滴加新鲜果蔬汁滴数,重复实验2~3次。
【数据记录】
【实验结论】
(4)_______ 。
【反思与评价】查阅《食物营养成分速查表》数据,与本实验结果基本一致,但还存在一定偏差。
(5)从实验操作角度分析,下列操作可能引起误差的是_______ 。
a.制作果蔬汁时,用到的水未煮沸并迅速冷却
b.滴加果蔬汁时速度过快,没有及时振荡试管
c.滴加果蔬汁时液体滴在试管外面
从原理角度分析,果蔬是混合物,果蔬中除维生素C外,其他成分也可能使酸性高锰酸钾溶液褪色。另外,提供的四种果蔬新鲜程度也不一样等。严谨求实、质疑审辩的科学态度让本次实验找到新的探究起点。
【生活应用】
(6)结合维生素C性质分析,果蔬怎么吃能减少维生素C的流失______ (写一条即可)。
维生素C广泛存在于新鲜的果蔬中,对人体健康有多种益处。人体不能合成维生素C,需要从食物中获得。哪些果蔬维生素C含量较高?某兴趣小组选取猕猴桃、梨、紫甘蓝和黄瓜探究其维生素C含量高低。
| 资料卡片: 维生素  ,易溶于水,受热易分解;易被氧化,能使紫红色酸性高锰酸钾溶液褪色。 ,易溶于水,受热易分解;易被氧化,能使紫红色酸性高锰酸钾溶液褪色。 |
(1)维生素C越多,消耗的高锰酸钾越
【实验方案】步骤一:配制0.02%酸性高锰酸钾溶液
(2)配制溶液时,需要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、试剂瓶和
步骤二:制作新鲜果蔬汁
分别取等质量的猕猴桃、梨、紫甘蓝、黄瓜(可食用部分),切碎,加入等体积的水(果蔬中可食用部分和水的质量比均为
 ),分别放入榨汁机榨出四种果蔬汁,用纱布过滤,滤液放入滴瓶备用。
),分别放入榨汁机榨出四种果蔬汁,用纱布过滤,滤液放入滴瓶备用。步骤三:果蔬汁与0.02%酸性高锰酸钾溶液反应
(3)
【数据记录】
| 果蔬种类 | 猕猴桃汁 | 梨汁 | 紫甘蓝汁 | 黄瓜汁 | ||||||||
| 滴数/滴 | 11 | 13 | 12 | 31 | 35 | 33 | 20 | 20 | 20 | 25 | 27 | 26 |
| 平均滴数 | 12 | 33 | 20 | 26 | ||||||||
(4)
【反思与评价】查阅《食物营养成分速查表》数据,与本实验结果基本一致,但还存在一定偏差。
(5)从实验操作角度分析,下列操作可能引起误差的是
a.制作果蔬汁时,用到的水未煮沸并迅速冷却
b.滴加果蔬汁时速度过快,没有及时振荡试管
c.滴加果蔬汁时液体滴在试管外面
从原理角度分析,果蔬是混合物,果蔬中除维生素C外,其他成分也可能使酸性高锰酸钾溶液褪色。另外,提供的四种果蔬新鲜程度也不一样等。严谨求实、质疑审辩的科学态度让本次实验找到新的探究起点。
【生活应用】
(6)结合维生素C性质分析,果蔬怎么吃能减少维生素C的流失
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】酒精和含氯消毒液在抗击新冠肺炎疫情中发挥了重要作用。请回答下列问题:
Ⅰ.(1)体积分数为75%的酒精可直接用于消毒,酒精属于___________ 。(填“无机物”或“有机物”)
(2)大面积喷洒酒精易引起燃爆,这是因为酒精具有挥发性和___________ 性,故应小面积擦拭消毒。
Ⅱ.84消毒液是我国科研人员于1984年研制的一种含氯消毒液。某品牌84消毒液的使用说明如图,石榴化学兴趣小组对如何科学使用84消毒液进行了探究。

【查阅资料】
①84消毒液的主要成分是次氯酸钠(NaClO)。
②次氯酸(HClO)的漂白、消毒效果都强于次氯酸钠,但前者不稳定,保存和运输不方便。
(3)【探究1】小吴将少量84消毒液滴在pH试纸上,发现pH试纸先变蓝后褪色,说明84消毒液显___________ 性,并有漂白性。
(4)【探究2】根据“使用说明2”小娟猜测,在浸泡过程中,次氯酸钠与空气中的某种物质发生了反应。为了证实这一猜测,小蓝进行了以下实验:
胡老师提示,烧杯3中发生了化学反应,生成碳酸氢钠和一种漂白、消毒效果更强的物质。写出该反应的化学方程式___________ ,所以使用84消毒液时,浸泡30分钟效果更好。
(5)【拓展探究】漂白粉的漂白、消毒原理与84消毒液相似。已知漂白粉可溶于水,有效成分是次氯酸钙,保存不当易转化为碳酸钙而失效。请你设计一个简单的实验,判断漂白粉是否变质:(可供选择的试剂有:蒸馏水、稀盐酸、稀硫酸、氢氧化钠溶液)
实验步骤:___________ ;
实验现象:___________ ;
实验结论:___________ 。
Ⅰ.(1)体积分数为75%的酒精可直接用于消毒,酒精属于
(2)大面积喷洒酒精易引起燃爆,这是因为酒精具有挥发性和
Ⅱ.84消毒液是我国科研人员于1984年研制的一种含氯消毒液。某品牌84消毒液的使用说明如图,石榴化学兴趣小组对如何科学使用84消毒液进行了探究。

【查阅资料】
①84消毒液的主要成分是次氯酸钠(NaClO)。
②次氯酸(HClO)的漂白、消毒效果都强于次氯酸钠,但前者不稳定,保存和运输不方便。
(3)【探究1】小吴将少量84消毒液滴在pH试纸上,发现pH试纸先变蓝后褪色,说明84消毒液显
(4)【探究2】根据“使用说明2”小娟猜测,在浸泡过程中,次氯酸钠与空气中的某种物质发生了反应。为了证实这一猜测,小蓝进行了以下实验:
| 操作 | 现象 | |
| 将一块有色布条分成3等份,放入三个装有同浓度同体积的84消毒液的烧杯中 | 向烧杯1通入O2 | 布条褪色较慢 |
| 向烧杯2通入N2 | 布条褪色较慢 | |
| 向烧杯3通入 | 布条迅速褪色 | |
胡老师提示,烧杯3中发生了化学反应,生成碳酸氢钠和一种漂白、消毒效果更强的物质。写出该反应的化学方程式
(5)【拓展探究】漂白粉的漂白、消毒原理与84消毒液相似。已知漂白粉可溶于水,有效成分是次氯酸钙,保存不当易转化为碳酸钙而失效。请你设计一个简单的实验,判断漂白粉是否变质:(可供选择的试剂有:蒸馏水、稀盐酸、稀硫酸、氢氧化钠溶液)
实验步骤:
实验现象:
实验结论:
您最近一年使用:0次



