黄铜是铜和锌的合金。为了测定某黄铜样品中铜的质量分数,取20克该黄铜样品粉末加入到200克的稀硫酸中,恰好完全反应后,测得剩余物的总质量为219.8克,试求:
(1)产生氢气的质量(写出计算过程,下同);
(2)该黄铜样品中铜的质量分数。
(1)产生氢气的质量(写出计算过程,下同);
(2)该黄铜样品中铜的质量分数。
22-23九年级下·江苏泰州·阶段练习 查看更多[2]
江苏省泰州市姜堰区南苑学校2022-2023学年九年级下学期第二次月考化学试题(已下线)第五单元 课题3 利用化学方程式的简单计算-【巅峰课堂】2023-2024学年九年级化学上册同步精品讲+练(人教版)
更新时间:2023-07-08 16:09:53
|
相似题推荐
计算题
|
困难
(0.15)
【推荐1】钢铁工业是一个国家的支柱产业之一。炼铁的主要化学方程式为: 。
。
(1)现有200t含氧化铁80%的赤铁矿石:
①这些矿石中含氧化铁的质量为_________t;
②若用这些矿石炼铁,理论上可炼出含铁96%的生铁多少t?(写出计算过程,计算结果精确到0.1)
(2)查阅资料得知:CO与Fe2O3在不同条件下反应生成铁的同时,也能生成一些FeO或Fe3O4。某实验室用CO和Fe2O3在密闭容器中隔绝空气加强热来测试某温度下的反应结果,假如某次测试实验前后收集到的数据如下表,请回答相关问题:
①表中a的值为_____________;M的化学式为__________;
②容器内发生反应的化学方程式可表示为:_______________。
 。
。(1)现有200t含氧化铁80%的赤铁矿石:
①这些矿石中含氧化铁的质量为_________t;
②若用这些矿石炼铁,理论上可炼出含铁96%的生铁多少t?(写出计算过程,计算结果精确到0.1)
(2)查阅资料得知:CO与Fe2O3在不同条件下反应生成铁的同时,也能生成一些FeO或Fe3O4。某实验室用CO和Fe2O3在密闭容器中隔绝空气加强热来测试某温度下的反应结果,假如某次测试实验前后收集到的数据如下表,请回答相关问题:
| 物质 | CO | Fe2O3 | Fe | M | CO2 |
| 反应前质量/g | 5.6 | 32 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.6 | a | 8.8 |
①表中a的值为_____________;M的化学式为__________;
②容器内发生反应的化学方程式可表示为:_______________。
您最近一年使用:0次
计算题
|
困难
(0.15)
【推荐2】实验室有一瓶纯碱(Na2CO3)固体中混有少量烧碱(NaOH),现在需要测出这瓶药品中烧碱的含量,便取固体药品12g置于含水100g烧杯中,搅拌至完全溶解,并滴加几滴酚酞试液,溶液呈红色;再滴加稀盐酸,当用去稀盐酸100g时,溶液恰好变成无色。 反应前后质量关系如表:
请回答:
(1)整个反应生成气体_______g
(2)原固体样品中含纯碱(Na2CO3)_____________g
(3)计算出使用的稀盐酸的溶质质量分数。
| 反应前 | 反应后 | ||
| 固体样品 | 水 | 稀盐酸 | 剩余液体 |
| 12g | 100g | 100g | 207.6g |
请回答:
(1)整个反应生成气体_______g
(2)原固体样品中含纯碱(Na2CO3)_____________g
(3)计算出使用的稀盐酸的溶质质量分数。
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐3】铜锌合金外观似金子,化学小组为检测其中锌的质量分数,按下列流程进行探究实验,充分反应,所得数据如图所示(忽略盐酸的挥发):

请回答下列问题:
(1)题中实验流程能称量出气体的质量,依据的化学原理是____________ ;
(2)某同学设计如下图,通过测量气体的体积,根据测得生成气体的体积计算出气体的质量。图中虚线框内有一种测量体积的仪器(未画出),该仪器是______ ;
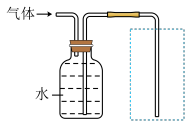
(3)结合实验方法和选择的装置分析,可能会造成实验结果不准确的原因是____________ ;
(4)列式计算合金中锌的质量分数。

请回答下列问题:
(1)题中实验流程能称量出气体的质量,依据的化学原理是
(2)某同学设计如下图,通过测量气体的体积,根据测得生成气体的体积计算出气体的质量。图中虚线框内有一种测量体积的仪器(未画出),该仪器是

(3)结合实验方法和选择的装置分析,可能会造成实验结果不准确的原因是
(4)列式计算合金中锌的质量分数。
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
解题方法
【推荐1】为了探究石灰石的纯度(假设样品中的杂质既不溶于水也不与盐酸反应),称取40g石灰石样品等分为4份(分别编号为①、②、③、④),每份样品分别与一定量的稀盐酸反应,所得数据如表所示:
然后,为了探究石灰石与稀盐酸反应后所得溶液中的溶质成分,将编号③所得溶液过滤,取滤液质量的 于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
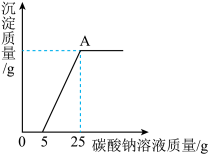
分析题中有关信息和图表,回答下列问题:
(1)该石灰石样品的纯度为 。
(2)编号③所用稀盐酸的质量m为 g。
(3)A点处对应的溶液中溶质的质量分数是多少?(写出计算过程)
| 样品编号 | ① | ② | ③ | ④ |
| 稀盐酸的质量 | 25g | 50g | m(80<m<150) | 150g |
| 剩余固体的质量 | 7.5g | 5g | 2g | 2g |
 于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
于烧杯中,向其中滴加质量分数为10.6%的碳酸钠溶液使其充分反应直至过量,有关的变化如图所示:
分析题中有关信息和图表,回答下列问题:
(1)该石灰石样品的纯度为 。
(2)编号③所用稀盐酸的质量m为 g。
(3)A点处对应的溶液中溶质的质量分数是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
解题方法
【推荐2】某化工厂生产的纯碱产品中常含有少量氯化钠。在探究质量守恒定律的实验中,甲乙两个小组分别取样品,向其中加入一定量的稀盐酸,研究反应前后质量是否改变。具体数据如下,回答下列问题:
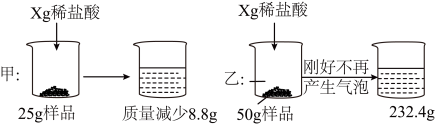
(1)写出发生反应的化学方程式______。
(2)列出甲组同学样品中参加反应的物质质量(X)的比例式______。
(3)两个小组所用盐酸样品中Xg的具体数值为_____。
(4)计算出样品中碳酸钠的质量分数_____。
(5)要把乙组所得溶液配制成16%的氯化钠溶液选种,需要_____水。
(6)若工厂要生成5t上述纯碱,理论上需要氯化钠的质量为______t。

(1)写出发生反应的化学方程式______。
(2)列出甲组同学样品中参加反应的物质质量(X)的比例式______。
(3)两个小组所用盐酸样品中Xg的具体数值为_____。
(4)计算出样品中碳酸钠的质量分数_____。
(5)要把乙组所得溶液配制成16%的氯化钠溶液选种,需要_____水。
(6)若工厂要生成5t上述纯碱,理论上需要氯化钠的质量为______t。
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
【推荐3】实验室有一瓶硫酸铵(含杂质氯化镁)样品。化学兴趣小组的同学为了测定该样品中氯化镁的含量,取该样品17.95g全部溶于152.35g水中,向所得溶液中滴加溶质质量分数为10%的氢氧化钠溶液,实验数据如表所示:
求:
(1)表中m的值为___________。
(2)该样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%)。
(3)当恰好完全反应时所得溶液中硫酸钠的质量分数(写出计算过程)。
| 时间/s | 30 | 60 | 90 | 120 | 150 |
| 产生沉淀的质量/g | 0.725 | m | 2.175 | 2.9 | 2.9 |
求:
(1)表中m的值为___________。
(2)该样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%)。
(3)当恰好完全反应时所得溶液中硫酸钠的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
解题方法
【推荐1】在托盘天平的两盘上各放一只等质量的烧杯,在两只烧杯里分别加入 50 g 溶质质量分数为 14.6%的稀盐酸。将天平调节平衡后,向左盘烧杯中投入一定量的碳酸钠固体,恰好完全 反应;向右盘烧杯中投入 6.4 g 金属镁的样品(样品有杂质且杂质不含镁元素,不与稀盐酸反应), 充分反应后天平再次平衡,则该金属镁样品中镁的质量分数 ω 的取值范围为______ 。
您最近一年使用:0次
计算题
|
困难
(0.15)
【推荐2】为测定金属锌和硫酸锌的固体混合物中锌元素 的质量分数,先称取混合物20g,放入一个干净的烧杯中,然后取一定溶质质量分数的稀硫酸75g,平均分成五次加入其中,充分振荡,实验数据表:
(1)上表中x=_____________ 。
(2)求金属锌和硫酸锌的固体混合物中,锌元素的质量分数(写出计算过程,结果精确到0.1%)。
(3)请在答题卷的图像中,请画出产生的氢气的质量与加入稀硫酸质量的变化图。

| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀硫酸的质量/g | 15 | 15 | 15 | 15 | 15 |
| 生成氢气的总质量/g | 0.12 | x | 0.36 | 0.4 | 0.4 |
(2)求金属锌和硫酸锌的固体混合物中,锌元素的质量分数(写出计算过程,结果精确到0.1%)。
(3)请在答题卷的图像中,请画出产生的氢气的质量与加入稀硫酸质量的变化图。

您最近一年使用:0次



