(1)城市家用燃料是天然气,天然气主要成分完全燃烧的化学方程式为
(2)质量相等的四种物质:①H2,②CH4,③CO,④C2H5OH完全燃烧,消耗氧气的质量由大到小的顺序为
更新时间:2023-08-28 10:00:39
|
相似题推荐
填空与简答-简答题
|
困难
(0.15)
解题方法
【推荐1】比较与分析归纳会使你变得更聪明。请分析下表中信息,回答有关问题:
⑴上述表中X=
⑵ ① 试归纳氟、氯、溴、碘的原子结构规律(答一点即可):
;
② 试归纳氟、氯、溴、碘对应单质的性质变化规律(答一点即可):
;
⑶已知:Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的反应方程式为:HClO+NaOH=NaClO+H2O,试分别写出Br2与水,Br2与NaOH溶液反应的化学方程式:
;
。
| 名称 | 符号 | 原子结构示意图 | 单质的 化学式 | 常温常压下 状态 | 单质与氢气反应 |
| 氟 | F | 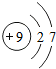 | F2 | 气态 | 黑暗处爆炸 |
| 氯 | Cl | 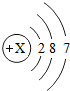 | Cl2 | 气态 | 光照爆炸 |
| 溴 | Br | 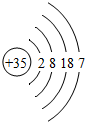 | Br2 | 液态 | 加热反应 |
| 碘 | I | 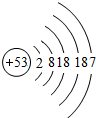 | I2 | 固态 | 持续加热缓慢反应 |
⑵ ① 试归纳氟、氯、溴、碘的原子结构规律(答一点即可):
;
② 试归纳氟、氯、溴、碘对应单质的性质变化规律(答一点即可):
;
⑶已知:Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的反应方程式为:HClO+NaOH=NaClO+H2O,试分别写出Br2与水,Br2与NaOH溶液反应的化学方程式:
;
。
您最近一年使用:0次
填空与简答-简答题
|
困难
(0.15)
【推荐2】铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2·12H2O]的工艺流程如图所示:(已知氢氧化铝能溶解在氢氧化钠溶液中,生成偏铝酸钠NaAlO2)
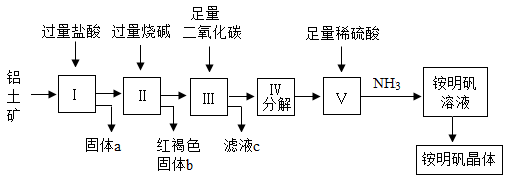
请回答下列问题:
(1)固体a的化学式为_____ ,Ⅲ中通入足量CO2气体能生成氢氧化铝和一种酸式盐。写出发生反应的化学方程式为_____ 。
(2)IV步分解指加热使氢氧化铝分解为相应的氧化物。由V制取铵明矾溶液的化学方程式为_____ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_____ 、冷却结晶、过滤洗涤。
(3)以1000kg含氧化铝30.6%的铝土矿为原料制取Al2(SO4)3,需消耗含溶质质量为_____ g的98%的浓硫酸(密度1.84g·cm-1)。
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的“微粒”个数之比为1:1,则投料时铝土矿中的AI2O3和H2SO4的“微粒”个数之比为_____ 。

请回答下列问题:
(1)固体a的化学式为
(2)IV步分解指加热使氢氧化铝分解为相应的氧化物。由V制取铵明矾溶液的化学方程式为
(3)以1000kg含氧化铝30.6%的铝土矿为原料制取Al2(SO4)3,需消耗含溶质质量为
(4)若同时制取铵明矾和硫酸铝,通过控制硫酸的用量调节两种产品的产量。若欲使制得的铵明矾和硫酸铝的“微粒”个数之比为1:1,则投料时铝土矿中的AI2O3和H2SO4的“微粒”个数之比为
您最近一年使用:0次
填空与简答-流程题
|
困难
(0.15)
解题方法
【推荐3】实验室以二氧化铈(CeO2)废渣为原料制备Cl-含量少的 ,其部分实验过程如下:
,其部分实验过程如下:

(1)“酸浸”时CeO2与 反应生成Ce3+并放出O2,该反应的离子方程式为
反应生成Ce3+并放出O2,该反应的离子方程式为________ 。
(2)pH约为7的CeCl3溶液与 溶液反应可生成
溶液反应可生成 沉淀,该沉淀中
沉淀,该沉淀中 含量与加料方式有关。得到含
含量与加料方式有关。得到含 量较少的
量较少的 的加料方式为______(填序号)。
的加料方式为______(填序号)。
(3)通过中和、萃取、反萃取CeCl3、沉淀等过程,可制备Cl-含量少的Ce2(CO3)3。已知Ce3+能被有机萃取剂(简称HA)萃取,其萃取原理可表示为 (有机层)+
(有机层)+ (水层)
(水层)
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是________ 。
②反萃取的目的是将有机层Ce3+转移到水层。使Ce3+尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有_______ (填两项)。
③与“反萃取”得到的水溶液比较,过滤Ce2(CO3)3溶液的滤液中,物质的量减小的离子有_______ (填化学式)。
(4)实验中需要测定溶液中Ce3+的含量。已知水溶液中Ce4+可用准确浓度的 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:
。请补充完整实验方案:

①准确量取 溶液[
溶液[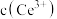 约为
约为 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;
容量瓶中后定容;
②按规定操作分别将 和待测Ce4+溶液装入如图所示的滴定管中;③
和待测Ce4+溶液装入如图所示的滴定管中;③_________ 。
 ,其部分实验过程如下:
,其部分实验过程如下:
(1)“酸浸”时CeO2与
 反应生成Ce3+并放出O2,该反应的离子方程式为
反应生成Ce3+并放出O2,该反应的离子方程式为(2)pH约为7的CeCl3溶液与
 溶液反应可生成
溶液反应可生成 沉淀,该沉淀中
沉淀,该沉淀中 含量与加料方式有关。得到含
含量与加料方式有关。得到含 量较少的
量较少的 的加料方式为______(填序号)。
的加料方式为______(填序号)。| A.将NH4HCO3溶液滴加到溶液中 |
| B.将CeCl3溶液滴加到NH4HCO3溶液中 |
 (有机层)+
(有机层)+ (水层)
(水层)①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是
②反萃取的目的是将有机层Ce3+转移到水层。使Ce3+尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
③与“反萃取”得到的水溶液比较,过滤Ce2(CO3)3溶液的滤液中,物质的量减小的离子有
(4)实验中需要测定溶液中Ce3+的含量。已知水溶液中Ce4+可用准确浓度的
 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:
。请补充完整实验方案:
①准确量取
 溶液[
溶液[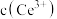 约为
约为 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;
容量瓶中后定容;②按规定操作分别将
 和待测Ce4+溶液装入如图所示的滴定管中;③
和待测Ce4+溶液装入如图所示的滴定管中;③
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
名校
解题方法
【推荐1】氢气被看做是理想的“绿色能源”,氢气的制备和储存是目前的研究热点。
I制氢
(1)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如下:

①甲烷和水蒸气反应的化学方程式是_________ 。
②600℃时加入CaO的作用是__________ 。
(2)还可利用太阳能光伏电池电解水制高纯氢,工作示意图如图甲。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接__________ (填“K1”或“K2”);改变开关连接方式,可得O2。
②利用太阳能光伏电池电解水制高纯氢的总反应化学方程式为__________ 。
Ⅱ储氢
(3)镁铝合金(Mg17Al12)是一种潜在的储氢材料,在氩气保护下,将一定化学计量比的Mg、A1单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为 ,反应后得到的混合物在一定条件下可释放出H2。
,反应后得到的混合物在一定条件下可释放出H2。
①根据完全吸氢的化学方程式计算:3.66g镁铝合金(Mg17A112)理论上能吸收氢气的质量为多少_________ ?(写出计算过程)。
②图乙为氢气球磨镁铝合金在不同温度下的放氢曲线(氢气球磨镁铝合金材料的储氢量约为3.03%),根据以上信息,下列关于镁铝合金储氢材料的说法正确的是_________ 。
a.镁铝合金的熔点介于金属镁和金属铝之间
b.镁铝合金在氩气中熔炼的目的是防止金属被氧化
c.由图可知,当温度高于260℃时,几乎所有的储存氢都能放出
d.当放氢温度由260℃升至320℃时,放氢的速度变快
I制氢
(1)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如下:

①甲烷和水蒸气反应的化学方程式是
②600℃时加入CaO的作用是
(2)还可利用太阳能光伏电池电解水制高纯氢,工作示意图如图甲。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接
②利用太阳能光伏电池电解水制高纯氢的总反应化学方程式为
Ⅱ储氢
(3)镁铝合金(Mg17Al12)是一种潜在的储氢材料,在氩气保护下,将一定化学计量比的Mg、A1单质在一定温度下熔炼获得。该合金在一定条件下完全吸氢的反应方程式为
 ,反应后得到的混合物在一定条件下可释放出H2。
,反应后得到的混合物在一定条件下可释放出H2。①根据完全吸氢的化学方程式计算:3.66g镁铝合金(Mg17A112)理论上能吸收氢气的质量为多少
②图乙为氢气球磨镁铝合金在不同温度下的放氢曲线(氢气球磨镁铝合金材料的储氢量约为3.03%),根据以上信息,下列关于镁铝合金储氢材料的说法正确的是
a.镁铝合金的熔点介于金属镁和金属铝之间
b.镁铝合金在氩气中熔炼的目的是防止金属被氧化
c.由图可知,当温度高于260℃时,几乎所有的储存氢都能放出
d.当放氢温度由260℃升至320℃时,放氢的速度变快
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐2】下表是20℃时部分物质的溶解度数据。
氢氧化铝为两性氢氧化物,能与酸反应也,能与强碱反应,与氢氧化钠反应能生成偏铝酸钠(NaAlO2)和水
(1)配制溶液。其中配制20℃时100g饱和氯化铝溶液的基本步骤是:称取氯化铝固体—量取水—溶解—装瓶贴标签。
①称取氯化铝固体的质量_____________ g。
②量取水加加入烧杯溶解。
③装瓶后贴标签,在标签上填写:_____________ 。
(2)进行性质探究实验。20℃时,根据数据回答下列问题:
①向氯化铝溶液中通入氢氧化钠直至过量,先生成Al(OH)3,再转化为NaAlO2,可观察到的现象是___________ ;Al(OH)3与氢氧化钠的反应方程式反应__________ 。
②将100g饱和氯化铝溶液,与足量的氢氧化钠反应能生成NaAlO2___________ g,同时需10%氢氧化钠溶液的质量至少为__________ g。(计算结果精确到0.1)
| 物质 | NaOH | AlCl3 | Al(OH)3 |
| 溶解度/g | 109 | 69.9 | 0.0015 |
(1)配制溶液。其中配制20℃时100g饱和氯化铝溶液的基本步骤是:称取氯化铝固体—量取水—溶解—装瓶贴标签。
①称取氯化铝固体的质量
②量取水加加入烧杯溶解。
③装瓶后贴标签,在标签上填写:
(2)进行性质探究实验。20℃时,根据数据回答下列问题:
①向氯化铝溶液中通入氢氧化钠直至过量,先生成Al(OH)3,再转化为NaAlO2,可观察到的现象是
②将100g饱和氯化铝溶液,与足量的氢氧化钠反应能生成NaAlO2
您最近一年使用:0次
填空与简答-填空题
|
困难
(0.15)
【推荐3】用金属铁通过一系列转化,可以制备新型消毒、净水剂K2FeO4.流程如下:

请回答下列问题:
(1)固体B的成分是_____________ (用化学式表示);反应①后经过__________ 操作可分别得到固体B和溶液A.
(2)反应①、②、③中没有涉及到的化学基本反应类型是__________ .
(3)请写出反应②的化学方程式___________________________ .
(4)如果所得净水剂K2FeO4的质量为19.8kg,则理论上参加反应的铁的质量为____ kg.

请回答下列问题:
(1)固体B的成分是
(2)反应①、②、③中没有涉及到的化学基本反应类型是
(3)请写出反应②的化学方程式
(4)如果所得净水剂K2FeO4的质量为19.8kg,则理论上参加反应的铁的质量为
您最近一年使用:0次



