金属在生产、生活和社会发展中的应用较为广泛。
(1)下图所示是某景区无人机表演的场景。高性能无人机框架最适合选用密度小、强度高、耐热、耐疲劳的_______(填字母)。
(2)我国的高铁技术世界领先。高铁列车的车体建设需要消耗大量的铝合金,铝有很好的抗腐蚀性能是因为______ 。
(3)北宋张潜在其《浸铜要略序》一书中对铜的冶炼有如下记载:“山麓有胆泉,土人汲以浸铁,数日辄类朽木,刮取其屑,锻炼成铜。”书中提及的“胆泉”为硫酸铜溶液,“浸铁”即将铁放入其中,写出此冶炼铜方法中生成铜的化学方程式:______ 。
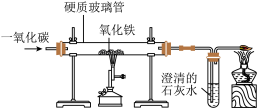
(4)铁轨通常用铁矿石制得,在如图所示的一氧化碳还原氧化铁实验中,证明一氧化碳具有还原性的实验现象是______ ;写出试管中发生反应的化学方程式:______ 。
①滤液中的溶质成分有哪些______ 。
②所得溶液质量与原混合溶液质量相比,如何变化:_________ 。
(6)河南是全国矿产资源大省之一。某钢铁公司采用CO在高温下与Fe3O4反应来炼铁,若每天生产生铁(含铁95%)800t,则该公司每天需要含Fe3O490%的磁铁矿石的质量是多少?(结果精确到0.1t)
(1)下图所示是某景区无人机表演的场景。高性能无人机框架最适合选用密度小、强度高、耐热、耐疲劳的_______(填字母)。

| A.不锈钢 | B.碳纤维复合材料 | C.合成纤维 |
(3)北宋张潜在其《浸铜要略序》一书中对铜的冶炼有如下记载:“山麓有胆泉,土人汲以浸铁,数日辄类朽木,刮取其屑,锻炼成铜。”书中提及的“胆泉”为硫酸铜溶液,“浸铁”即将铁放入其中,写出此冶炼铜方法中生成铜的化学方程式:
(4)铁轨通常用铁矿石制得,在如图所示的一氧化碳还原氧化铁实验中,证明一氧化碳具有还原性的实验现象是
①滤液中的溶质成分有哪些
②所得溶液质量与原混合溶液质量相比,如何变化:
(6)河南是全国矿产资源大省之一。某钢铁公司采用CO在高温下与Fe3O4反应来炼铁,若每天生产生铁(含铁95%)800t,则该公司每天需要含Fe3O490%的磁铁矿石的质量是多少?(结果精确到0.1t)
更新时间:2023-08-28 10:00:39
|
相似题推荐
综合应用题
|
较难
(0.4)
解题方法
【推荐1】金属用途广泛,其结构和性质等是化学研究的重要内容。
(1)镁常用于国防工业。下图是镁的原子结构示意图,下列说法不正确的是_______(填字母)。

(2)地壳中含量最高的金属元素可用于制作蒸锅,主要利用了金属的延展性和_______ 性;该金属制品具有较好的耐腐蚀性,用化学方程式表示原因:_______ 。
(3)下图所示装置可以用于多种气体的实验室制取。

①实验室用该装置制取氢气,反应的化学方程式是_______ 。
②制取CO2后,检验装置内的废液是否显酸性,可选用的试剂(或用品)较多,如紫色石蕊溶液、pH试纸、氧化铜和金属等。请写出一种满足要求的金属____ 。
(4)向一定量AgNO3和Cu(NO3)2混合溶液中加入锌粉,充分反应后过滤,得到溶液A和固体B。
①写出一定发生的反应的化学方程式_____ 。
②溶液A中的溶质不可能是Zn(NO3)2、AgNO3,其理由是什么?_____
(5)铁制品容易生锈,造成资源浪费。某工厂消耗质量分数为10%的废硫酸49t来除锈,并回收生成的盐。理论上可回收盐的质量是多少?(假设金属单质不参与反应,结果保留到0.1t)
(1)镁常用于国防工业。下图是镁的原子结构示意图,下列说法不正确的是_______(填字母)。

| A.镁原子的核外电子数为12 |
| B.在化合物中镁通常显+2价 |
| C.图中“x”的值为10 |
| D.镁位于元素周期表中第三周期 |
(3)下图所示装置可以用于多种气体的实验室制取。

①实验室用该装置制取氢气,反应的化学方程式是
②制取CO2后,检验装置内的废液是否显酸性,可选用的试剂(或用品)较多,如紫色石蕊溶液、pH试纸、氧化铜和金属等。请写出一种满足要求的金属
(4)向一定量AgNO3和Cu(NO3)2混合溶液中加入锌粉,充分反应后过滤,得到溶液A和固体B。
①写出一定发生的反应的化学方程式
②溶液A中的溶质不可能是Zn(NO3)2、AgNO3,其理由是什么?
(5)铁制品容易生锈,造成资源浪费。某工厂消耗质量分数为10%的废硫酸49t来除锈,并回收生成的盐。理论上可回收盐的质量是多少?(假设金属单质不参与反应,结果保留到0.1t)
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐2】金属在人类文明史上有着重要的意义,某小组同学以金属为主题开展项目式学习
(1)金属的发展历程:人类冶炼不同金属的年代大致如下,据此分析冶炼金属的早晚主要和_____ 有关。

(2)金属的冶炼:明代宋应星的《天工开物》描绘了我国古代炼铁术。同学们用如图装置进行模拟炼铁。

①写出A处发生反应的化学方程式_____ 。
②分析装置中气球的作用是_____ 。
③能证明氧化铁已经被完全还原为铁的证据是______ 。
(3)金属活动性顺序的探究:如图1是探究铁、铜、银三种金属活动性顺序的实验,实验过程观察到两个试管中溶液颜色均发生了变化。

①通过该实验得出三种金属的活功性顺序为_____ 。
②写出该实验发生反应的化学方程式______ (写出一个即可)。
③将A中剩余的铁加入B中回收B试管溶液中的金属。试管B中固体质量的变化曲线如图2所示,至t时间后固体质量不再变化。分析最后B试管中的固体成分是_____ 。 (写出有情况)
(4)金属的应用:实验室常用锌与稀硫酸反应制取氢气。若用500 g溶质质量分数为9.8%的稀硫酸与足量锌反应制取氢气,请计算生成氢气的质量。
(1)金属的发展历程:人类冶炼不同金属的年代大致如下,据此分析冶炼金属的早晚主要和

(2)金属的冶炼:明代宋应星的《天工开物》描绘了我国古代炼铁术。同学们用如图装置进行模拟炼铁。

①写出A处发生反应的化学方程式
②分析装置中气球的作用是
③能证明氧化铁已经被完全还原为铁的证据是
(3)金属活动性顺序的探究:如图1是探究铁、铜、银三种金属活动性顺序的实验,实验过程观察到两个试管中溶液颜色均发生了变化。

①通过该实验得出三种金属的活功性顺序为
②写出该实验发生反应的化学方程式
③将A中剩余的铁加入B中回收B试管溶液中的金属。试管B中固体质量的变化曲线如图2所示,至t时间后固体质量不再变化。分析最后B试管中的固体成分是
(4)金属的应用:实验室常用锌与稀硫酸反应制取氢气。若用500 g溶质质量分数为9.8%的稀硫酸与足量锌反应制取氢气,请计算生成氢气的质量。
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】某化学小组向 Al(NO3)3、Cu(NO3)2和 AgNO3的混合溶液甲中加入一定量的锌粉,充分反应后过滤,得到固体乙和溶液丙,且溶液甲和溶液丙的质量相等。
(1)写出一个有关反应的化学方程式:______ 。
(2)写出溶液丙中一定含有的金属离子:______ 、 ______ (写化学符号)。

(3)若溶液丙为蓝色,向固体乙上滴加盐酸___ (填“一定有”“可能有”或“一定没有”)气泡产生。
(3)向 10.7 g Mg、Al、Zn 固体混合物中加入一定量的 H2SO4恰好完全反应,反应后的溶液质量增加了 10.1 g,将反应后溶液蒸发结晶,干燥。获得固体质量为_____
a.15.5 g b.25.1 g c.39.5 g d.20.3 g
(1)写出一个有关反应的化学方程式:
(2)写出溶液丙中一定含有的金属离子:

(3)若溶液丙为蓝色,向固体乙上滴加盐酸
(3)向 10.7 g Mg、Al、Zn 固体混合物中加入一定量的 H2SO4恰好完全反应,反应后的溶液质量增加了 10.1 g,将反应后溶液蒸发结晶,干燥。获得固体质量为
a.15.5 g b.25.1 g c.39.5 g d.20.3 g
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】金属材料是日常生活中应用广泛的材料。
(1)①铜运用于航母的电力系统是利用了铜的___________ 性。
②金属铝比铁活泼,但铝制品更耐腐蚀的原因是___________ 。
③废旧铁锅、铝锅不要随意丢弃,应回收利用。这样做的意义是_________ 。(答一点即可)
(2)某化学小组在Al(NO3)3,Cu(NO3)2和AgNO3的混合溶液甲中加入一定量的锌粉,充分反应后过滤,得到固体乙和溶液丙。且溶液甲和溶液丙的质量相等。

①写出一个有关反应的化学方程式_____________ 。
②向固体乙上滴加盐酸______________ 。(选填“一定有”、“可能有”或“一定没有”)气泡产生。
③写出溶液丙中一定含有的金属离子_____________ (写化学符号)。
(3)利用下图装置可以用纯净、干燥的CO还原Fe2O3并检验气体产物。已知一氧化碳发生装置得到的CO中混有杂质CO2和H2O(氢氧化钠溶液可以吸收二氧化碳;浓硫酸具有吸水性,可以做干燥剂)。

①装置B中应盛放的试剂是___________ 。
②装置C玻璃管中观察到的现象是____________ 。
③实验中装置E的作用是___________ 。
(1)①铜运用于航母的电力系统是利用了铜的
②金属铝比铁活泼,但铝制品更耐腐蚀的原因是
③废旧铁锅、铝锅不要随意丢弃,应回收利用。这样做的意义是
(2)某化学小组在Al(NO3)3,Cu(NO3)2和AgNO3的混合溶液甲中加入一定量的锌粉,充分反应后过滤,得到固体乙和溶液丙。且溶液甲和溶液丙的质量相等。

①写出一个有关反应的化学方程式
②向固体乙上滴加盐酸
③写出溶液丙中一定含有的金属离子
(3)利用下图装置可以用纯净、干燥的CO还原Fe2O3并检验气体产物。已知一氧化碳发生装置得到的CO中混有杂质CO2和H2O(氢氧化钠溶液可以吸收二氧化碳;浓硫酸具有吸水性,可以做干燥剂)。

①装置B中应盛放的试剂是
②装置C玻璃管中观察到的现象是
③实验中装置E的作用是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】金属材料对于促进生产发展、改善人类生活发挥了重大作用。
(1)铝具有很好的抗腐蚀性能,原因是_________ 。
(2)一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式_________ 。
(3)向硝酸银溶液中加入一定质量的锌粉和铜粉的混合物,充分反应后过滤,得到滤渣和滤液。以下推断正确的是_________ 。
A 若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定有银、铜、锌
B 若滤液为无色,则滤渣中一定有锌
C 若滤液为蓝色,则滤液中一定有硝酸银、硝酸铜和硝酸锌
D 滤渣的质量一定比反应前锌粉和铜粉混合物质量大
(4)下列保护金属资源的做法不正确的是_________ 。
A 任意开采矿物
B 回收利用废旧金属
C 铁制品存放在潮湿的环境中
D 用塑料代替金属材料制造管道
(5)某废弃物中可能含有Cu、CuO、Mg、Zn中的一种或几种,为确定其成分并回收金属,取样品进行如图实验。

①步骤Ⅱ的操作是_________ 。
②步骤Ⅱ中产生的现象是_________ 。步骤Ⅰ中锌和稀硫酸反应的化学方程式为_________ 。
③若溶液C中只含一种溶质,则样品的成分是_________ 。
④通过测氢气的质量,也可确定样品的成分,则w的值为_________ (用m和n的代数式表示)。
(1)铝具有很好的抗腐蚀性能,原因是
(2)一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式
(3)向硝酸银溶液中加入一定质量的锌粉和铜粉的混合物,充分反应后过滤,得到滤渣和滤液。以下推断正确的是
A 若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定有银、铜、锌
B 若滤液为无色,则滤渣中一定有锌
C 若滤液为蓝色,则滤液中一定有硝酸银、硝酸铜和硝酸锌
D 滤渣的质量一定比反应前锌粉和铜粉混合物质量大
(4)下列保护金属资源的做法不正确的是
A 任意开采矿物
B 回收利用废旧金属
C 铁制品存放在潮湿的环境中
D 用塑料代替金属材料制造管道
(5)某废弃物中可能含有Cu、CuO、Mg、Zn中的一种或几种,为确定其成分并回收金属,取样品进行如图实验。

①步骤Ⅱ的操作是
②步骤Ⅱ中产生的现象是
③若溶液C中只含一种溶质,则样品的成分是
④通过测氢气的质量,也可确定样品的成分,则w的值为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】某化学小组向 Al(NO3)3、Cu(NO3)2和 AgNO3的混合溶液甲中加入一定量的锌粉,充分反应后过滤,得到固体乙和溶液丙,且溶液甲和溶液丙的质量相等。
(1)写出一个有关反应的化学方程式:______ 。
(2)写出溶液丙中一定含有的金属离子:______ 、 ______ (写化学符号)。

(3)若溶液丙为蓝色,向固体乙上滴加盐酸___ (填“一定有”“可能有”或“一定没有”)气泡产生。
(3)向 10.7 g Mg、Al、Zn 固体混合物中加入一定量的 H2SO4恰好完全反应,反应后的溶液质量增加了 10.1 g,将反应后溶液蒸发结晶,干燥。获得固体质量为_____
a.15.5 g b.25.1 g c.39.5 g d.20.3 g
(1)写出一个有关反应的化学方程式:
(2)写出溶液丙中一定含有的金属离子:

(3)若溶液丙为蓝色,向固体乙上滴加盐酸
(3)向 10.7 g Mg、Al、Zn 固体混合物中加入一定量的 H2SO4恰好完全反应,反应后的溶液质量增加了 10.1 g,将反应后溶液蒸发结晶,干燥。获得固体质量为
a.15.5 g b.25.1 g c.39.5 g d.20.3 g
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】人类对金属的冶炼和使用经历了漫长的历史。
(1)模拟炼铁的实验装置如图所示,请回答下列问题:

加热氧化铁之前,先通一段时间CO的作用是________ 。加热后,玻璃管中的实验现象为: ________ ;试管里的澄清石灰水变浑浊,原因是 ________ (用化学方程式表示);实验设计的最后一步放置酒精灯目的是 ____ 。
(2)为测定某赤铁矿石中氧化铁的质量分数,用足量的一氧化碳与20g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用氢氧化钠溶液完全吸收,溶液总质量与反应时间的变化关系如图。上述反应产生二氧化碳的质量为________ g。
(3)该赤铁矿石中氧化铁的质量分数___ 。(根据化学方程式写出完整的计算步骤,结果保留一位小数)

(1)模拟炼铁的实验装置如图所示,请回答下列问题:

加热氧化铁之前,先通一段时间CO的作用是
(2)为测定某赤铁矿石中氧化铁的质量分数,用足量的一氧化碳与20g赤铁矿石样品充分反应(杂质不参与反应),并将生成的气体用氢氧化钠溶液完全吸收,溶液总质量与反应时间的变化关系如图。上述反应产生二氧化碳的质量为
(3)该赤铁矿石中氧化铁的质量分数

您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】今年扬州迎来高铁交通发展的高潮。高铁给我们带来的不仅是交通方便,出行快捷,甚至是带来旅游业的繁荣。制造铁轨需要大量的合金钢,新集中学化学兴趣小组为此展开探究:
(一)工业上炼铁炼钢和轧制钢材的主要流程如下图:
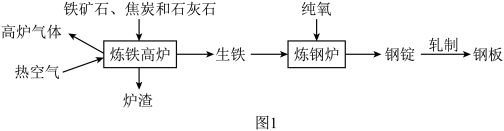
已知:生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(1)炼铁的固体原料中加入焦炭的作用是_____ ,_____ (用方程式表示);
(2)炼铁的固体原料需经过粉碎,其目的是_____ ;
(3)热空气和高炉气体的主要成分有一种相同,这种气体是_____ (填化学式);
(4)炼钢炉中,通入纯氧而不用空气的目的是_____ 。将钢锭轧成钢板,体现了金属的_____ 性。
(二)该兴趣小组发现未经处理的钢铁容易生锈。同学们接着探究了铁生锈的相关问题。
【知识回顾】铁生锈的条件为铁与_____ 、_____ 同时接触,为了防止铁制品生锈,应采取的措施是_____ (写出一种)。
【查阅资料】铁锈成分复杂,化学式可简单表示为Fe2O3•nH2O,在加热时会分步反应,首先失去结晶水,其反应可表示为Fe2O3•nH2O Fe2O3+nH2O。浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
Fe2O3+nH2O。浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
【提出问题】铁锈(Fe2O3•nH2O)中n的值等于多少呢?
【问题探究】小明发现实验室中有一保管不善的铁粉,大部分已经结块成红褐色,为了探究铁锈(Fe2O3•nH2O)的组成,称取27.0g这种铁粉样品,按如图2所示装置进行实验。

(1)实验前应先_____ ;
(2)为了保证实验安全,实验开始时应先_____ ,目的是_____ ;
(3)D的作用是_____ ;
(4)请指出该装置中有一处明显不足_____ ;
【数据处理】图3是加热时间和A中固体质量关系图象,下表是B、C中质量不再变化时B中浓硫酸、C中碱石灰装置质量变化情况。

(5)铁锈(Fe2O3•nH2O)中n的值是_____ ;
(6)写出T3﹣T4时间段发生反应的化学方程式_____ ;
(7)计算原样品中单质铁的质量分数是_____ 。(计算结果保留到0.1%)
(一)工业上炼铁炼钢和轧制钢材的主要流程如下图:

已知:生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
(1)炼铁的固体原料中加入焦炭的作用是
(2)炼铁的固体原料需经过粉碎,其目的是
(3)热空气和高炉气体的主要成分有一种相同,这种气体是
(4)炼钢炉中,通入纯氧而不用空气的目的是
(二)该兴趣小组发现未经处理的钢铁容易生锈。同学们接着探究了铁生锈的相关问题。
【知识回顾】铁生锈的条件为铁与
【查阅资料】铁锈成分复杂,化学式可简单表示为Fe2O3•nH2O,在加热时会分步反应,首先失去结晶水,其反应可表示为Fe2O3•nH2O
 Fe2O3+nH2O。浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
Fe2O3+nH2O。浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。【提出问题】铁锈(Fe2O3•nH2O)中n的值等于多少呢?
【问题探究】小明发现实验室中有一保管不善的铁粉,大部分已经结块成红褐色,为了探究铁锈(Fe2O3•nH2O)的组成,称取27.0g这种铁粉样品,按如图2所示装置进行实验。

(1)实验前应先
(2)为了保证实验安全,实验开始时应先
(3)D的作用是
(4)请指出该装置中有一处明显不足
【数据处理】图3是加热时间和A中固体质量关系图象,下表是B、C中质量不再变化时B中浓硫酸、C中碱石灰装置质量变化情况。

| 反应前(g) | 反应后(g) | |
| B | 100 | 105.4 |
| C | 150 | 163.2 |
(6)写出T3﹣T4时间段发生反应的化学方程式
(7)计算原样品中单质铁的质量分数是
您最近一年使用:0次
综合应用题
|
较难
(0.4)
名校
解题方法
【推荐3】人类社会发展离不开金属材料,结合所学知识,回答下列问题:
(1)生活中使用的金属材料大多是合金,而不是纯金属,这是因为合金具有更多优良性能。下列属于金属材料的是______(填字母)。
(2)下列用品中,主要利用金属导电性的是______(填字母)。
(3)为了一次性验证铜、铝、银三种金属的活动性顺序,下列四种方案中可行的是______ (填序号)。
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(4)工业炼铁的原理是一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,写出该反应的化学方程式______ 。某钢铁厂每天需消耗4900 t含Fe2O3 76%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁的质量是______ t。
(5)如图是初中化学教科书中探究铁生锈条件的实验装置示意图,请回答下列问题:

该实验通过对比______ (选填试管编号)两支试管中的现象,可得出铁生锈与水有关,通过该实验还可得出铁生锈不仅与水有关,还与空气中的______ 有关(写化学式) 。请写出一种防止厨房里铁锅生锈的具体措施______ 。为什么铝锅比铁锅更耐腐蚀,原因是______ (用化学方程式表示)。
(6)为了测定某银、锌合金(假设合金中只含银和锌)中银的质量分数,某同学称取20g银锌合金粉末进行实验,现将125g稀硫酸分五次加入合金粉末中,充分反应后测得生成气体的总质量如表所示:
请完成下列问题:
①表中m的值为______ ;
②银、锌合金中银的质量分数为______ 。(写出计算过程)
(1)生活中使用的金属材料大多是合金,而不是纯金属,这是因为合金具有更多优良性能。下列属于金属材料的是______(填字母)。
| A.黄铜 | B.塑料 | C.生铁 |
| A.铂金饰品 | B.铁锅 | C.铝导线 |
①将铝、银分别浸入到硫酸铜溶液中 ②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中 ④将铜分别浸入到硫酸铝、硝酸银溶液中
(4)工业炼铁的原理是一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,写出该反应的化学方程式
(5)如图是初中化学教科书中探究铁生锈条件的实验装置示意图,请回答下列问题:

该实验通过对比
(6)为了测定某银、锌合金(假设合金中只含银和锌)中银的质量分数,某同学称取20g银锌合金粉末进行实验,现将125g稀硫酸分五次加入合金粉末中,充分反应后测得生成气体的总质量如表所示:
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 滴入稀硫酸的质量/g | 25 | 25 | 25 | 25 | 25 |
| 生成气体的总质量/g | 0.05 | m | 0.15 | 0.20 | 0.20 |
①表中m的值为
②银、锌合金中银的质量分数为
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐1】材料学的发展水平,制约着制造业的发展水平。
(1)在棉花、玻璃钢、橡胶、塑料几种物质中属于复合材料的是________________ 。
(2)金属材料应用广泛。
①铝制品经久耐用的原因是________________________________ ;
②铁制品被腐蚀的外界条件是___________________ ;
③下图是实验室模拟用铁矿石炼铁的装置。

氧化铁和CO发生反应时的化学方程式为___________________ ;试验结束后,取少量B中溶液于试管中,滴加过量的BaCl2溶液,生成沉淀,再在上层澄清溶液中滴加酚酞试液,溶液呈现红色。由此可知此时B中溶液的成分是________________ 。
(3)硅(S)属于重要的无机非金属材料
①工业上用SiO2和过量的C混合,高温条件下反应制备硅单质。则制取中设备排放出的气态氧化物主要是___________________ ;
②玻璃中的SiO2和NaOH溶液反应,生成具有黏合剂作用的Na2SiO3,反应的化学方程式应为_________________________ ;
(4)钼(Mo)是一种重要的战略物质。河南的钼储量全国最多,洛阳钼业生产的钼酸铵【(NH4)2MoO4】,在一定温度下分解成氨、水和三氧化钼。请计算49kg的钼酸铵,完全分解可以制得三氧化钼__________________________ 千克?
(1)在棉花、玻璃钢、橡胶、塑料几种物质中属于复合材料的是
(2)金属材料应用广泛。
①铝制品经久耐用的原因是
②铁制品被腐蚀的外界条件是
③下图是实验室模拟用铁矿石炼铁的装置。

氧化铁和CO发生反应时的化学方程式为
(3)硅(S)属于重要的无机非金属材料
①工业上用SiO2和过量的C混合,高温条件下反应制备硅单质。则制取中设备排放出的气态氧化物主要是
②玻璃中的SiO2和NaOH溶液反应,生成具有黏合剂作用的Na2SiO3,反应的化学方程式应为
(4)钼(Mo)是一种重要的战略物质。河南的钼储量全国最多,洛阳钼业生产的钼酸铵【(NH4)2MoO4】,在一定温度下分解成氨、水和三氧化钼。请计算49kg的钼酸铵,完全分解可以制得三氧化钼
您最近一年使用:0次
综合应用题
|
较难
(0.4)
【推荐2】见证中国力量,实现民族复兴
(1)中国“嫦娥四号”登月探测器首次在月球背面软着陆。“嫦娥四号”月球探测器首次证实构成月幔的主要物质之一是Fe2SiO4,Fe2SiO4从物质的分类上属于______ (填“氧化物”或“酸”或“碱”或“盐”)。“嫦娥四号”月球探测器中使用了大量材料如铝合金、高效吸能合金、有机高分子薄膜、玻璃钢等,这些材料中属于复合材料的是______ ;铝合金的优点是______ (写一条即可)。
(2)12月11日上午,由我国自主设计的世界首座高速铁路悬索桥一五峰山长江大桥正式通车。建设者采用了一系列国内自主生产的新材料,获得20余项专利,创造了多项纪录,代表着中国乃至世界同类型桥梁建设的最高水平。请根据材料及所学知识回答下列问题:
①高速铁路离不开无缝钢轨,无缝钢轨表面有防锈涂漆,起到防锈的作用。铁生锈是铁与空气中的______ 、______ 共同作用的结果。下列实验组合能够达到验证上述结论目的的是______ 。

A.②③ B.①②③ C.②③⑤ D.②③④
②工人师傅在焊接钢铁制品时,通常先用稀盐酸清洗铁制品表面的铁锈,该反应的化学方程式为______ ,基本反应类型为______ 反应。
(3)1926年我国科学家侯德榜创立侯氏制碱法,以饱和食盐水、二氧化碳、氨气等为主要原料制取纯碱,大大提高了食盐的利用率,促进了世界制碱技术的发展。Na2CO3和NH4C1的溶解度曲线如图所示,请回答下列问题:

①根据如图所示,写出P点表示的意义______ (写出一条即可)。
②t1℃时,50g水中加入15gNa2CO3固体,经充分搅拌后,所得溶液的质量为______ g。
③t1℃时,将不同质量的NH4C1饱和溶液和Na2CO3饱和溶液均升温至t2℃。此时,NH4C1溶液的溶质质量分数______ Na2CO3溶液的溶质质量分数(填写“大于”、“等于”、“小于”之一)。
④氯化铵是一种常用的化肥。下列有关化肥与农药的说法中,不正确的是______ 。
A.铵态氮肥与碱性物质混合使用会降低肥效
B.波尔多液(主要成分是硫酸铜)是常用的农药,可用铁桶盛放
C.开发研制和推广使用新型高效、低毒、低残留的农药
D.大棚种植中常用二氧化碳作为气态肥料
(1)中国“嫦娥四号”登月探测器首次在月球背面软着陆。“嫦娥四号”月球探测器首次证实构成月幔的主要物质之一是Fe2SiO4,Fe2SiO4从物质的分类上属于
(2)12月11日上午,由我国自主设计的世界首座高速铁路悬索桥一五峰山长江大桥正式通车。建设者采用了一系列国内自主生产的新材料,获得20余项专利,创造了多项纪录,代表着中国乃至世界同类型桥梁建设的最高水平。请根据材料及所学知识回答下列问题:
①高速铁路离不开无缝钢轨,无缝钢轨表面有防锈涂漆,起到防锈的作用。铁生锈是铁与空气中的

A.②③ B.①②③ C.②③⑤ D.②③④
②工人师傅在焊接钢铁制品时,通常先用稀盐酸清洗铁制品表面的铁锈,该反应的化学方程式为
(3)1926年我国科学家侯德榜创立侯氏制碱法,以饱和食盐水、二氧化碳、氨气等为主要原料制取纯碱,大大提高了食盐的利用率,促进了世界制碱技术的发展。Na2CO3和NH4C1的溶解度曲线如图所示,请回答下列问题:

①根据如图所示,写出P点表示的意义
②t1℃时,50g水中加入15gNa2CO3固体,经充分搅拌后,所得溶液的质量为
③t1℃时,将不同质量的NH4C1饱和溶液和Na2CO3饱和溶液均升温至t2℃。此时,NH4C1溶液的溶质质量分数
④氯化铵是一种常用的化肥。下列有关化肥与农药的说法中,不正确的是
A.铵态氮肥与碱性物质混合使用会降低肥效
B.波尔多液(主要成分是硫酸铜)是常用的农药,可用铁桶盛放
C.开发研制和推广使用新型高效、低毒、低残留的农药
D.大棚种植中常用二氧化碳作为气态肥料
您最近一年使用:0次
综合应用题
|
较难
(0.4)
解题方法
【推荐3】金属及其化合物与我们的生活生产息息相关,其中铁及其化合物的使用最为广泛。
一、金属的广泛应用
(1)人体因摄入铁元素不足而易导致的疾病是________ ;
(2)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到__________ (填字母)
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
二、钢铁的冶炼和探究
(3)联合钢铁工业的基本生产流程示意如下:

①写出以赤铁矿为原料在高温下与一氧化碳反应制取铁的化学方程式:__________ 。
②生铁和钢的最大区别是:______________ 。
③某赤铁矿石中含Fe2O380%,用3000 t这种矿石,可炼出含杂质4%的生铁质量是多少________ ?(请写出计算过程)
(4)甲组同学取24gFe2O3粉末设计了如图1所示的实验装置测定一氧化碳与氧化铁反应后的固体产物。已知B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。

如果实验成功,请回答下列问题:
①写出A中玻璃管内反应的实验现象_________ 。
②实验开始应先通入一段时间的一氧化碳,再点燃酒精灯,目的是________ 。
③B、C装置的作用是_________ (填字母序号)
a 收集二氧化碳 b 检验二氧化碳 c 收集一氧化碳
(5)查阅资料得知CO与氧化铁反应,在不同的温度下,氧化铁因失氧程度不同而生成其他铁的氧化物(或铁单质)和CO2。乙组同学采集了用某种热分析仪记录的CO与氧化铁反应的有关数据,并得到固体质量与反应温度的关系曲线,如图2所示。根据相关信息,回答如下问题:
①图中D点对应的物质化学式为________ ;
②写出400℃~500℃发生的化学方程式________ 。
一、金属的广泛应用
(1)人体因摄入铁元素不足而易导致的疾病是
(2)铁与铬、镍等金属熔合可形成“不锈钢”,用不锈钢丝和聚乙烯纤维为原料可制作耐酸防护服材料。以上叙述中不涉及到
A 合金 B 无机非金属材料 C 合成材料 D 复合材料
二、钢铁的冶炼和探究
(3)联合钢铁工业的基本生产流程示意如下:

①写出以赤铁矿为原料在高温下与一氧化碳反应制取铁的化学方程式:
②生铁和钢的最大区别是:
③某赤铁矿石中含Fe2O380%,用3000 t这种矿石,可炼出含杂质4%的生铁质量是多少
(4)甲组同学取24gFe2O3粉末设计了如图1所示的实验装置测定一氧化碳与氧化铁反应后的固体产物。已知B装置中的液体为过量的氢氧化钠与氢氧化钙混合液,氢氧化钠吸收二氧化碳能力比氢氧化钙强。

如果实验成功,请回答下列问题:
①写出A中玻璃管内反应的实验现象
②实验开始应先通入一段时间的一氧化碳,再点燃酒精灯,目的是
③B、C装置的作用是
a 收集二氧化碳 b 检验二氧化碳 c 收集一氧化碳
(5)查阅资料得知CO与氧化铁反应,在不同的温度下,氧化铁因失氧程度不同而生成其他铁的氧化物(或铁单质)和CO2。乙组同学采集了用某种热分析仪记录的CO与氧化铁反应的有关数据,并得到固体质量与反应温度的关系曲线,如图2所示。根据相关信息,回答如下问题:
①图中D点对应的物质化学式为
②写出400℃~500℃发生的化学方程式
您最近一年使用:0次



