某兴趣小组同学对过氧化氢分解的实验进行如下探究。
实验1:探究过氧化氢溶液浓度、温度对反应速率的影响
【实验方案】在一定温度下,向相同质量的过氧化氢溶液中加入相同质量的二氧化锰(MnO2)粉末,测量收集150mL氧气(O2)所需的时间。
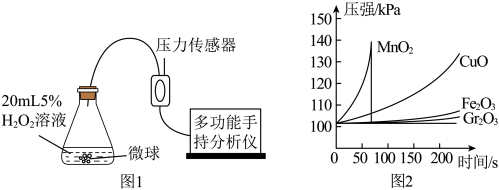
实验2:依据下图1装置进行实验(部分仪器略去),探究催化剂种类对反应速率的影响。
【实验方案】取用相同粒数的二氧化锰(MnO2)、氧化铜(CuO)、氧化铁(Fe2O3)、氧化铬(Gr2O3)四种催化剂微球(质量相等、表面积相同),分别进行实验,锥形瓶内压强随时间的变化如图2所示。
【解释与结论】
(1)实验1中反应的文字表达式是_______ 。二氧化锰在反应前后质量和_______ 没有发生改变。
(2)为了达到实验1的目的,补全实验方案。
①若a与b不相等,若a=15;则b=____ 。②若a与b相等,则设计实验I、III的目的是___ 。
(3)实验2中使用相同粒数催化剂微球的原因是_______ 。
(4)通过对实验2数据的分析,可得出的结论是_______ 。
【反思与评价】
(5)为了完成实验1,该兴趣小组收集氧气的装置可以选用下图中的_______。(可多选)
(6)实验1是通过测量收集等体积氧气(O2)所需时间来比较过氧化氢(H2O2)溶液分解的反应速率,还可以通过测量_______ 来比较过氧化氢(H2O2)溶液分解的反应速率。
(7)该兴趣小组成员通过网上查阅资料获悉:除二氧化锰、氧化铜、氧化铁、氧化铬外,硫酸铜、猪肝、马铃薯等也可以作为过氧化氢分解的催化剂。下列有关催化剂的说法正确的是_______
实验1:探究过氧化氢溶液浓度、温度对反应速率的影响
【实验方案】在一定温度下,向相同质量的过氧化氢溶液中加入相同质量的二氧化锰(MnO2)粉末,测量收集150mL氧气(O2)所需的时间。
| 实验序号 | 过氧化氢溶液的浓度/% | 温度/℃ | 时间/s |
| Ⅰ | 30 | 20 | 待测 |
| Ⅱ | 15 | 30 | 特测 |
| Ⅲ | a | b | 待测 |
【实验方案】取用相同粒数的二氧化锰(MnO2)、氧化铜(CuO)、氧化铁(Fe2O3)、氧化铬(Gr2O3)四种催化剂微球(质量相等、表面积相同),分别进行实验,锥形瓶内压强随时间的变化如图2所示。

【解释与结论】
(1)实验1中反应的文字表达式是
(2)为了达到实验1的目的,补全实验方案。
①若a与b不相等,若a=15;则b=
(3)实验2中使用相同粒数催化剂微球的原因是
(4)通过对实验2数据的分析,可得出的结论是
【反思与评价】
(5)为了完成实验1,该兴趣小组收集氧气的装置可以选用下图中的_______。(可多选)
A.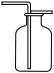 | B.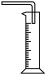 | C. | D.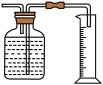 |
(7)该兴趣小组成员通过网上查阅资料获悉:除二氧化锰、氧化铜、氧化铁、氧化铬外,硫酸铜、猪肝、马铃薯等也可以作为过氧化氢分解的催化剂。下列有关催化剂的说法正确的是_______
| A.二氧化锰可作任何反应的催化剂 | B.同一个反应可能有多种催化剂 |
| C.催化剂一定能加快化学反应速率 | D.没有催化剂,化学反应不能发生 |
| E.在很多工业反应中,加入催化剂能起到增加生成物质量的效果 | |
更新时间:2023-10-14 21:28:04
|
相似题推荐
【推荐1】学习了二氧化锰对过氧化氢分解有催化作用的知识后,我们对催化剂已有了初步的认识。下列有关于催化剂的说法中错误的是_________ 。(填字母)
A.催化剂只能加快化学反应速率
B.催化剂可以增加产物的质量
C.二氧化锰是可做所有反应的催化剂
D.一个化学反应只有一种催化剂
实验一:某同学想:氧化铜(CuO)能否起到类似的催化剂作用呢?于是进行了以下探究。
【猜想与假设】
I.氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变:
II.氧化铜参与了反应产生氧气,反应前后质量和化学性质发生改变:
III.氧化铜是反应的催化剂,反应前后_________ 。
【进行实验】
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下图实验:

(1)请补充能证明猜想Ⅲ成立的实验现象:步骤③现象为_______ ,步骤⑥中二氧化锰固体质量为_____ g。结论:猜想成立。
(2)步骤①的目的是_________ 。
(3)定性判断步骤①和步骤②的反应快慢,可根据________ 。
(4)过氧化氢能被CuO催化分解放出氧气的符号表达式为_______ 。
实验二:探究制取氧气的适宜催化剂。实验方案如下:
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
II.取30粒含MnO2的海藻酸钠微球,采用如图2所示装置进行实验。改用其他三种微球,分别重复上述实验,得到如图3所示的锥形瓶内压强随时间变化的曲线图。

(5)每次实验时,海藻酸钠微球数应相同的目的是_______ 。
(6)从实验曲线看,催化效果较好、反应温和的催化剂是_______ (填化学符号)
(7)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是________ 。
(8)除上述影响过氧化氢溶液分解的因素外,你认为过氧化氢溶液的分解速率还可能与______ 有关。
A.催化剂只能加快化学反应速率
B.催化剂可以增加产物的质量
C.二氧化锰是可做所有反应的催化剂
D.一个化学反应只有一种催化剂
实验一:某同学想:氧化铜(CuO)能否起到类似的催化剂作用呢?于是进行了以下探究。
【猜想与假设】
I.氧化铜不是催化剂,也不参与反应,反应前后质量和化学性质不变:
II.氧化铜参与了反应产生氧气,反应前后质量和化学性质发生改变:
III.氧化铜是反应的催化剂,反应前后
【进行实验】
用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下图实验:

(1)请补充能证明猜想Ⅲ成立的实验现象:步骤③现象为
(2)步骤①的目的是
(3)定性判断步骤①和步骤②的反应快慢,可根据
(4)过氧化氢能被CuO催化分解放出氧气的符号表达式为
实验二:探究制取氧气的适宜催化剂。实验方案如下:
I.用MnO2、CuO、Fe2O3、Cr2O3四种催化剂分别与海藻酸钠溶液混合,滴入氯化钙溶液制成含等质量催化剂、大小相同的海藻酸钠微球,备用。
II.取30粒含MnO2的海藻酸钠微球,采用如图2所示装置进行实验。改用其他三种微球,分别重复上述实验,得到如图3所示的锥形瓶内压强随时间变化的曲线图。

(5)每次实验时,海藻酸钠微球数应相同的目的是
(6)从实验曲线看,催化效果较好、反应温和的催化剂是
(7)用含MnO2的海藻酸钠微球进行实验,60s时压强瞬间回落,其原因是
(8)除上述影响过氧化氢溶液分解的因素外,你认为过氧化氢溶液的分解速率还可能与
您最近一年使用:0次
【推荐2】通过近期的化学学习,相信你对制取气体的思路和方法有了一定的了解。
Ⅰ、氧气制取方法的梳理。
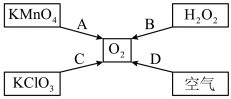
(1)用图中A、B、C所示的方法能够取氧气,是因为它们的反应物中都含有______ 。(填“氧元素”或“氧原子”)
(2)工业上用D制取氧气的方法为______ ,属于______ (填“物理”或“化学”)变化。
(3)写出方法A制取氧气的文字表达式______ 。该反应的基本反应类型为__________ 。
(4)小亮同学欲用过氧化氢溶液和二氧化锰制取氧气,可供选择的实验装置如下:
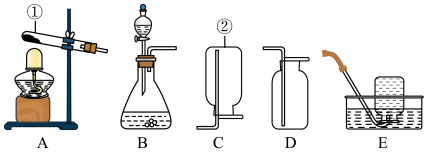
写出图中有标号仪器的名称:①______ ;②______ 。
请你帮助他选择一种发生装置______ (填字母序号,下同),小亮用E装置收集氧气,理由是______ 。若改用D装置收集,检验氧气集满的方法是______ 。
Ⅱ、大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是______ 化学反应速率(填“改变”或“加快”)。
(2)小亮及其研究小组发现,将适量红砖粉末放入过氧化氢溶液中,过氢化氢溶液的分解速率加快。对于此现象,该小组同学进行了如下探究:
【提出问题】红砖粉末能否作过氧化氢分解的催化剂?
【作出猜想】红砖粉末能作过氧化氢分解的催化剂。
【实验验证】
③写出红砖粉末催化过氧化氢分解的文字表达式:______ 。
【实验拓展】
④该小组设计了如图1所示装置对比红砖粉末与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据如表:
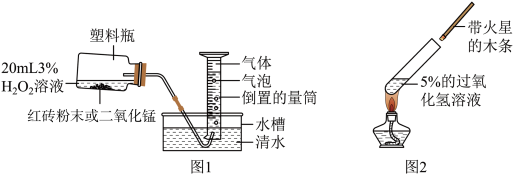
上述实验中若a>b,则可得出的结论是______ 。
⑤温度升高过氧化氢的分解速率会加快,某同学取足量5%的过氧化氢溶液进行加热,如图2所示,可实验中带火星的木条往往难以复燃,请解释原因______ 。
Ⅰ、氧气制取方法的梳理。

(1)用图中A、B、C所示的方法能够取氧气,是因为它们的反应物中都含有
(2)工业上用D制取氧气的方法为
(3)写出方法A制取氧气的文字表达式
(4)小亮同学欲用过氧化氢溶液和二氧化锰制取氧气,可供选择的实验装置如下:

写出图中有标号仪器的名称:①
请你帮助他选择一种发生装置
Ⅱ、大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是
(2)小亮及其研究小组发现,将适量红砖粉末放入过氧化氢溶液中,过氢化氢溶液的分解速率加快。对于此现象,该小组同学进行了如下探究:
【提出问题】红砖粉末能否作过氧化氢分解的催化剂?
【作出猜想】红砖粉末能作过氧化氢分解的催化剂。
【实验验证】
| 实验步骤 | 实验现象 | 结论及解释 |
实验1: | A中无明显现象,B中产生能使带火星的木条复燃的气体。 | ①B中产生的气体是 |
| 实验2:待实验1结束后,向B试管中重新加入的过氧化氢溶液,反应停止后过滤出红砖粉末、洗涤、干燥、称量 | B中又产生大量使带火星木条复燃的气体,红砖粉末质量为ag | ②红砖粉未的 |
【实验拓展】
④该小组设计了如图1所示装置对比红砖粉末与二氧化锰的催化效果,实验均以生成25mL气体为准,其他可能的影响因素忽略不计,相关数据如表:

实验编号 | 3%过氧化氢溶液的体积 | 其他物质质量 | 收集25mL气体所需时间 |
1 | 20mL | 红砖粉末0.5g | a |
2 | 20mL | 二氧化锰0.5g | b |
⑤温度升高过氧化氢的分解速率会加快,某同学取足量5%的过氧化氢溶液进行加热,如图2所示,可实验中带火星的木条往往难以复燃,请解释原因
您最近一年使用:0次
【推荐3】学习了过氧化氢制取氧气后,实验兴趣小组的同学进行了以下两个拓展探究;
【探究一】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其效果如何?
(1)实验Ⅱ、Ⅲ证明:氧化铁的质量和_______ 在反应前后均没有发生变化,可以作为过氧化氢分解的催化剂。
(2)实验Ⅲ的步骤中应填写_______ ;实验Ⅳ的步骤中应填写_______ 。
(3)设计实验Ⅳ的目的是_______ 。
【探究二】测定过氧化氢在二氧化锰的催化作用下分解生成O2的质量和体积,并处理数据。
【实验设计】通过下列两个实验分别测定O2的质量和体积:
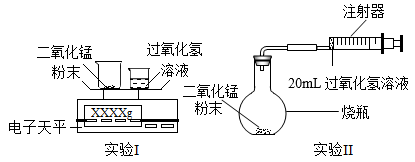
【记录与处理】
(4)已知实验Ⅰ反应前的总质量【m(大烧杯+二氧化锰粉末)+m(小烧杯+过氧化氢溶液)】要计算生成O2的质量,至少还需要的数据是_______ 。
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(5)实验Ⅰ中,已知反应前总质量为20g。过氧化氢溶液刚好分5次等质量加入大烧杯中,每一次待反应完全时,再加下一次。(注:过氧化氢在常温下自身分解产生的氧气忽略不计)。实验Ⅰ数据记录如下:
根据以上实验过程和数据综合分析,X的值等于_______ ;最终生成 O2的质量等于_______ g。
(6)实验Ⅱ中,如何检查装置的气密性_______
(7)经检查,装置不漏气,然后装好药品,用注射器将20mL过氧化氢溶液快速推入烧瓶中(装置中注射器活塞与内壁摩擦非常小,可忽略不计)。如果最终注射器活塞停在60mL处,则氧气的体积为_____ mL;理由是_______ 。
(8)若过氧化氢溶液是缓慢推入的,则可能造成的后果是_______ (不考虑仪器连接处脱落)。
【探究一】氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其效果如何?
| 实验步骤 | 实验现象 |
| Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象。 | A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
| Ⅱ.待A试管中没有现象发生时,重新加入5mL5%过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象。 | 试管中产生气泡,带火星木条复燃 |
| Ⅲ.将实验Ⅱ中的剩余物小心过滤,并进行洗涤、干燥、____(填操作) | 所得固体质量仍为ag |
| Ⅳ.分别量取___过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末向D试管中加入ag二氧化锰粉末,观察现象 |
(1)实验Ⅱ、Ⅲ证明:氧化铁的质量和
(2)实验Ⅲ的步骤中应填写
(3)设计实验Ⅳ的目的是
【探究二】测定过氧化氢在二氧化锰的催化作用下分解生成O2的质量和体积,并处理数据。
【实验设计】通过下列两个实验分别测定O2的质量和体积:

【记录与处理】
(4)已知实验Ⅰ反应前的总质量【m(大烧杯+二氧化锰粉末)+m(小烧杯+过氧化氢溶液)】要计算生成O2的质量,至少还需要的数据是
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(5)实验Ⅰ中,已知反应前总质量为20g。过氧化氢溶液刚好分5次等质量加入大烧杯中,每一次待反应完全时,再加下一次。(注:过氧化氢在常温下自身分解产生的氧气忽略不计)。实验Ⅰ数据记录如下:
| 加入次数/次 | 1 | 2 | 3 | 4 | 5 |
| 电子天平示数/g | 19.2 | 18.4 | 17.6 | 16.8 | X |
根据以上实验过程和数据综合分析,X的值等于
(6)实验Ⅱ中,如何检查装置的气密性
(7)经检查,装置不漏气,然后装好药品,用注射器将20mL过氧化氢溶液快速推入烧瓶中(装置中注射器活塞与内壁摩擦非常小,可忽略不计)。如果最终注射器活塞停在60mL处,则氧气的体积为
(8)若过氧化氢溶液是缓慢推入的,则可能造成的后果是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】初三某化学兴趣小组同学。依据教材实验对化学反应前后质量变化进行了探究。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【实验装置设计】甲、乙、丙小组同学分别设计如图装置:
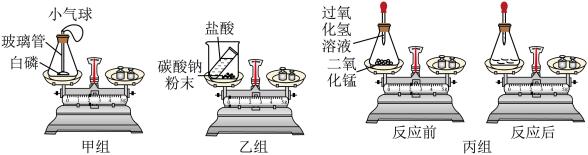
【讨论与探究】
(1)甲小组实验中,白磷燃烧时,在锥形瓶底部放少量细沙,其目的是:___________ ,实验过程中,除了看到红磷燃烧产生大量白烟这一明显现象外,还观察到气球___________ 。
(2)请根据乙组和丙组设计的“质量守恒定律”的实验装置进行探究,并按要求完成乙组和丙组实验。
①乙组实验结束后可观察到天平___________ (填“是”或“否”)平衡:此反应___________ (填“遵守”或“不遵守”)质量守恒定律。
②丙组过氧化氢溶液(少量)分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和___________ (填“大于”、“等于”或“小于”)反应后生成的各物质的质量总和。该反应中二氧化锰起___________ 作用。
【实验结论】
(3)通过甲、乙、丙实验探究,你得到的结论是:___________ 。
【实验分析】
(4)化学反应的过程是___________ 重新组合的过程。从微观角度分析,化学反应前后一定不变的是___________ (填数字序号)。
①原子种类②分子种类③原子数目④分子数目⑤原子质量
【反思与交流】
(5)两位同学通过交流反思得到启示,在探究化学反应前后物质的总质量是否发生改变时,对于___________ 的化学反应,一定要在密闭装置中进行。
【查阅资料】碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
【实验装置设计】甲、乙、丙小组同学分别设计如图装置:

【讨论与探究】
(1)甲小组实验中,白磷燃烧时,在锥形瓶底部放少量细沙,其目的是:
(2)请根据乙组和丙组设计的“质量守恒定律”的实验装置进行探究,并按要求完成乙组和丙组实验。
①乙组实验结束后可观察到天平
②丙组过氧化氢溶液(少量)分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和
【实验结论】
(3)通过甲、乙、丙实验探究,你得到的结论是:
【实验分析】
(4)化学反应的过程是
①原子种类②分子种类③原子数目④分子数目⑤原子质量
【反思与交流】
(5)两位同学通过交流反思得到启示,在探究化学反应前后物质的总质量是否发生改变时,对于
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐2】小雨阅读课外资料得知:双氧水分解除了用二氧化锰还可用氧化铜等物质作催化剂,于是她对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
(1)上述实验应测量的“待测数据"是_____________ ;
(2)若实验②比实验①的“待测数据”更___________ (选填“大"或“小"),说明氧化铜能加快氯酸钾的分解速率;
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,说明________________ ;
(4)再将该黑色粉末放入试管中,加入________________ ,若观察到_________ ,说明黑色粉末的化学性质在反应前后保持不变。
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是____________ 。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | CuO 0.5g | |
| ③ | 1.2g | MnO20.5g |
(1)上述实验应测量的“待测数据"是
(2)若实验②比实验①的“待测数据”更
(3)将实验②反应后的固体加水溶解、过滤、洗涤、干燥,若称量得到0.5g黑色粉末,说明
(4)再将该黑色粉末放入试管中,加入
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐3】君君和茵茵同学发现,带火星的木条在空气中不会复燃,但集气瓶中装有一定量氧气时能使带火星的木条复燃。为了找到能使带火星木条复燃的氧气含量最小值,他们进行了探究:
【提出问题】能使带火星木条复燃的氧气含量最小值是多少?
【设计实验】君君和茵茵计划用如下图的装置来制取氧气,该装置的圆底烧杯中放入25毫升水的目的是______ 。
【实验思路】君君设想:以排水法收集氧气,通过排出集气瓶中预留水的量来控制所装纯氧气的体积,其余装空气,从而寻找出理想的答案。
【实验探究】第一组实验:君君取3只集气瓶,编号为①②③,标记预留15%、30%和45%水的水位线并装水,盖上玻片倒置在水槽中、当制氧产生气泡______ 放出时,导管口伸入集气瓶小心把预留的15%、30%和45%水排出,将相同的3支带火星木条分别插入①~③号瓶中,记录实验现象,茵茵则按类似做法做了第二组实验,并记录实验现象。两组实验数据和现象见下表:

【反复探究】得出上述两组实验现象后,茵茵认为还不能确定能使带火星木条复燃的氧气含量最小值,需继续进行第三组实验。则第三组实验序号⑦⑧⑨的集气瓶装水的体积分数从小到大依次分别应该是______ 。
【实验结论】再经过数次重复实验后,确认序号⑧实验即留水______ %时恰好能使带火星木条复燃,为实验所寻求的“最小值”。
【列式计算】此时能使带火星木条复燃的氧气含量最小值为______ 。
【提出问题】能使带火星木条复燃的氧气含量最小值是多少?
【设计实验】君君和茵茵计划用如下图的装置来制取氧气,该装置的圆底烧杯中放入25毫升水的目的是
【实验思路】君君设想:以排水法收集氧气,通过排出集气瓶中预留水的量来控制所装纯氧气的体积,其余装空气,从而寻找出理想的答案。
【实验探究】第一组实验:君君取3只集气瓶,编号为①②③,标记预留15%、30%和45%水的水位线并装水,盖上玻片倒置在水槽中、当制氧产生气泡

实验分组 | 第一组 | 第二组 | ||||
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
集气瓶装水的体积分数/% | 15 | 30 | 45 | 34 | 38 | 42 |
带火星木条状况 | 亮 | 很亮 | 复燃 | 很亮 | 复燃 | 复燃 |
【实验结论】再经过数次重复实验后,确认序号⑧实验即留水
【列式计算】此时能使带火星木条复燃的氧气含量最小值为
您最近一年使用:0次
科学探究题
|
较难
(0.4)
解题方法
【推荐1】实验小组研究不同催化剂对过氧化氢分解速率的影响。
【查阅资料】
i.MnO2、FeCl3均可作为加快过氧化氢分解速率的催化剂。
ii.锥形瓶内氧气浓度达到最大值时,表明过氧化氢已完全分解。
【实验准备】组装图1所示装置(夹持仪器已略),经检验,装置的气密性良好。

实验1:比较催化剂种类对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入催化剂,用注射器推入过氧化氢溶液,记录实验数据。
【解释与结论】
(1)用MnO2催化过氧化氢分解的文字表达式为_______ 。
(2)为达成实验1的目的,需要被控制成相同的变量有过氧化氢溶液的浓度、_______ 和_______ 。
(3)依据实验1的数据可推知MnO2催化过氧化氢分解的速率大于FeCl3,其证据是_______ 。
实验2:继续探究FeCl3质量对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入FeCl3,用注射器推入5% 过氧化氢溶液,记录实验数据。
【解释与结论】
(4)由实验2可得结论:过氧化氢溶液体积等条件相同时,FeCl3质量在0.03~0.05g范围内,___ 。
【反思与评价】
(5)实验小组用1-2的方案制备氧气,发现反应速率偏慢。根据上述实验结论,你认为可采取的改进措施有_______ (写出两条)。
【查阅资料】
i.MnO2、FeCl3均可作为加快过氧化氢分解速率的催化剂。
ii.锥形瓶内氧气浓度达到最大值时,表明过氧化氢已完全分解。
【实验准备】组装图1所示装置(夹持仪器已略),经检验,装置的气密性良好。

实验1:比较催化剂种类对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入催化剂,用注射器推入过氧化氢溶液,记录实验数据。
| 序号 | 药品 | 氧气浓度传感器的数据 | |
| 1-1 | 3 mL、5% 过氧化氢溶液 | 0.03 g MnO2固体 | 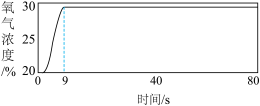 |
| 1-2 | 3 mL、5% 过氧化氢溶液 | 0.03 g FeCl3固体 | 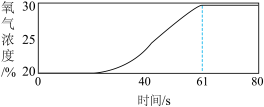 |
(1)用MnO2催化过氧化氢分解的文字表达式为
(2)为达成实验1的目的,需要被控制成相同的变量有过氧化氢溶液的浓度、
(3)依据实验1的数据可推知MnO2催化过氧化氢分解的速率大于FeCl3,其证据是
实验2:继续探究FeCl3质量对过氧化氢分解速率的影响。
【进行实验】如下表所示,在锥形瓶中放入FeCl3,用注射器推入5% 过氧化氢溶液,记录实验数据。
| 序号 | FeCl3质量 | 过氧化氢溶液体积 | 过氧化氢完全分解所用时间 |
| 2-1 | 0.03g | 3 mL | 61s |
| 2-2 | 0.04g | 3 mL | 56s |
| 2-3 | 0.05g | 3 mL | 49s |
(4)由实验2可得结论:过氧化氢溶液体积等条件相同时,FeCl3质量在0.03~0.05g范围内,
【反思与评价】
(5)实验小组用1-2的方案制备氧气,发现反应速率偏慢。根据上述实验结论,你认为可采取的改进措施有
您最近一年使用:0次
科学探究题
|
较难
(0.4)
【推荐2】某学习小组对铁锈蚀进行探究。
【提出问题】铁锈蚀与哪些因素有关?
【查阅资料】
(1)氯化钙固体可作干燥剂。
(2)一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
(3)常温常压,氢气密度是dg/mL。
【设计与实验】
实验一:定性探究铁锈蚀的因素
取四枚相同的洁净无锈铁钉分别放入试管,进行图1实验,现象如表。
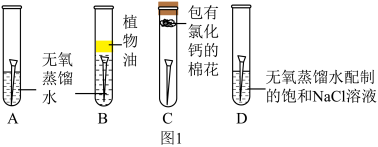
(1)对比A、B、C试管中实验现象,说明铁锈蚀主要是与空气中的______ 发生化学反应。
(2)对比A、D试管中实验现象,说明铁锈蚀还与______ 有关。
(3)铁锈蚀后应及时除锈的原因是______ ,写出除铁锈的化学方程式______ 。
实验二:定量探究铁锈蚀的因素
小组设计了如图装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,t1时刻加入2mL饱和NaCl溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上,采集数据。
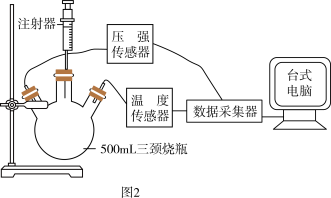
(4)据图,t2时刻后反应并未停止温度却开始降低,原因是______ 。
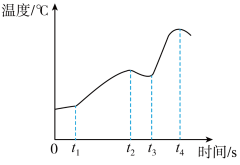
(5)据图,对比AB段和BC段说明______ 分析t3时刻压强突然变大的原因是______ 。
实验三:测定铁锈含量
将实验二烧瓶中剩余物质过滤、洗涤、干燥,得mg固体,连接如图装置,检查气密性,加入固体与足量稀盐酸进行实验。
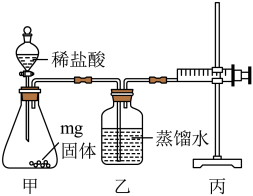
(6)完全反应后,常温常压下测得生成气体体积为VmL,则该固体中铁锈质量分数表达式为______ 。
(7)该实验条件下测得铁锈质量分数偏小的原因是______ ,解决方法是______ 。
【反思与评价】
(8)与实验一对比,实验二铁锈蚀明显更快的原因是______ 。
【提出问题】铁锈蚀与哪些因素有关?
【查阅资料】
(1)氯化钙固体可作干燥剂。
(2)一定条件下,碳可加快铁的锈蚀,但碳本身不参加反应。
(3)常温常压,氢气密度是dg/mL。
【设计与实验】
实验一:定性探究铁锈蚀的因素
取四枚相同的洁净无锈铁钉分别放入试管,进行图1实验,现象如表。

| 试管 | 一周后现象 |
| A | 铁钉表面有一层铁锈 |
| B | 铁钉表面无明显变化 |
| C | 铁钉表面无明显变化 |
| D | 铁钉表面有较厚铁锈 |
(2)对比A、D试管中实验现象,说明铁锈蚀还与
(3)铁锈蚀后应及时除锈的原因是
实验二:定量探究铁锈蚀的因素
小组设计了如图装置,检查气密性,将5g铁粉和2g碳粉加入三颈烧瓶,t1时刻加入2mL饱和NaCl溶液后,再将一只装有5mL稀盐酸的注射器插到烧瓶上,采集数据。

(4)据图,t2时刻后反应并未停止温度却开始降低,原因是

(5)据图,对比AB段和BC段说明

实验三:测定铁锈含量
将实验二烧瓶中剩余物质过滤、洗涤、干燥,得mg固体,连接如图装置,检查气密性,加入固体与足量稀盐酸进行实验。

(6)完全反应后,常温常压下测得生成气体体积为VmL,则该固体中铁锈质量分数表达式为
(7)该实验条件下测得铁锈质量分数偏小的原因是
【反思与评价】
(8)与实验一对比,实验二铁锈蚀明显更快的原因是
您最近一年使用:0次
科学探究题
|
较难
(0.4)
名校
解题方法
【推荐3】鱼浮灵【主要成分是过碳酸钠(2Na2CO3·3H2O2)】是水产养殖中常见的增氧剂,溶于水后生成Na2CO3和H2O2,能迅速增加水体溶氧量,某课外小组用如图装置探究促进H2O2分解的因素。
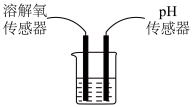
【查阅资料】H2O2常温下分解很慢。
NaCl溶于水解离出Na+和Cl-。
Na2CO3溶于水解离出Na+和CO32-,CO32-与水作用使溶液呈碱性。
【猜想与假设】①.Na+促进H2O2分解。②.溶液的碱性促进H2O2分解。
【进行实验】
探究一:分别进行下列3个实验(80mL蒸馏水中加入6.7g“鱼浮灵”,所得溶液中H2O2的浓度约为4%)。
【解释与结论】
(1)根据实验1的实验结果,加入“鱼浮灵”后,液体的变化是______ 。
(2)通过实验______ ,证明猜想1不成立。
(3)证明猜想2成立的依据是______ 。
探究二:向5个烧杯中分别加入80mL4%的H2O2溶液,再分别滴加NaOH溶液,测得不同pH下的溶解氧情况如下表所示。
(4)探究二得出的结论是______ 。
【反思与评价】
(5)下列物质能加快H2O2分解的是_______ 。
A MnO2 B NaCl C NaOH D Na2CO3
(6)探究一中,实验2-①与实验1-①对比,溶解氧增大的原因是______ 。

【查阅资料】H2O2常温下分解很慢。
NaCl溶于水解离出Na+和Cl-。
Na2CO3溶于水解离出Na+和CO32-,CO32-与水作用使溶液呈碱性。
【猜想与假设】①.Na+促进H2O2分解。②.溶液的碱性促进H2O2分解。
【进行实验】
探究一:分别进行下列3个实验(80mL蒸馏水中加入6.7g“鱼浮灵”,所得溶液中H2O2的浓度约为4%)。
| 实验 | 实验内容 | 实验结果 | |
| pH | 溶解氧(mg/L) | ||
| 1 | ① 80 mL蒸馏水 | 6.96 | 5.68 |
| ② 加“鱼浮灵”6.7g | 9.89 | 7.97 | |
| 2 | ① 80 mL 4%的H2O2溶液 | 6.01 | 6.44 |
| ② 加少量NaCl | 6.00 | 6.46 | |
| ③ 再加少量Na2CO3 | 8.14 | 9.11 | |
| 3 | 80 mL 4%的H2O2溶液中加少量NaOH溶液 | 9.26 | 10.97 |
【解释与结论】
(1)根据实验1的实验结果,加入“鱼浮灵”后,液体的变化是
(2)通过实验
(3)证明猜想2成立的依据是
探究二:向5个烧杯中分别加入80mL4%的H2O2溶液,再分别滴加NaOH溶液,测得不同pH下的溶解氧情况如下表所示。
| 烧杯 | 1 | 2 | 3 | 4 | 5 |
| pH | 8.00 | 8.59 | 9.29 | 10.43 | 11.47 |
| 溶解氧(mg/L) | 6.88 | 9.30 | 13.82 | 17.57 | 13.15 |
(4)探究二得出的结论是
【反思与评价】
(5)下列物质能加快H2O2分解的是
A MnO2 B NaCl C NaOH D Na2CO3
(6)探究一中,实验2-①与实验1-①对比,溶解氧增大的原因是
您最近一年使用:0次



