验证某混合气体含有CO和H2,并除去含有的少量CO2杂质。甲同学进行了如下实验:

(1)A中氢氧化钠溶液的作用是_____ ,B中浓硫酸的作用是吸收水分,观察到C中黑色氧化铜变_____ ,D中澄清石灰水变浑浊,写出D中反应的化学方程式_____ 。
(2)乙同学认为上述实验现象不能确定混合气体含有H2,他改进实验后证明了混合气体中含有H2.请写出乙同学的实验改进方法和现象_____ 。从环境保护角度,该实验中最后导出的尾气处理方法是_____ 。
(3)丙同学对A装置反应后的溶液成分进行验证,请根据实验现象填写下列空白处:
若将Ⅱ中加入的溶液换成_____ (写化学式),也可得出Ⅱ中相同的结论。写出相应的化学方程式为:_____ 。

(1)A中氢氧化钠溶液的作用是
(2)乙同学认为上述实验现象不能确定混合气体含有H2,他改进实验后证明了混合气体中含有H2.请写出乙同学的实验改进方法和现象
(3)丙同学对A装置反应后的溶液成分进行验证,请根据实验现象填写下列空白处:
| 实验操作过程 | 实验现象 | 实验结论 |
| Ⅰ.取待测液少量于试管中,向其中滴加适量溶液 | 产生白色沉淀 | 溶液中含Na2CO3 |
| Ⅱ.将上述反应后的混合物静置后,再向上层清液中加入溶液。 | 溶液呈红色 | 溶液中含NaOH |
若将Ⅱ中加入的溶液换成
2014·上海松江·中考模拟 查看更多[4]
更新时间:2016-11-28 12:03:10
|
相似题推荐
实验题
|
困难
(0.15)
解题方法
【推荐1】下图所示为实验室中常见气体制备、净化、干燥、收集和进行实验探究的部分仪器(组装实验装置时,可重复选择仪器),某化学小组的同学利用其进行下列化学实验。

试根据题目要求,回答下列问题:
(1)以锌和稀盐酸为原料,在实验室中制备并收集干燥、纯净的氢气。按照要求设计实验装置,连接仪器,检查装置的气密性,进行实验。
①所选仪器的连接顺序为______ (从左到右填写仪器序号字母)。
②上述方法制取氢气的化学方程式为______ 。
③下列有关氢气制取和性质的叙述中,不正确的是______ (填选项序号之一)。
A.氢气难溶于水且不与水反应,也可以用排水法收集
B.点燃氢气前,一定要注意先检验氢气的纯度
C.锌和稀盐酸充分反应后,溶液的pH减小
D.纯净的氢气在空气中燃烧,火焰呈淡蓝色
(2)以过氧化氢溶液为原料(MnO2为催化剂)在实验室中制取氧气,并测定某塑料(CxHy)试样的元素组成比例,所选仪器按“C→B1→D→B2→A→碱石灰干燥管”的顺序连接(B1、B2为浓硫酸洗气瓶),检验装置的气密性,然后进行实验。使一定质量的该塑料试样碎屑在充足氧气中充分燃烧,观察现象,收集有关实验数据。(假设所发生的化学反应都充分反应)
①在该装置中,洗气瓶B2的作用为______ 。
②装置C锥形瓶中液体里出现的现象之一为______ 。
③该塑料试样充分燃烧后,测得仪器B2质量增加1.8g,仪器A质量增加4.4g,则该塑料试样(CxHy)中x:y=______ (填写最简整数比)。
(3)用一氧化碳气体测定某铜粉样品(含少量氧化铜杂质)的纯度。所选装置按CO→D→E”的顺序连接(实验前检验装置的气密性)。
①在该装置中,仪器E的作用为______ 。
②仪器D的大玻璃管中放入铜粉样品的质量为mg,若经过充分反应,测得反应后仪器D的质量减少ag,则该铜粉样品中单质铜的质量是______ g(结果用含字母的代数式表示)。
③某同学选用另外一种试剂自选装置进行实验,也测定出了该铜粉样品(含少量氧化铜杂质)的纯度。该试剂不可能是______ (填选项序号之一)。
A.H2 B.O2 C.稀盐酸 D.NaOH溶液

试根据题目要求,回答下列问题:
(1)以锌和稀盐酸为原料,在实验室中制备并收集干燥、纯净的氢气。按照要求设计实验装置,连接仪器,检查装置的气密性,进行实验。
①所选仪器的连接顺序为
②上述方法制取氢气的化学方程式为
③下列有关氢气制取和性质的叙述中,不正确的是
A.氢气难溶于水且不与水反应,也可以用排水法收集
B.点燃氢气前,一定要注意先检验氢气的纯度
C.锌和稀盐酸充分反应后,溶液的pH减小
D.纯净的氢气在空气中燃烧,火焰呈淡蓝色
(2)以过氧化氢溶液为原料(MnO2为催化剂)在实验室中制取氧气,并测定某塑料(CxHy)试样的元素组成比例,所选仪器按“C→B1→D→B2→A→碱石灰干燥管”的顺序连接(B1、B2为浓硫酸洗气瓶),检验装置的气密性,然后进行实验。使一定质量的该塑料试样碎屑在充足氧气中充分燃烧,观察现象,收集有关实验数据。(假设所发生的化学反应都充分反应)
①在该装置中,洗气瓶B2的作用为
②装置C锥形瓶中液体里出现的现象之一为
③该塑料试样充分燃烧后,测得仪器B2质量增加1.8g,仪器A质量增加4.4g,则该塑料试样(CxHy)中x:y=
(3)用一氧化碳气体测定某铜粉样品(含少量氧化铜杂质)的纯度。所选装置按CO→D→E”的顺序连接(实验前检验装置的气密性)。
①在该装置中,仪器E的作用为
②仪器D的大玻璃管中放入铜粉样品的质量为mg,若经过充分反应,测得反应后仪器D的质量减少ag,则该铜粉样品中单质铜的质量是
③某同学选用另外一种试剂自选装置进行实验,也测定出了该铜粉样品(含少量氧化铜杂质)的纯度。该试剂不可能是
A.H2 B.O2 C.稀盐酸 D.NaOH溶液
您最近一年使用:0次
实验题
|
困难
(0.15)
名校
【推荐2】长郡双语九年级“我们爱化学”活动小组的同学,在探究木炭与CuO反应时,完成了如图实验,请回答下列问题:

如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)实验结束时,应________ (填写下列操作代号)。
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
小组中小双同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:

已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
(2)仪器B中所盛试剂为________ ,其作用为检验二氧化碳。
(3)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有:__________ 。
(4)实验前,需检查装置__________ ;点燃酒精灯前,先打开K,通入N2一段时间,其作用为__________ 。
(5)请指出上述实验中的一项缺陷________ 。
(6)将1.44g木炭和16.0g CuO在较高温度下反应生成Cu,理论上可生成CO2______ g。
小组中吴华同学通过查阅资料发现:Cu2O为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。
(7)请设计简单实验验证CuO和足量木炭反应后所得的红色固体中是否有Cu2O:_____ 。

如图所示装置进行实验,很快发现澄清的石灰水变浑浊;
(1)实验结束时,应
①先撤出导管,再熄灭酒精灯
②先熄灭酒精灯,再撤出导管
小组中小双同学通过仔细阅读教材,认为当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,小组的同学们在老师指导下设计实验进行了验证:

已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
(2)仪器B中所盛试剂为
(3)D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有:
(4)实验前,需检查装置
(5)请指出上述实验中的一项缺陷
(6)将1.44g木炭和16.0g CuO在较高温度下反应生成Cu,理论上可生成CO2
小组中吴华同学通过查阅资料发现:Cu2O为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。
(7)请设计简单实验验证CuO和足量木炭反应后所得的红色固体中是否有Cu2O:
您最近一年使用:0次
实验题
|
困难
(0.15)
名校
【推荐3】某气体可能含有CO2、CO、H2中的一种或几种,某化学小组的同学们为确定气体成分。设计如图所示装置并进行实验(夹持装置已省略)。
查阅资料:浓硫酸有吸水性,无水硫酸铜吸水后变蓝,氢氧化钠固体能吸收水和二氧化碳。

实验过程中,观察到A中溶液变浑浊,C中固体由黑色变红色,D中固体由白色变蓝色。反应前后分别对C、D装置进行了称量,结果如表所示:
回答下列问题:
(1)A装置的作用是:______ ;
(2)从环保角度分析。该装置还需要进行的改进是______ ;
(3)若没有装置B,对实验的影响是:______ ;
(4)分析上述现象得出结论:C中一定发生反应的化学方程式为:______ ;
(5)小明同学测得反应后E装置质量增加。由此得出结论:原气体中一定含有CO。小聪不同意他的观点,理由是:______ ;
(6)对于无法确定的气体成分,同学们利用表中数据进行分析。能证明该气体存在的关系式是:______ 。
查阅资料:浓硫酸有吸水性,无水硫酸铜吸水后变蓝,氢氧化钠固体能吸收水和二氧化碳。

实验过程中,观察到A中溶液变浑浊,C中固体由黑色变红色,D中固体由白色变蓝色。反应前后分别对C、D装置进行了称量,结果如表所示:
| 反应前 | 反应后 | |
| C装置中玻璃管与固体总质量(g) | a | b |
| D装置中U形管与固体总质量(g) | c | d |
(1)A装置的作用是:
(2)从环保角度分析。该装置还需要进行的改进是
(3)若没有装置B,对实验的影响是:
(4)分析上述现象得出结论:C中一定发生反应的化学方程式为:
(5)小明同学测得反应后E装置质量增加。由此得出结论:原气体中一定含有CO。小聪不同意他的观点,理由是:
(6)对于无法确定的气体成分,同学们利用表中数据进行分析。能证明该气体存在的关系式是:
您最近一年使用:0次
实验题
|
困难
(0.15)
【推荐1】化学兴趣小组制备Fe(OH)2,并进行相关探究。
资料摘要I、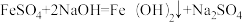 。
。
Ⅱ、Fe(OH)2是白色难溶物质,Fe(OH)3是红褐色难溶物质。
〖实验1〗
(1)同学们按图甲、图乙所示进行实验。写出图甲反应的现象______ 。
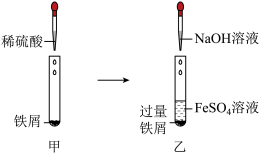
(2)观察到图乙试管内有白色沉淀生成,一会儿变为红褐色。重复上述实验后迅速塞紧橡皮塞(如图丙所示),并测得实验数据如图丁、图戊所示。
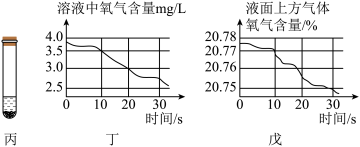
据此可知:沉淀颜色的改变与氧气有关。其依据是______ 。
〖实验2〗老师对实验进行改进(如图所示),可使制备的Fe(OH)2能较长时间保持白色。具体实验步骤如下:
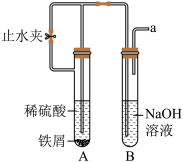
①检查装置气密性:
②往A、B试管中加入试剂,打开止水夹,塞紧橡皮塞:
③检验B试管中排出H2的纯度:
④当排出的H2纯净时,进行操作X,使A试管的液体进入B试管中,观察到B试管内有白色沉淀产生。
(3)步骤①的具体做法:组装好仪器后,在a处连接注射器,______ (填操作),出现______ ,则该装置气密性良好。
(4)为达到实验目的,在步骤②中加入的液体试剂需先加热处理,其作用是______ 。
(5)步骤④中操作X为______ 。
〖实验3〗
同学们用以下实验仪器和试剂对实验1进行改进,制得Fe(OH)2也能较长时间保持白色。
仪器:试管、胶头滴管(或注射器)
试剂:铁屑、热处理后的稀硫酸和氢氧化钠溶液、植物油
(6)实验改进方案:往装有过量铁屑的试管中加入稀硫酸,待反应完全后,先滴入植物油,再______ 。铁屑用过量的目的是:______ 。
资料摘要I、
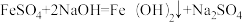 。
。Ⅱ、Fe(OH)2是白色难溶物质,Fe(OH)3是红褐色难溶物质。
〖实验1〗
(1)同学们按图甲、图乙所示进行实验。写出图甲反应的现象

(2)观察到图乙试管内有白色沉淀生成,一会儿变为红褐色。重复上述实验后迅速塞紧橡皮塞(如图丙所示),并测得实验数据如图丁、图戊所示。

据此可知:沉淀颜色的改变与氧气有关。其依据是
〖实验2〗老师对实验进行改进(如图所示),可使制备的Fe(OH)2能较长时间保持白色。具体实验步骤如下:

①检查装置气密性:
②往A、B试管中加入试剂,打开止水夹,塞紧橡皮塞:
③检验B试管中排出H2的纯度:
④当排出的H2纯净时,进行操作X,使A试管的液体进入B试管中,观察到B试管内有白色沉淀产生。
(3)步骤①的具体做法:组装好仪器后,在a处连接注射器,
(4)为达到实验目的,在步骤②中加入的液体试剂需先加热处理,其作用是
(5)步骤④中操作X为
〖实验3〗
同学们用以下实验仪器和试剂对实验1进行改进,制得Fe(OH)2也能较长时间保持白色。
仪器:试管、胶头滴管(或注射器)
试剂:铁屑、热处理后的稀硫酸和氢氧化钠溶液、植物油
(6)实验改进方案:往装有过量铁屑的试管中加入稀硫酸,待反应完全后,先滴入植物油,再
您最近一年使用:0次
实验题
|
困难
(0.15)
【推荐2】小红学碱的性质时做了如图两个实验,并把两个实验的滤液都倒入了一个烧杯中,结果烧杯中产生了少量气泡,最终还有白色沉淀生成。回答下列问题:

(1)实验①中酚酞溶液的作用___________________ 。
(2)实验②中滤液的溶质除有氢氧化钠外,还有________________ (填化学式)。
(3)烧杯中产生白色沉淀物的化学方程式____________ 。
(4)小红对烧杯中的溶质的成分进行探究:小红认为除有NaCl外,还可能含有:
猜想1:还可能含有CaCl2
猜想2: 还可能含有___________ ,为了验证猜想1提出方案如下:

(1)实验①中酚酞溶液的作用
(2)实验②中滤液的溶质除有氢氧化钠外,还有
(3)烧杯中产生白色沉淀物的化学方程式
(4)小红对烧杯中的溶质的成分进行探究:小红认为除有NaCl外,还可能含有:
猜想1:还可能含有CaCl2
猜想2: 还可能含有
| 实验操作 | 实验现象 | 实验结论 |
| 取烧杯中的少量滤液于试管中,加入Na2CO3溶液 | 猜想1正确 |
您最近一年使用:0次
实验题
|
困难
(0.15)
【推荐3】实验是实现科学探究的重要途径。请回答以下有关化学实验的问题。
(1)下列实验操作中正确的是____________ (填序号)。
A.用玻璃棒搅拌加快过滤
B.用镊子取用二氧化锰
C.用量筒量取液体时最后改用胶头滴管加至刻度
D.实验室模拟炼铁时先加热氧化铁再通入一氧化碳
(2)如图1是实验室制取和收集气体的装置,请回答:


①写出实验室用A装置制取氧气的化学方程式:_____________________________ 。
②用B装置制取气体并能随时停止反应,上部与下部对接应选____________ (填“a”或“b”)。
③用装置E排空气收集H2,气体应从导管的___________ (填“c”或“d”)端进入。
④从装置A~E中选择:加热氢氧化钙和氯化铵的固体混合物制取氨气并用排空气法收集,应选用图中的____ (填字母)。
(3)在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图2所示的装置(夹持仪器已略去),引起同学们的兴趣。请回答问题:
①打开活塞K,整个装置中会出现什么现象?_______________
②写出装置③中发生反应的化学方程式。__________________
(4)工业上电解食盐水可制得烧碱,同时得到氯气和最轻的气体.若将20 t溶质质量分数为23.4%的氯化钠溶液完全电解,可得烧碱多少吨_____________ ?
(1)下列实验操作中正确的是
A.用玻璃棒搅拌加快过滤
B.用镊子取用二氧化锰
C.用量筒量取液体时最后改用胶头滴管加至刻度
D.实验室模拟炼铁时先加热氧化铁再通入一氧化碳
(2)如图1是实验室制取和收集气体的装置,请回答:


①写出实验室用A装置制取氧气的化学方程式:
②用B装置制取气体并能随时停止反应,上部与下部对接应选
③用装置E排空气收集H2,气体应从导管的
④从装置A~E中选择:加热氢氧化钙和氯化铵的固体混合物制取氨气并用排空气法收集,应选用图中的
(3)在“创新实验装置”的竞赛中,某化学兴趣小组设计了如图2所示的装置(夹持仪器已略去),引起同学们的兴趣。请回答问题:
①打开活塞K,整个装置中会出现什么现象?
②写出装置③中发生反应的化学方程式。
(4)工业上电解食盐水可制得烧碱,同时得到氯气和最轻的气体.若将20 t溶质质量分数为23.4%的氯化钠溶液完全电解,可得烧碱多少吨
您最近一年使用:0次
实验题
|
困难
(0.15)
【推荐1】铁和铁的化合物在工农业生产中有广泛的应用。铁的冶炼和探究。取24.0g Fe2O3粉末,小组同学用如图装置模拟炼铁,并测定反应后固体成分。

资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先______________ ,再装入药品。
(2)实验时先通入CO,目的是_____________ 。
(3)①控制A中温度在700℃至固体全部 变黑,继续通CO至冷却。目的是除了防止生成的Fe被氧化外还有_______________ 。
②通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是_____________ 。
③现直接测得装置A中剩余固体质量为19.2g。则装置B中固体应增重_______ g。
(4)经分析A中剩余固体19.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4充分反应,得H2 0.3g。
①固体中Fe质量为________ g。
②FexOy的化学式为________ 。

资料:碱石灰可吸收H2O和CO2。
(1)连接装置,先
(2)实验时先通入CO,目的是
(3)①控制A中温度在700℃至固体
②通过测定装置B中固体的质量变化,可准确求得装置A中剩余固体质量。装置C的作用是
③现直接测得装置A中剩余固体质量为19.2g。则装置B中固体应增重
(4)经分析A中剩余固体19.2g为Fe和FexOy的混合物,向其中加入足量的稀H2SO4充分反应,得H2 0.3g。
①固体中Fe质量为
②FexOy的化学式为
您最近一年使用:0次
实验题
|
困难
(0.15)
【推荐2】研究性学习小组对教材实验结论“葡萄糖与新制氢氧化铜反应生成的红色沉淀是氧化亚铜(Cu2O)”。提出质疑,他们认为红色沉淀不一定全是氧化亚铜。为了确定红色沉淀的成分,开展了如下研究:
提出猜想:红色沉淀可能是①Cu2O ②Cu2O和 Cu
查阅资料:①氨气与氧化亚铜可以发生如下反应∶2NH3+3Cu2O N2+6Cu+3H2O
N2+6Cu+3H2O
②浓氨水与固体CaO接触,会逸出大量氨气、碱石灰是氧化钙和氢氧化钠的混合物可吸收水和二氧化碳
设计方案:装置如下图所示,实验步骤如下:
①连好装置,检查装置气密性
②准确称取28.8克的红色沉淀于玻璃管中,
③先A处反应,通一段时间氨气后称量D质量为108.3克
④加热装置C
⑤待D中恒重为111.9克时,停止加热,继续通氨气直到装置C冷却。

(1)A处为用浓氨水与固体CaO接触,以产生稳定持续的氨气则A处的发生装置应选______ (填“甲”,“乙”或“丙”)。

(2)B中碱石灰的作用是______ ,停止加热,继续通氨气的作用为______
(3)写出D中发生的化学方程式______ 。
(4)为防止未反应的氨气扩散到空气中E处可以连接的装置为(液体均为稀硫酸,下列选项中选择)______

(5)红色沉淀的成分为______ (列式计算说明)。
提出猜想:红色沉淀可能是①Cu2O ②Cu2O和 Cu
查阅资料:①氨气与氧化亚铜可以发生如下反应∶2NH3+3Cu2O
 N2+6Cu+3H2O
N2+6Cu+3H2O②浓氨水与固体CaO接触,会逸出大量氨气、碱石灰是氧化钙和氢氧化钠的混合物可吸收水和二氧化碳
设计方案:装置如下图所示,实验步骤如下:
①连好装置,检查装置气密性
②准确称取28.8克的红色沉淀于玻璃管中,
③先A处反应,通一段时间氨气后称量D质量为108.3克
④加热装置C
⑤待D中恒重为111.9克时,停止加热,继续通氨气直到装置C冷却。

(1)A处为用浓氨水与固体CaO接触,以产生稳定持续的氨气则A处的发生装置应选

(2)B中碱石灰的作用是
(3)写出D中发生的化学方程式
(4)为防止未反应的氨气扩散到空气中E处可以连接的装置为(液体均为稀硫酸,下列选项中选择)

(5)红色沉淀的成分为
您最近一年使用:0次
实验题
|
困难
(0.15)
名校
【推荐3】通过下列实验装置探究碳及其化合物的性质。

①装置A中反应的化学方程式为_____ 。
②装置B中氢氧化钠溶液的作用是_____ 。
③装置C中黑色固体变红色,其化学方程式为_____ 。
④下列对该实验的分析正确的是_____ (选填编号)。
I.给装置A中通入0.1mol二氧化碳,装置C中可生成0.2mol铜
II.装置C中固体减少的质量与装置D中增加的质量相等
III.实验结束时应先熄灭C处酒精灯
IV.反应结束后继续通入二氧化碳的目的是防止铜被氧化

①装置A中反应的化学方程式为
②装置B中氢氧化钠溶液的作用是
③装置C中黑色固体变红色,其化学方程式为
④下列对该实验的分析正确的是
I.给装置A中通入0.1mol二氧化碳,装置C中可生成0.2mol铜
II.装置C中固体减少的质量与装置D中增加的质量相等
III.实验结束时应先熄灭C处酒精灯
IV.反应结束后继续通入二氧化碳的目的是防止铜被氧化
您最近一年使用:0次



