氢气的开发利用是氢能研究的热点。
一、氢气的发现和制备
(1)1766年,英国科学家卡文迪许用铁与稀盐酸作用,制得了可燃性的H2,同时还得到了浅绿色的氯化亚铁溶液,写出该反应的符号表达式___________ 。
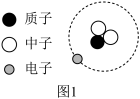
(2)目前制氢的方法主要有电解水制氢。电解水制氢中,使用氚进行核能发电,图1能表示氚的原子结构,氚属于___________ 元素的一种原子,氚原子的相对原子质量约为___________ 。
(3)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如图2:
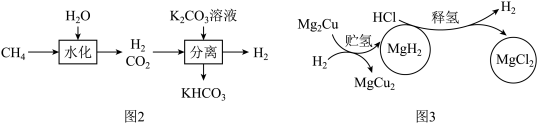
①“分离”时K2CO3溶液吸收CO2生成KHCO3,反应的符号表达式为___________ 。
②甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为___________ 。
二、氢气的贮存和释放
Mg2Cu可用于化学储氢,其贮氢与释氢过程如图3所示。
(4)贮氢反应需要在高温和隔绝空气的条件下进行,隔绝空气的原因___________ 。
(5)释氢释放的H2比贮氢吸收的H2___________ (选填“多”或“少”)
(6)释放出的氢气可用作氢燃料电池,氢燃料电池工作时将___________ 能转化为电能。
(7)2022年北京冬奥会火炬“飞扬”以氢气为燃料,氢气燃烧的符号表达式为___________ 。
三、氢气在工业生产中的应用
合成氨工艺需要用到氢气,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气。
(8)N2是合成氨的重要原料。工业上可从空气中获得N2,利用空气中各成分的___________ 不同将空气成分进行分离。
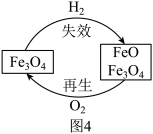
(9)Fe3O4是铁触媒的主要成分。合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图4所示。“再生”过程中铁元素的质量分数___________ (选填“变大”、“不变”或“变小”)。
(10)图5是Fe3O4在失效和再生过程中的质量与时间变化的关系图。

T1~T3时刻,是Fe3O4失效过程,T4~T5时刻,是固体再生过程。
则:A点处,固体中铁元素的质量=___________ g。
B点处,固体中含Fe3O4的质量为46.4g,则M=___________ g。
C点处,Fe3O4和FeO的质量比为___________ 。
一、氢气的发现和制备
(1)1766年,英国科学家卡文迪许用铁与稀盐酸作用,制得了可燃性的H2,同时还得到了浅绿色的氯化亚铁溶液,写出该反应的符号表达式
(2)目前制氢的方法主要有电解水制氢。电解水制氢中,使用氚进行核能发电,图1能表示氚的原子结构,氚属于

(3)甲烷和水蒸气催化重整是制高纯氢的方法之一,主要流程如图2:

①“分离”时K2CO3溶液吸收CO2生成KHCO3,反应的符号表达式为
②甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为
二、氢气的贮存和释放
Mg2Cu可用于化学储氢,其贮氢与释氢过程如图3所示。
(4)贮氢反应需要在高温和隔绝空气的条件下进行,隔绝空气的原因
(5)释氢释放的H2比贮氢吸收的H2
(6)释放出的氢气可用作氢燃料电池,氢燃料电池工作时将
(7)2022年北京冬奥会火炬“飞扬”以氢气为燃料,氢气燃烧的符号表达式为
三、氢气在工业生产中的应用
合成氨工艺需要用到氢气,在铁触媒作用下,用体积比为1:3的氮气和氢气合成氨气。
(8)N2是合成氨的重要原料。工业上可从空气中获得N2,利用空气中各成分的

(9)Fe3O4是铁触媒的主要成分。合成氨催化过程中因部分Fe3O4与H2反应使催化剂“失效”。在一定温度下可用O2将其“再生”,原理如图4所示。“再生”过程中铁元素的质量分数
(10)图5是Fe3O4在失效和再生过程中的质量与时间变化的关系图。

T1~T3时刻,是Fe3O4失效过程,T4~T5时刻,是固体再生过程。
则:A点处,固体中铁元素的质量=
B点处,固体中含Fe3O4的质量为46.4g,则M=
C点处,Fe3O4和FeO的质量比为
更新时间:2023-11-22 17:07:44
|
相似题推荐
综合应用题
|
困难
(0.15)
解题方法
【推荐1】草酸镍晶体(NiC2O4·2H2O)难溶于水,可用于制镍催化剂。
【探究一】
某小组用废镍催化剂(主要成分含有Ni,还含有少量的Al2O3、Fe)制备草酸镍晶体的部分实验流程如图1:____ 、____ 。
(2)“一系列操作”主要是为了除去溶液中铁元素对应的离子和___ (填写离子符号)等。
(3)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率(硫酸镍的产率)随时间变化如图2。从工业生产和能源利用率的角度分析,“酸浸”的最适宜温度与时间分别为 (单项选择)。
_____ ,“沉镍”后的滤液在农业中可用作_____ 。
【探究二】
对草酸镍晶体(NiC2O4·2H2O)进行热重分析,温度与TG%的关系如图3所示
【查阅资料】
①NiC2O4·2H2O加热至200℃左右完全失去结晶水,生成NiC2O4;继续加热,则剩余固体会受热分解生成镍的氧化物、CO2和CO。
②
(5)A点(TG=90.16)物质的化学式______ 。
(6)C点(TG=45.36)物质的化学式______ 。
【探究二】
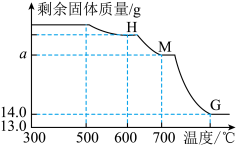
研究团队在模拟炼铁的过程中,对一定质量的氧化铁进行加热,通过精密仪器测定反应过程中固体质量的变化,曲线图如下:
【查阅资料】
用 CO还原Fe2O₃ 炼铁的过程大致分为三个阶段:
阶 段 1 :
阶 段 2:
阶 段 3:
(7)温度控制在300℃-500℃范围时,固体质量没有发生变化,原因是______ 。
(8)图中H点对应的固成分是____ 。
(9)图中M对应a的质量=____ 。
【探究一】
某小组用废镍催化剂(主要成分含有Ni,还含有少量的Al2O3、Fe)制备草酸镍晶体的部分实验流程如图1:
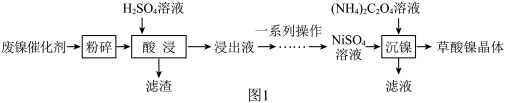
(2)“一系列操作”主要是为了除去溶液中铁元素对应的离子和
(3)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率(硫酸镍的产率)随时间变化如图2。从工业生产和能源利用率的角度分析,“酸浸”的最适宜温度与时间分别为 (单项选择)。
| A.30℃、30min | B.90℃、150min |
| C.70℃、120min | D.90℃、120min |
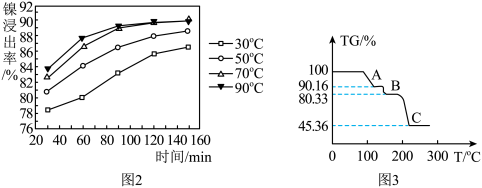
【探究二】
对草酸镍晶体(NiC2O4·2H2O)进行热重分析,温度与TG%的关系如图3所示
【查阅资料】
①NiC2O4·2H2O加热至200℃左右完全失去结晶水,生成NiC2O4;继续加热,则剩余固体会受热分解生成镍的氧化物、CO2和CO。
②

(5)A点(TG=90.16)物质的化学式
(6)C点(TG=45.36)物质的化学式
【探究二】
研究团队在模拟炼铁的过程中,对一定质量的氧化铁进行加热,通过精密仪器测定反应过程中固体质量的变化,曲线图如下:
【查阅资料】
用 CO还原Fe2O₃ 炼铁的过程大致分为三个阶段:
阶 段 1 :

阶 段 2:

阶 段 3:

(7)温度控制在300℃-500℃范围时,固体质量没有发生变化,原因是
(8)图中H点对应的固成分是
(9)图中M对应a的质量=

您最近一年使用:0次
综合应用题
|
困难
(0.15)
名校
【推荐2】铁及其化合物在生活生产中应用非常广泛。
(一)铁材料的有关知识

(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、 Al三种金属的活动性由强到弱的顺序是_______________ 。
(2)磁铁矿是早期司南(如图)的材料,磁铁矿中所含铁的氧化物主要是________________ 。
(3)我国C919大型客机去年惊艳亮相,客机上大规模使用碳纤维复合材料、铝锂合金、铁钛合金、纳米陶瓷等先进材料,其中不涉及到的材料是_________ (选填序号)。
A 合金
B 无机非金属材料
C 合成材料
D 复合材料
(4)铁矿石有赤铁矿、磁铁矿、黄铁矿(FeS2)等。工业上用黄铁矿制取硫酸而不用于炼铁,不用于炼铁原因是:①冶炼中产生SO2污染环境;②______________ 。
(二)制取碱式硫酸铁
碱式硫酸铁是-种废水处理剂,用硫酸厂的废渣(主要成分为铁的氧化物、少量FeS及SiO2)制备碱式硫酸铁晶体[Fe4(OH)2(SO4)5·6H2O]主要流程如下:

(1)废渣应研磨成粉末,目的是_____ 。
(2)“酸溶”过程中生成H2S气体的化学方程式为________
(3)过滤后洗涤,证明固体已洗净的方法是_______ 。
(4)“转化”发生反应的化学方程式为_______ ,该反应温度不宜过高的原因是________ 。
(三)碱式硫酸铁晶体的热分解实验
兴趣小组称取此晶体样品25.38g,在科研人员的指导下用下图装置进行热分解实验。

[查阅资料]①碱式硫酸铁晶体(相对分子质量为846)200°C完全分解生成Fe2O3、H2O和Fe2(SO4)3;
②Fe2(SO4)3在500°C完全分解为Fe2O3、SO2、SO3和O2;
③B装置中浓硫酸只能吸收SO3和H2O。.
(1)装配好实验装置后,先要_________ 。
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和______ 。
(3)控制不同的温度对A中固体加热,测得装置B、C和D中的质量变化如下表,测得剩余固体质量随温度的变化如图所示。

①如图中m1=____________ 。
②表格中x=_____________ 。
③将最终的剩余固体继续加热到更高的温度,发现固体减少0.32g后质量不再改变,写出此过程中发生反应的化学方程式____________ 。
(一)铁材料的有关知识

(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、 Al三种金属的活动性由强到弱的顺序是
(2)磁铁矿是早期司南(如图)的材料,磁铁矿中所含铁的氧化物主要是
(3)我国C919大型客机去年惊艳亮相,客机上大规模使用碳纤维复合材料、铝锂合金、铁钛合金、纳米陶瓷等先进材料,其中不涉及到的材料是
A 合金
B 无机非金属材料
C 合成材料
D 复合材料
(4)铁矿石有赤铁矿、磁铁矿、黄铁矿(FeS2)等。工业上用黄铁矿制取硫酸而不用于炼铁,不用于炼铁原因是:①冶炼中产生SO2污染环境;②
(二)制取碱式硫酸铁
碱式硫酸铁是-种废水处理剂,用硫酸厂的废渣(主要成分为铁的氧化物、少量FeS及SiO2)制备碱式硫酸铁晶体[Fe4(OH)2(SO4)5·6H2O]主要流程如下:

(1)废渣应研磨成粉末,目的是
(2)“酸溶”过程中生成H2S气体的化学方程式为
(3)过滤后洗涤,证明固体已洗净的方法是
(4)“转化”发生反应的化学方程式为
(三)碱式硫酸铁晶体的热分解实验
兴趣小组称取此晶体样品25.38g,在科研人员的指导下用下图装置进行热分解实验。

[查阅资料]①碱式硫酸铁晶体(相对分子质量为846)200°C完全分解生成Fe2O3、H2O和Fe2(SO4)3;
②Fe2(SO4)3在500°C完全分解为Fe2O3、SO2、SO3和O2;
③B装置中浓硫酸只能吸收SO3和H2O。.
(1)装配好实验装置后,先要
(2)加热前后及过程中均通入N2,停止加热后继续通N2的目的是防止倒吸和
(3)控制不同的温度对A中固体加热,测得装置B、C和D中的质量变化如下表,测得剩余固体质量随温度的变化如图所示。

| 温度/C | 室温 | 220 | 520 |
| B装置/g | 200.00 | 203.78 | 207.78 |
| C装置/g | 200.00 | 200.00 | x |
| D装置/g | 100.00 | 100.00 | 101.60 |
①如图中m1=
②表格中x=
③将最终的剩余固体继续加热到更高的温度,发现固体减少0.32g后质量不再改变,写出此过程中发生反应的化学方程式
您最近一年使用:0次
综合应用题
|
困难
(0.15)
名校
【推荐3】某水溶液中含有以下离子中的若干种:K+、Cl-、Ca2+、H+、CO32-、SO42-,现取两份溶液中各100ml,分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有溶液生成。根据上述实验,回答下列问题。
(1)写出第(2)步中生成沉淀的反应方程式:__________ 。
(2)根据第(1)(2)步实验操作判断原溶液中_______ (填“肯定有”或“肯定无”、“可能有”) CO32-和SO42-;
(3)原溶液中CO32-和SO42-的个数比为________
(4)原溶液中肯定没有的离子:__________ 。
(1)第一份加入AgNO3溶液有沉淀生成
(2)第二份加足量BaCl2溶液后,得沉淀物6.63g,经足量硝酸洗涤、干燥后,沉淀质量为4.66g;在所得滤液中加入AgNO3溶液有溶液生成。根据上述实验,回答下列问题。
(1)写出第(2)步中生成沉淀的反应方程式:
(2)根据第(1)(2)步实验操作判断原溶液中
(3)原溶液中CO32-和SO42-的个数比为
(4)原溶液中肯定没有的离子:
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐1】氢气是密度最小的无色气体,被认为是最清洁的燃料。
(1)氢气燃烧的化学方程式为_________________ ,氢能源没有大量使用是因为_________________ (写一条即可)。
(2)氢气能夺取金属氧化物中的氧,使其还原为金属,如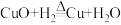 ,该实验可观察到的固体颜色由
,该实验可观察到的固体颜色由_________________ 。王峰同学根据氢气的还原性,在实验室用如图所示装置测定某赤铁矿中铁元素的质量分数,该赤铁矿中的主要成分是Fe2O3,还含有少量的FeO。C装置的硬质玻璃管中的固体物质是干燥的赤铁矿粉,旋钮a可以控制氢气的_________________ 。
(3)装置A中发生的化学反应方程式为_________________ 。
(4)装置B中试剂为_________________ 。

(5)若赤铁矿粉的质量为25 g,完全反应后,U型管E的质量增加了8.1 g。赤铁矿粉中铁元素的质量分数为_________________ 。
(6)反思与评价:U型管E右边连接干燥管F的目的是_________________ ,无干燥管F,则测得样品中铁的质量分数会_________________ (填“偏小”“不变”或“偏大”)。
(1)氢气燃烧的化学方程式为
(2)氢气能夺取金属氧化物中的氧,使其还原为金属,如
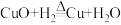 ,该实验可观察到的固体颜色由
,该实验可观察到的固体颜色由(3)装置A中发生的化学反应方程式为
(4)装置B中试剂为

(5)若赤铁矿粉的质量为25 g,完全反应后,U型管E的质量增加了8.1 g。赤铁矿粉中铁元素的质量分数为
(6)反思与评价:U型管E右边连接干燥管F的目的是
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐1】金属及其化合物在生产生活中有广泛的应用。
(一)金属的广泛应用
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、A1三种金属的活动性由强到弱的顺序是__________ 。
(2)现代高铁的机身采用铝合金材料,下列不属于该合金性质的是__________ (填字母)。
A 密度大
B 耐腐蚀
C 硬度大
(3)高铁路基中使用的钢筋混凝土属于__________ 材料(选填金属或复合)。高铁机身通过受电弓滑板与沿线架设高压电线相连,这是利用了受电滑板的__________ 性。(填“导电”或“导热”)
(4)在西汉有“曾青得铁化为铜”之说,用化学方程式表示其原理__________ 。
(二)铁及其化合物的实验
聚合硫酸铁(PFS)是一种新型的饮用水处理剂和净化剂、其化学组成可表示为【Fex(OH)y(SO4)z】m
聚合硫酸铁的工业生成是以回收废铁屑为原料制备、如下图:

(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为_____ ,“过筛”与化学实验中的__________ 原理相似(填操作名称)。
(2)写出废铁屑中铁与硫酸反应的化学反应方程式__________ 。
(3)与常压蒸发相比,减压蒸发的优点是__________ 。
A 有利于水分蒸发
B 降低沸点,防止晶体分解
C 降低生产成本
(三)聚合硫酸铁的成分探究。
(1)聚合硫酸铁的热分解气体产物成分探究。将5.52g聚合硫酸铁在一定条件下加热完全分解,对所得气体中除了产生水外还有哪些成分进行实验探究。(查阅资料:1.SO3在低于16.8℃时为固态。2.SO2能使品红溶液褪色)
【提出假设】①SO3②SO2、O2 ③____________ 。
【设计实验】

实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是___________ 。
【实验结论】通过实验现象判断,假设_________ 成立。
(2)研究小组为确定聚合硫酸铁的化学式,进行了如下实验:
①称取5.52g聚合硫酸铁样品溶于足量的稀盐酸中并充分混合;
②向①所得溶液中加足量BaCl2溶液,充分反应,经过滤、洗涤、干燥、称重,得沉淀4.66g。
③向步骤②的滤液中加过量NaOH溶液,充分反应,经过滤、洗涤、灼烧、称重,得固体3.20g。
实验步骤②中如何证明沉淀已洗净___________ 。
则聚合硫酸铁【Fex(OH)y(SO4)z】m样品中的x:y:z的值为___________ 。
(一)金属的广泛应用
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、A1三种金属的活动性由强到弱的顺序是
(2)现代高铁的机身采用铝合金材料,下列不属于该合金性质的是
A 密度大
B 耐腐蚀
C 硬度大
(3)高铁路基中使用的钢筋混凝土属于
(4)在西汉有“曾青得铁化为铜”之说,用化学方程式表示其原理
(二)铁及其化合物的实验
聚合硫酸铁(PFS)是一种新型的饮用水处理剂和净化剂、其化学组成可表示为【Fex(OH)y(SO4)z】m
聚合硫酸铁的工业生成是以回收废铁屑为原料制备、如下图:

(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为
(2)写出废铁屑中铁与硫酸反应的化学反应方程式
(3)与常压蒸发相比,减压蒸发的优点是
A 有利于水分蒸发
B 降低沸点,防止晶体分解
C 降低生产成本
(三)聚合硫酸铁的成分探究。
(1)聚合硫酸铁的热分解气体产物成分探究。将5.52g聚合硫酸铁在一定条件下加热完全分解,对所得气体中除了产生水外还有哪些成分进行实验探究。(查阅资料:1.SO3在低于16.8℃时为固态。2.SO2能使品红溶液褪色)
【提出假设】①SO3②SO2、O2 ③
【设计实验】

实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是
【实验结论】通过实验现象判断,假设
(2)研究小组为确定聚合硫酸铁的化学式,进行了如下实验:
①称取5.52g聚合硫酸铁样品溶于足量的稀盐酸中并充分混合;
②向①所得溶液中加足量BaCl2溶液,充分反应,经过滤、洗涤、干燥、称重,得沉淀4.66g。
③向步骤②的滤液中加过量NaOH溶液,充分反应,经过滤、洗涤、灼烧、称重,得固体3.20g。
实验步骤②中如何证明沉淀已洗净
则聚合硫酸铁【Fex(OH)y(SO4)z】m样品中的x:y:z的值为
您最近一年使用:0次
综合应用题
|
困难
(0.15)
真题
【推荐2】现有一种碱性调味液,是碳酸钠和氯化钠组成的溶液。为了测定碱性调味液中碳酸钠和氯化钠的质量分数,设计了如下实验方案。
【实验一】取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某盐酸中,测得三组实验数据见下表(气体的溶解忽略不计):
根据实验及有关数据进行分析与计算:
(1)100g碱性调味液与盐酸完全反应生成气体的质量为_________ g。
(2)碱性调味液中碳酸钠的质量分数为多少?(写出计算过程)
(3)100g碱性调味液与该盐酸反应后溶液pH=7时,需要盐酸的质量为__________ g。
【实验二】在上述第Ⅲ组反应后的溶液中加AgNO3溶液,测得实验数据见下图:

根据实验及有关数据进行分析:
(4)某同学计算出碱性调味液中氯化钠的质量分数为20.5%(保留到小数点后一位)后经检查无数字运算错误。请判断该计算结果是否正确,如不正确要指出错误原因。
【实验一】取三份碱性调味液各100g,分别缓慢加入到20g、40g和60g某盐酸中,测得三组实验数据见下表(气体的溶解忽略不计):
| 第I组 | 第Ⅱ组 | 第Ⅲ组 | |
| 盐酸的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 2.2 | 4.4 | 5.5 |
(1)100g碱性调味液与盐酸完全反应生成气体的质量为
(2)碱性调味液中碳酸钠的质量分数为多少?(写出计算过程)
(3)100g碱性调味液与该盐酸反应后溶液pH=7时,需要盐酸的质量为
【实验二】在上述第Ⅲ组反应后的溶液中加AgNO3溶液,测得实验数据见下图:

根据实验及有关数据进行分析:
(4)某同学计算出碱性调味液中氯化钠的质量分数为20.5%(保留到小数点后一位)后经检查无数字运算错误。请判断该计算结果是否正确,如不正确要指出错误原因。
您最近一年使用:0次
综合应用题
|
困难
(0.15)
【推荐3】铁及铁的化合物在生产、生活中有着极其广泛的应用。

(一)铁的广泛应用
(1)绿矾(FeSO4•7H2O)可用于制备Fe2O3、复印用Fe3O4粉、还原铁粉等,还可以制成药物,有利于防治________ 病。
(2)铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用钢筋和水泥为原料可制作钢筋混凝土材料。以上叙述中不涉及到 (选填序号)。
(3)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理______ 。
(二)生产复印用高档Fe3O4粉
工业上用绿矾制备高档Fe3O4粉,主要流程如下:
(4)写出反应①中加入适量NaOH溶液时发生的化学反应方程式________ 。
(5)副产品P的化学式是_____ 。由溶液N获得该副产品的操作顺序是b→_______ → ______ →d。
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
(6)检验沉淀已洗净的方法是:________ ,则沉淀已洗净。
(7)若制取Fe(OH)2,实验操作是:向盛有5ml新制FeSO4溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶O2),胶头滴管的正确使用方法是_____(填字母)。
(三)绿矾的热分解实验
兴趣小组称取绿矾固体5.56g,在科研人员的指导下用如图装置进行热分解实验。

【查阅资料】①FeSO4在t3℃时完全分解为铁的氧化物、SO2、SO3三种氧化物;
②将SO2气体通入BaCl2溶液无明显现象;
(8)加热前后均需通入N2,加热后通N2的目的是_________ 。
(9)控制温度在不同的范围对A中样品加热。测得剩余固体质量随温度的变化如右上图所示。当加热到t3℃时,称量装置C中产生沉淀的质量为m1g。

①装置D的作用是________ ,A处晶体的化学式为________ 。
②请写出绿矾加热到t3℃时受热分解的化学方程式___________ 。
③m1=________ g。

(一)铁的广泛应用
(1)绿矾(FeSO4•7H2O)可用于制备Fe2O3、复印用Fe3O4粉、还原铁粉等,还可以制成药物,有利于防治
(2)铁与铬(Cr)、镍(Ni)等金属熔合可形成“不锈钢”,用钢筋和水泥为原料可制作钢筋混凝土材料。以上叙述中不涉及到 (选填序号)。
| A.合金 | B.无机非金属材料 | C.合成材料 | D.复合材料 |
(3)我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理
(二)生产复印用高档Fe3O4粉
工业上用绿矾制备高档Fe3O4粉,主要流程如下:
(4)写出反应①中加入适量NaOH溶液时发生的化学反应方程式
(5)副产品P的化学式是
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
(6)检验沉淀已洗净的方法是:
(7)若制取Fe(OH)2,实验操作是:向盛有5ml新制FeSO4溶液的试管中加入10滴植物油,然后用胶头滴管加煮沸的NaOH溶液(驱赶O2),胶头滴管的正确使用方法是_____(填字母)。
A. | B.  | C.  | D. |
(三)绿矾的热分解实验
兴趣小组称取绿矾固体5.56g,在科研人员的指导下用如图装置进行热分解实验。

【查阅资料】①FeSO4在t3℃时完全分解为铁的氧化物、SO2、SO3三种氧化物;
②将SO2气体通入BaCl2溶液无明显现象;
(8)加热前后均需通入N2,加热后通N2的目的是
(9)控制温度在不同的范围对A中样品加热。测得剩余固体质量随温度的变化如右上图所示。当加热到t3℃时,称量装置C中产生沉淀的质量为m1g。

①装置D的作用是
②请写出绿矾加热到t3℃时受热分解的化学方程式
③m1=
您最近一年使用:0次




