下图是以空气等为原料合成化学肥料尿素[CO(NH2)2]的流程(部分产物略去)。
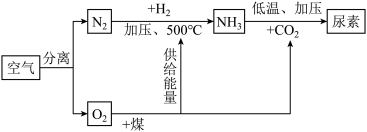
(1)合成氨是化学对社会发展和进步的巨大贡献之一,很大程度上解决了地球上因粮食不足而导致的饥饿问题。工业合成氨气(NH3)的原料是氮气和氢气,氮气可从空气中分离获得,工业上分离空气获得氮气的变化属于_______ (填“物理变化”或“化学变化”)。
(2)煤与氧气的反应_______ (填 “放出”或“吸收”)热量。
(3)N2与H2合成氨气(NH3)的反应符号表达式是_______ 。
(4)合成尿素的原料是_______ (填化学式)。尿素中氮元素的质量分数为_______ (精确到0.1%)。

(1)合成氨是化学对社会发展和进步的巨大贡献之一,很大程度上解决了地球上因粮食不足而导致的饥饿问题。工业合成氨气(NH3)的原料是氮气和氢气,氮气可从空气中分离获得,工业上分离空气获得氮气的变化属于
(2)煤与氧气的反应
(3)N2与H2合成氨气(NH3)的反应符号表达式是
(4)合成尿素的原料是
更新时间:2023-12-06 10:08:22
|
相似题推荐
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】甲酸(HCOOH)广泛用于轻工、医药等行业、甲酸钠法是最早工业化的甲酸生产工艺,主要流程如下图所示:

(1)甲酸钠(HCOONa)的组成元素中,属于金属元素的是______ 。
(2)图中所涉及的物质中,属于氧化物的是______ (写一种)。
(3)甲酸蒸馏塔中发生的是______ (填“物理”或“化学”)变化。

(1)甲酸钠(HCOONa)的组成元素中,属于金属元素的是
(2)图中所涉及的物质中,属于氧化物的是
(3)甲酸蒸馏塔中发生的是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】在化学、生产、生活等场境中都有重要用途的高锰酸钾是一种重要的化工产品。某地化工厂生产高锰酸钾的流程如下图所示,请完成下列问题:
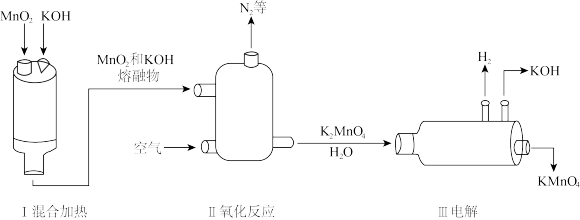
(1)写出用高锰酸钾制取氧气的化学方程式______ 。
(2)“I混合加热”发生的主要是______ (填“物理”或“化学”)变化。
(3)请将“Ⅱ氧化反应”发生反应的化学方程式补充完整(在横线上填化学式):______ + 2MnO2 + 4KOH=2K2MnO4 + 2______ 。
(4)“Ⅲ电解”反应中,反应前后化合价发生变化的元素有______ (写元素符号)。
(5)生产流程中可循环利用的物质是______ (写化学式)。

(1)写出用高锰酸钾制取氧气的化学方程式
(2)“I混合加热”发生的主要是
(3)请将“Ⅱ氧化反应”发生反应的化学方程式补充完整(在横线上填化学式):
(4)“Ⅲ电解”反应中,反应前后化合价发生变化的元素有
(5)生产流程中可循环利用的物质是
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下面的科普短文,回答相关问题
在通常情况下,甲醛(CH2O)是一种无色有刺激性气味的气体,易挥发。作为室内装修最常见的污染物,其具有潜在的致敏、致癌性。温度对甲醛的释放有较大影响,研究人员选取了部分装修后的住宅,测定了不同温度下室内甲醛浓度的变化,结果如表1:
表1不同温度下室内甲醛浓度变化
降低室内甲醛含量最简单有效的方法是开窗通风。利用活性炭可以吸附甲醛,该法是将甲醛从气态转化为固态存储,本质上并未改变其性质,因此当吸附接近饱和后,会有部分甲醛再次被释放,造成二次污染。采用化学降解法能彻底地去除甲醛,在甲醛催化分解材料的研究中,二氧化锰(MnO2)因其较高的低温催化活性和低毒、廉价等优势,而具有良好的应用前景。研究人员通过实验比较了不同形貌结构的MnO2 (茧状、海胆状、鸟巢状)对甲醛的去除效果,其结果如图。

(1)甲醛的化学式CH2O的微观意义是________ (写出1点即可),甲醛中碳元素的质量分数是________ 。
(2)利用活性炭可以吸附甲醛,说明活性炭具有________ 性。
(3)下列说法正确的是______。
(4)对比图中三条曲线,得到的结论是:在80~ 180℃的温度范围内,当温度相同时,________ 状MnO2去除甲醛效果最好。
在通常情况下,甲醛(CH2O)是一种无色有刺激性气味的气体,易挥发。作为室内装修最常见的污染物,其具有潜在的致敏、致癌性。温度对甲醛的释放有较大影响,研究人员选取了部分装修后的住宅,测定了不同温度下室内甲醛浓度的变化,结果如表1:
表1不同温度下室内甲醛浓度变化
| 温度/°C | ≤23 | 23~25 | 25~27 | ≥27 |
| 甲醛浓度增长率/% | 12.9 | 26.7 | 21.5 | 36.9 |

(1)甲醛的化学式CH2O的微观意义是
(2)利用活性炭可以吸附甲醛,说明活性炭具有
(3)下列说法正确的是______。
| A.由表1可知,甲醛浓度增长率随温度升高而增大 |
| B.利用活性炭吸附甲醛时,甲醛分子不改变 |
| C.在通常情况下,甲醛易挥发属于甲醛的物理性质 |
| D.采用活性炭吸附法能彻底地去除甲醛 |
(4)对比图中三条曲线,得到的结论是:在80~ 180℃的温度范围内,当温度相同时,
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】生活离不开化学,正确认识化学使你的生活更美好。
①人类赖以生存的空气中含量最多的气体是_________ 。(填化学式)
②生理盐水中溶质是_________ 。(填化学式)
③酸雨是指pH小于5.6的雨水。造成酸雨的主要气体是_________ 。(填物质名称)
④天然物质中最坚硬的物质是_________ 。(填物质名称)
⑤丁酸乙酯(C6H12O2)广泛应用于食用香精配方中,丁酸乙酯的摩尔质量为________ ;一个丁酸乙酯分子中有_____ 个原子,丁酸乙酯分子中碳、氢、氧原子的个数比为_____ ;丁酸乙酯中碳元素的质量分数为______ (结果保留至0.1%);11.6g丁酸乙酯的物质的量是______ ,含有________ 个丁酸乙酯分子。
①人类赖以生存的空气中含量最多的气体是
②生理盐水中溶质是
③酸雨是指pH小于5.6的雨水。造成酸雨的主要气体是
④天然物质中最坚硬的物质是
⑤丁酸乙酯(C6H12O2)广泛应用于食用香精配方中,丁酸乙酯的摩尔质量为
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】请认真阅读下列材料,然后回答下列问题:
材料一:2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因也是奶粉中含有三聚氰胺.在奶制品行业中,通常利用氮元素含量来衡量其中蛋白质的含量(合格奶粉含氮量在2.8%左右,蛋白质平均含氮量在16%).
材料二:三聚氰胺性状为纯白色单斜棱晶体,分子式C3N6H6,无味,密度1.573 g/cm3(16℃ ).常压熔点354℃(分解);快速加热升华,升华温度300℃.溶于热水,微溶于冷水,极微溶于热乙醇,不溶于醚、苯和四氯化碳,可溶于甲醇、甲醛、乙酸、热乙二醇、甘油、吡啶等.低毒.在一般情况下较稳定,但在高温下可能会分解放出氰化物.
(1)三聚氰胺分子式为C3N6H6,相对分子质量是_________ ,其中氮元素的质量分数为_____________ .三聚氰胺也被人称为“蛋白精”,价格便宜.牛奶和奶粉添加三聚氰胺,主要是因为它能冒充蛋白质.试解释三聚氰胺可以冒充蛋白质的原因:______________________ .
(2)为安全起见,一般采用三聚氰胺制造的食具都会标明“不可放进微波炉使用”.试解释相关原因:____________________ .
(3)一般只在奶粉中添加三聚氰胺,液体牛奶中一般不添加.尝试说出一点原因:_____________ .
(4)“食品安全无小事”由“三鹿婴幼儿奶粉受污染事件”,你对避免此类事件发生有何建议________________ .(答一点即可)
材料一:2008年9月,中国爆发三鹿婴幼儿奶粉受污染事件,导致食用了受污染奶粉的婴幼儿产生肾结石病症,其原因也是奶粉中含有三聚氰胺.在奶制品行业中,通常利用氮元素含量来衡量其中蛋白质的含量(合格奶粉含氮量在2.8%左右,蛋白质平均含氮量在16%).
材料二:三聚氰胺性状为纯白色单斜棱晶体,分子式C3N6H6,无味,密度1.573 g/cm3(16℃ ).常压熔点354℃(分解);快速加热升华,升华温度300℃.溶于热水,微溶于冷水,极微溶于热乙醇,不溶于醚、苯和四氯化碳,可溶于甲醇、甲醛、乙酸、热乙二醇、甘油、吡啶等.低毒.在一般情况下较稳定,但在高温下可能会分解放出氰化物.
(1)三聚氰胺分子式为C3N6H6,相对分子质量是
(2)为安全起见,一般采用三聚氰胺制造的食具都会标明“不可放进微波炉使用”.试解释相关原因:
(3)一般只在奶粉中添加三聚氰胺,液体牛奶中一般不添加.尝试说出一点原因:
(4)“食品安全无小事”由“三鹿婴幼儿奶粉受污染事件”,你对避免此类事件发生有何建议
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】工业上以空气、水等自然资源为原料合成碳酸氢铵的工艺流程图如图所示:

(1)步骤1是利用各成分的_______ 不同,通过冷却、加压、蒸馏将其分离。
(2)实验室中完成步骤④,玻璃棒作用是_______ 。
(3)步骤②涉及的化学反应基本类型为_______ 。
(4)写出合成碳酸氢铵NH4HCO3的化学方程式_______ 。

(1)步骤1是利用各成分的
(2)实验室中完成步骤④,玻璃棒作用是
(3)步骤②涉及的化学反应基本类型为
(4)写出合成碳酸氢铵NH4HCO3的化学方程式
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】2023年5月30日,神舟十六号载人飞船发射成功,航天员将在中国空间站完成各项任务,因此,保障航天员的氧气需求至关重要。那么,空间站的氧气从哪里来?
Ⅰ.从地球带下去
(1)实验室用高锰酸钾等原料制氧,写出高锰酸钾分解的化学方程式:____________ ;市售高锰酸钾每500克30元,航天工业需要大量的氧气,工业上选择空气为原料的主要原因是____________ 。
(2)工业上采用分离液态空气法获得氧气,其过程可用如下图所示实验模拟。

浸入液氮3min后,试管内产生约占其容积1/3的液态空气。取出试管,液态空气沸腾,伸入燃着的木条,木条熄灭;1min后伸入带火星的木条,观察到木条复燃。由实验现象可知氮气与氧气的沸点比较低的气体是______ 。
(3)利用分子筛可将氧分子从空气中“筛”出去,通过增压与减压的交替循环,实现氮气和氧气的分离,从而获得高浓度的氧气。原理示意图如下图:

①由此可知两种分子的大小:
______ (填“>”或“<”) 。
。
②用分子筛吸附氮气发生的是______ (填“物理”或“化学”)变化。
③分子筛对氮气的吸附能力与吸附塔内气体的______ 有关。
④分子筛______ (填“可以”或“不可以”)重复使用。
Ⅱ.在天宫制出来
(4)早期空间站利用过氧化钠( )制氧气,过氧化钠与
)制氧气,过氧化钠与 反应后生成碳酸钠(
反应后生成碳酸钠( )和
)和 ,写出反应方程式:
,写出反应方程式:____________ ,空间站内二氧化碳的主要来源是____________ 。
(5)空间站是一个相对封闭的场所,解决“气体从哪里来”的问题必然伴生着“气体往哪里去”的问题。为此,科学家设计了生物再生生命保障系统,实现了“水—氧—碳”的循环转化。下列叙述正确的是______。填序号)。
Ⅰ.从地球带下去
(1)实验室用高锰酸钾等原料制氧,写出高锰酸钾分解的化学方程式:
(2)工业上采用分离液态空气法获得氧气,其过程可用如下图所示实验模拟。

浸入液氮3min后,试管内产生约占其容积1/3的液态空气。取出试管,液态空气沸腾,伸入燃着的木条,木条熄灭;1min后伸入带火星的木条,观察到木条复燃。由实验现象可知氮气与氧气的沸点比较低的气体是
(3)利用分子筛可将氧分子从空气中“筛”出去,通过增压与减压的交替循环,实现氮气和氧气的分离,从而获得高浓度的氧气。原理示意图如下图:

①由此可知两种分子的大小:

 。
。②用分子筛吸附氮气发生的是
③分子筛对氮气的吸附能力与吸附塔内气体的
④分子筛
Ⅱ.在天宫制出来
(4)早期空间站利用过氧化钠(
 )制氧气,过氧化钠与
)制氧气,过氧化钠与 反应后生成碳酸钠(
反应后生成碳酸钠( )和
)和 ,写出反应方程式:
,写出反应方程式:(5)空间站是一个相对封闭的场所,解决“气体从哪里来”的问题必然伴生着“气体往哪里去”的问题。为此,科学家设计了生物再生生命保障系统,实现了“水—氧—碳”的循环转化。下列叙述正确的是______。填序号)。
| A.“水—氧—碳”的循环转化,减少了氧气的携带量,减轻了火箭和飞船的载重 |
| B.富含二氧化碳空气经过净化后送达植物舱,供植物光合作用;植物舱产生的富氧空气经空气净化后送到综合舱供人和动物呼吸,形成碳氧循环 |
| C.人体代谢产物中的水既有气态又有液态,设计系统时应考虑水的冷凝与净化 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】(1)在氧气、二氧化碳、水蒸气、氮气、氖气、空气六种气体中,选择填合适物质在下面空格中
①属于混合物的是___________
②可用于制造硝酸和氮肥的是________________
③能使澄清的石灰水变浑浊的是____________
④可用于医疗急救病人的是____________
⑤充入测电笔中可产生红光的是________________
(2)根据所学知识,完成下列填空:
①分离液态空气法制氧气:是利用氧气和氮气的_______ (沸点或者密度)不同进行分离的。
②做“铁燃烧”实验时,集气瓶底放水的目的是___________
③写出钠离子符号___________
①属于混合物的是
②可用于制造硝酸和氮肥的是
③能使澄清的石灰水变浑浊的是
④可用于医疗急救病人的是
⑤充入测电笔中可产生红光的是
(2)根据所学知识,完成下列填空:
①分离液态空气法制氧气:是利用氧气和氮气的
②做“铁燃烧”实验时,集气瓶底放水的目的是
③写出钠离子符号
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】认真阅读下列短文,回答有关问题。
煤被誉为“工业的粮食”“黑色金子”。煤燃烧可用于发电。煤燃烧过程中产生硫的氧化物可以生产出优质硫酸。煤灰(主要成分SiO2、Al2O3等)可以用来制造水泥等建筑材料,在煤灰里还可以提取出半导体材料——锗和镓。“煤氏三兄弟”是指无烟煤、烟煤、褐煤,它们的含碳量依次降低。无烟煤是一种很好的燃料,烧起来火力很强,发热量高,烟尘很少,燃烧后灰渣也不多。
(1)阅读材料可知,煤中一定含有的元素有___________ ;
(2)煤燃烧发电的能量转化是化学能转化为___________ ;
(3)无烟煤作为一种很好的燃料,原因是___________ (任写两点);
(4)我国蕴含有丰富的煤炭资源,你认为应如何开发利用___________ 。
煤被誉为“工业的粮食”“黑色金子”。煤燃烧可用于发电。煤燃烧过程中产生硫的氧化物可以生产出优质硫酸。煤灰(主要成分SiO2、Al2O3等)可以用来制造水泥等建筑材料,在煤灰里还可以提取出半导体材料——锗和镓。“煤氏三兄弟”是指无烟煤、烟煤、褐煤,它们的含碳量依次降低。无烟煤是一种很好的燃料,烧起来火力很强,发热量高,烟尘很少,燃烧后灰渣也不多。
(1)阅读材料可知,煤中一定含有的元素有
(2)煤燃烧发电的能量转化是化学能转化为
(3)无烟煤作为一种很好的燃料,原因是
(4)我国蕴含有丰富的煤炭资源,你认为应如何开发利用
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
名校
【推荐2】环境、能源、材料与人类的生活和社会经济发展密切相关。请回答:
Ⅰ.煤、石油等化石燃料的综合利用既节约了能源,又减少了污染。
(1)煤的干馏属于______________________ 变化, 干馏获得的焦炭可用于高炉炼铁,高炉内用赤铁矿炼铁反应的化学反应方程式____________________ 。
(2)煤的气化过程中,碳与水蒸气生成两种气体燃料,其中一种是单质,该单质是___________________ 。
Ⅱ金属材料、无机非金属材料以各自的特点满足着人类多方面的需要。
(1)一些地区采用太阳能电池供电。生产太阳能电池需要纯硅。工业上由粗硅生产纯硅的工艺流程如图所示:

①上述步骤中属于物理变化的是步骤_____________________ 。
②步骤Ⅲ发生了置换反应,写出反应的化学方程式:____________________ 。
③与太阳能电池能量转化不同,火力发电是将化石燃料燃烧产生的____________________ 能转化为电能。
(2)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是_____________________ 。
(3)沪通高铁预计在2020年通车,制造铁轨的材料是合金铝钢,主要原因是合金钢具有____________________ (要求回答一点)的优越性能:
(4)某同学在实验室进行了两个有关金属性质的实验:
实验一:硫酸铝溶液和铁粉混合
实验二:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验一和实验二的物质全部倒入同一烧杯中,发现烧杯内红色固体明显增多,原因是______________________ (用文字说明)。一段时间后过滤,向滤渣中滴加盐酸,结果没有气泡产生。那么,滤液中所含金属离子的情况可能是______________________ (填数字序号)
①A13+ ②A13+、Fe2+ ③A13+、Fe3+ ④Fe2+、Cu2+ ⑤A13+、 Fe2+、Cu2+
Ⅰ.煤、石油等化石燃料的综合利用既节约了能源,又减少了污染。
(1)煤的干馏属于
(2)煤的气化过程中,碳与水蒸气生成两种气体燃料,其中一种是单质,该单质是
Ⅱ金属材料、无机非金属材料以各自的特点满足着人类多方面的需要。
(1)一些地区采用太阳能电池供电。生产太阳能电池需要纯硅。工业上由粗硅生产纯硅的工艺流程如图所示:

①上述步骤中属于物理变化的是步骤
②步骤Ⅲ发生了置换反应,写出反应的化学方程式:
③与太阳能电池能量转化不同,火力发电是将化石燃料燃烧产生的
(2)考古工作者发现铁质的出土文物往往锈蚀严重,铁生锈的条件是
(3)沪通高铁预计在2020年通车,制造铁轨的材料是合金铝钢,主要原因是合金钢具有
(4)某同学在实验室进行了两个有关金属性质的实验:
实验一:硫酸铝溶液和铁粉混合
实验二:硫酸铜溶液与铁粉混合
在上述两个实验结束后,该同学将实验一和实验二的物质全部倒入同一烧杯中,发现烧杯内红色固体明显增多,原因是
①A13+ ②A13+、Fe2+ ③A13+、Fe3+ ④Fe2+、Cu2+ ⑤A13+、 Fe2+、Cu2+
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐3】太阳能电池已经广泛应用于交通、通讯、气象等领域,太阳能汽车是其中—个重要应用。请回答下列问题:

(1)为了使太阳能汽车车身更为轻便,应大量使用下列_______ 材料来制造。
A 铝合金 B 锰钢 C 黄铜 D 焊锡
(2)太阳能汽车车身表面需要搭载太阳能电池板,太阳能电池板吸收能量,让汽车行驶,电池板在以上过程中的能量转化从最初的_______ 能最终转化为__________ 。
(3)太阳能汽车电池一般为硅电池,工业上在高温下用焦炭还原石英砂(主要成分是二氧化硅),得到粗的单质硅,反应的同时生成一种大气污染物,该反应的方程式为____________ ,反应前后硅元素的化合价分别为________ 。
(4)太阳能发电安全可靠,可以部分解决_________ 面临耗尽的问题,并在一定程度上减少对空气的污染。还有一些能源,如潮汐能、地热能、风能、_______ 、_________ 、也是人们正在开发和利用的其它能源。

(1)为了使太阳能汽车车身更为轻便,应大量使用下列
A 铝合金 B 锰钢 C 黄铜 D 焊锡
(2)太阳能汽车车身表面需要搭载太阳能电池板,太阳能电池板吸收能量,让汽车行驶,电池板在以上过程中的能量转化从最初的
(3)太阳能汽车电池一般为硅电池,工业上在高温下用焦炭还原石英砂(主要成分是二氧化硅),得到粗的单质硅,反应的同时生成一种大气污染物,该反应的方程式为
(4)太阳能发电安全可靠,可以部分解决
您最近一年使用:0次




