为了防止污染,用黄铜矿(主要成分是CuFeS2及少量含Zn的化合物)炼铜时,将产生的废气、废液转换成工业原料,设计流程如下:(假定每一步都完全反应)
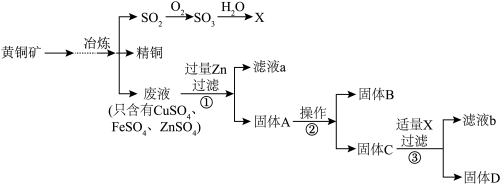
(1)废气处理后得到的产品X是____________ 。
(2)滤液a和滤液b中溶质的成分___________ (填“相同”或“不相同”)。
(3)步骤②的操作是________ 判断X适量的现象是_____________ 。
(4)若操作过程中物质的损失忽略不汁,要生成2.8 gB和3.2gD、则加入Zn的质量应至少大于___________ 。
(5)根据上述过程能否判断铜、铁、锌之间的活动性,说明理由__________ 。

(1)废气处理后得到的产品X是
(2)滤液a和滤液b中溶质的成分
(3)步骤②的操作是
(4)若操作过程中物质的损失忽略不汁,要生成2.8 gB和3.2gD、则加入Zn的质量应至少大于
(5)根据上述过程能否判断铜、铁、锌之间的活动性,说明理由
更新时间:2023-12-12 19:39:54
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
【推荐1】同学们在完成铁与硫酸铜反应的实验后,欲从废液(含硫酸铜和硫酸亚铁)中回收金属铜,并得到硫酸亚铁,其设计的流程如下:

(1)操作a的名称是______ ,操作过程中,同学发现速度太慢,可能的原因是______ 。
(2)写出流程中固体的成分是______ (写化学式);写出加入过量A时反应的化学方程式______ ;写出加入适量B时反应的化学方程式______ 。
(3)某同学误将锌粉当作A加入到废液中,操作b后得到的晶体是______ 。

(1)操作a的名称是
(2)写出流程中固体的成分是
(3)某同学误将锌粉当作A加入到废液中,操作b后得到的晶体是
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】A~I为初中化学常见物质,相互转化关系如图所示,“→”表示转化关系,“—”表示相互之间能发生反应(部分反应物、生成物以及反应条件省略)。其中,A、C、F、H含相同金属元素且所属物质类别不同,H、I类别相同;A、B为金属单质,B为紫红色;C、D为氧化物,C为红棕色固体;G溶液呈蓝色,E的浓溶液常用作某些气体的干燥剂。请回答问题:
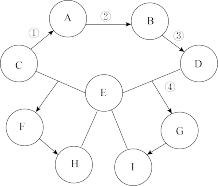
(1)B的化学式________ ,F的名称__________ 。
(2)写出化学方程式:
反应①______________________________ ,
反应④_______________________________ 。

(1)B的化学式
(2)写出化学方程式:
反应①
反应④
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐3】金属材料在生产、生活中具有十分重要的用途:
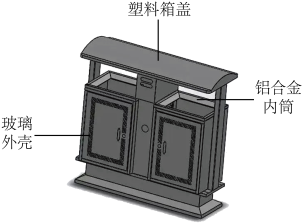
(1)贵阳的道路两旁的垃圾箱结构如图所示:垃圾箱内筒使用铝合金,是利用其_________ 优点。易拉罐应放入_________ (填“可回收”或“不可回收”)的桶内。
(2)铁制品在空气中锈蚀,实际上是铁与___________ 等物质发生一系列复杂的化学反应,防止铁制品生锈可采用的方法有__________ 。
(3)铜是人类最早使用的金属之一,炼铜工艺的发展史如图所示:

①西汉时期,刘安所著的《淮南万毕术》中,就有“曾青得铁则化为铜”的记载,“湿法炼铜”的化学方程式为___________ 。
②火法炼铜涉及的化学反应之一为Cu2(OH)2CO3 2CuO+H2O+CO2↑。生物炼铜是先将硫化铜在硫杆菌的作用下与空气中的氧气化合生成硫酸铜,硫酸铜再转化为铜。与“火法炼铜”相比,“生物炼铜”的优点是
2CuO+H2O+CO2↑。生物炼铜是先将硫化铜在硫杆菌的作用下与空气中的氧气化合生成硫酸铜,硫酸铜再转化为铜。与“火法炼铜”相比,“生物炼铜”的优点是__________ 。
(4)①某工厂的废水中含有Mg2+、Fe2+、Cu2+、Ag+等离子,某化学兴趣小组的同学取该厂废水样品加入锌,充分反应后过滤,得到滤液滤渣,若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定含有__________ 。
②某金属粉末含有Mg、Al、Cu中的一种或几种,取12g该金属粉末与足量稀盐酸反应产生1g氢气,则该金属粉末的组成可能为____________ 。

(1)贵阳的道路两旁的垃圾箱结构如图所示:垃圾箱内筒使用铝合金,是利用其
(2)铁制品在空气中锈蚀,实际上是铁与
(3)铜是人类最早使用的金属之一,炼铜工艺的发展史如图所示:

①西汉时期,刘安所著的《淮南万毕术》中,就有“曾青得铁则化为铜”的记载,“湿法炼铜”的化学方程式为
②火法炼铜涉及的化学反应之一为Cu2(OH)2CO3
 2CuO+H2O+CO2↑。生物炼铜是先将硫化铜在硫杆菌的作用下与空气中的氧气化合生成硫酸铜,硫酸铜再转化为铜。与“火法炼铜”相比,“生物炼铜”的优点是
2CuO+H2O+CO2↑。生物炼铜是先将硫化铜在硫杆菌的作用下与空气中的氧气化合生成硫酸铜,硫酸铜再转化为铜。与“火法炼铜”相比,“生物炼铜”的优点是(4)①某工厂的废水中含有Mg2+、Fe2+、Cu2+、Ag+等离子,某化学兴趣小组的同学取该厂废水样品加入锌,充分反应后过滤,得到滤液滤渣,若向滤渣中加入稀盐酸有气泡产生,则滤渣中一定含有
②某金属粉末含有Mg、Al、Cu中的一种或几种,取12g该金属粉末与足量稀盐酸反应产生1g氢气,则该金属粉末的组成可能为
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐1】有A、B、C、D、E、F、N、M八种物质,其中A为一种应用最广泛的金属,B由三种元素组成,C、D为单质且C为红色金属,D为黑色固体。它们之间有如下转化关系:①A + M B + C;②A + N
B + C;②A + N B + H2↑;③A +O2
B + H2↑;③A +O2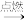 F;④D + F
F;④D + F A + CO2↑;⑤D+CO2
A + CO2↑;⑤D+CO2 E;⑥E + F
E;⑥E + F A + CO2↑。请回答下列问题
A + CO2↑。请回答下列问题
(1)E的用途__________ ;M为蓝色溶液,则其中含有的金属阳离子是_______ (填化学符号)。
(2)用化学方程式表示下列转化,并填空:
①A + M B + C
B + C _________ ;
②A + N B + H2↑
B + H2↑ __________ ,观察到的现象是__________ 。
③D + F A + CO2↑
A + CO2↑_________ ,其反应的基本类型是_________ 。
 B + C;②A + N
B + C;②A + N B + H2↑;③A +O2
B + H2↑;③A +O2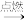 F;④D + F
F;④D + F A + CO2↑;⑤D+CO2
A + CO2↑;⑤D+CO2 E;⑥E + F
E;⑥E + F A + CO2↑。请回答下列问题
A + CO2↑。请回答下列问题(1)E的用途
(2)用化学方程式表示下列转化,并填空:
①A + M
 B + C
B + C ②A + N
 B + H2↑
B + H2↑ ③D + F
 A + CO2↑
A + CO2↑
您最近一年使用:0次
填空与简答-推断题
|
较难
(0.4)
解题方法
【推荐2】下图表示某些物质间转化关系(“→”表示物质之间存在转化关系,部分反应的条件已省略)。其中B、C是由相同元素组成的无色液体,且 B 具有消毒杀菌作用;D、H、I 为气体单质,其中 H 为空气含量最多的气体;M 为有刺激性气味的气体;A、E、F 为固体,F 呈红棕色。回答下列问题:
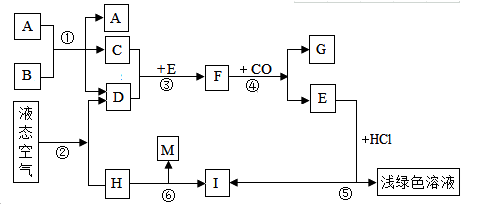
(1)①中 A 的作用是_____ ;
(2)②处利用_____ 不同(填字母,A.沸点 B.密度 C.溶解性),分离得两种气体;
(3)分别写出反应④和⑤的化学方程式:④_____ 、⑤ _____ 。
(4)已知同温同压下不同气体的体积之比等于气体分子个数之比。化合反应⑥是工业上的重要反应,为提高反应物的利用率,反应时应提供 H 和I 的最佳体积比为_____ 。
(5)工业上用 M 和 G 在一定条件下合成高效氮肥尿素 CO(NH2)2,反应中 M 和 G 的质量比为_____ 。

(1)①中 A 的作用是
(2)②处利用
(3)分别写出反应④和⑤的化学方程式:④
(4)已知同温同压下不同气体的体积之比等于气体分子个数之比。化合反应⑥是工业上的重要反应,为提高反应物的利用率,反应时应提供 H 和I 的最佳体积比为
(5)工业上用 M 和 G 在一定条件下合成高效氮肥尿素 CO(NH2)2,反应中 M 和 G 的质量比为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐3】电子工业上制造铜电路板,常用30%的FeC13溶液腐蚀镀铜电路板上的铜箔(Cu),如图是某兴趣小组设计的处理该生产过程中产生废液,并回收铜的流程图,据如图回答下列问题:
查阅资料: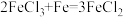
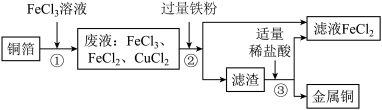
(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种成分,据此写出步骤①中发生的化学方程式_____________________ 。
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是_________ ,步骤②还需要进行的实验操作是_________ ,需用的玻璃仪器有烧杯、玻璃棒和_________ 。
(3)步聚③加入适量稀盐酸充分反应,当观察_________ 现象时,说明步骤②的铁粉过量。
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是_________ 。(填化学式)
(5)铜铁合金若干克经粉碎后与足量的稀盐酸充分反应,过滤后,得到的滤渣在空气中充分灼烧,结果灼烧后的生成物质量与原合金质量相等,则原合金中铁的质量分数为________________ 。
查阅资料:

(1)步骤①所得的废液中只含有FeCl3、CuCl2、FeCl2三种成分,据此写出步骤①中发生的化学方程式
(2)步骤②中加入的铁粉与氯化铜发生反应的化学方程式是
(3)步聚③加入适量稀盐酸充分反应,当观察
(4)步骤②③所得FeCl2可与一种气体单质发生化合反应生成FeCl3,实现循环使用,根据质量守恒定律可推测该单质是
(5)铜铁合金若干克经粉碎后与足量的稀盐酸充分反应,过滤后,得到的滤渣在空气中充分灼烧,结果灼烧后的生成物质量与原合金质量相等,则原合金中铁的质量分数为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
解题方法
【推荐1】金属在生产和生活中具有广泛的应用。
(1)冬天取暖用的暖气片有铸铁材料、铜铝材料等多种。这主要利用了金属的________ 性。
(2)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收ZnSO4和有关金属,流程如下:
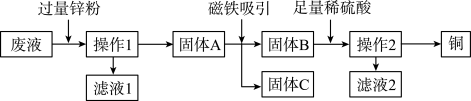
①“操作1”和“操作2”的名称是__________________ 。
②废液中加入过量锌粉的目的是______ ,写出该步骤中任意一个反应的化学方程式____ 。③滤液1和滤液2含有相同的溶质,该溶质是________________ (填化学式)。
(1)冬天取暖用的暖气片有铸铁材料、铜铝材料等多种。这主要利用了金属的
(2)某电镀厂为减少水污染及节约成本,从含有CuSO4、ZnSO4、FeSO4的废水中回收ZnSO4和有关金属,流程如下:

①“操作1”和“操作2”的名称是
②废液中加入过量锌粉的目的是
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】铁及其合金是人类较早使用的金属材料之一,与人类的生产生活紧密联系。
(1)日常生活中用铁锅烧水煮饭,这是利用了金属铁的______ 性。制造铁锅的金属材料常用生铁,生铁和钢是含碳量不同的两种铁合金,其中生铁的含碳量_______ (填“大于”或“小千”)钢的含碳量。
(2)铁粉可作食品脱氧剂,其原理与铁生锈相同,实际上是铁与空气中的水蒸气、________ 等发生化学反应。
(3)猛钢常用于制造铁轨。已知锰(Mn)的金属活动性介于镁和锌之间,下列试剂能够验证铁和锰的金属活动性强弱的是 (填序号)。
(4)我国古代很早就认识到铜盐溶液里的铜能被铁置换,这一方法是湿法冶金技术的起源。铁与硫酸铜溶液反应的化学方程式为_________ 。
(1)日常生活中用铁锅烧水煮饭,这是利用了金属铁的
(2)铁粉可作食品脱氧剂,其原理与铁生锈相同,实际上是铁与空气中的水蒸气、
(3)猛钢常用于制造铁轨。已知锰(Mn)的金属活动性介于镁和锌之间,下列试剂能够验证铁和锰的金属活动性强弱的是 (填序号)。
| A.Fe、Mn、MgSO4溶液 |
| B.Fe、Mn、ZnSO4溶液 |
| C.Cu、FeSO4溶液、MnSO4溶液 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】化学是人类进步的阶梯。
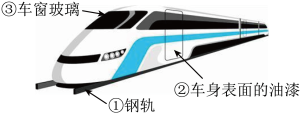
(1)鲁南高铁日照段已经开通,高速铁路可以加快出行步伐,给日照的经济发展带来前所未有的大好机遇。 结合所学化学知识,回答下列问题:
①图中标示的物质中属于金属材料的是______ (填序号);列车的电路中主要使用的是铜线,这主要是利用了铜的______ 性。
②修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。用赤铁矿炼铁的化学方程式为______ 。
③高铁酸钠(Na2FeO4)是高铁列车上常用的一种“绿色环保高效”消毒剂。其铁元素化合价为______ 。
(2)2019年4月23日,庆祝中国人民解放军海军成立70周年海上阅兵活动在青岛附近海空域举行。图为我国首号001A 型国产航母。根据所学知识填空。

①建造航母用到了钛合金。构成金属钛的粒子是______ (填“原子”“分子”或“离子”),工业制钛有一种反应为: ,X 的化学式为
,X 的化学式为______ 。
②为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验, 其中能达到目的是______ (填序号)。
A、稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B、ZnCl2溶液中加入足量铁粉后,再加入 CuCl2溶液
C、ZnCl2溶液中加入足量铁粉后,再加入 Cu 粉
③在 FeCl2和 CuCl2的混合溶液中加入 Zn 粉,下列说法错误的是______ 。
A、若反应完成后Zn无剩余,溶液中若有 CuCl2,则一定有 FeCl2
B、若反应完成后Zn无剩余,溶液中若无 CuCl2,则可能有 FeCl2
C、若反应完成后Zn有剩余,则溶液中有 ZnCl2,无 CuCl2和 FeCl2
D、若反应完成后Zn有剩余,则溶液中有 ZnCl2,无 CuCl2可能有 FeCl2

(1)鲁南高铁日照段已经开通,高速铁路可以加快出行步伐,给日照的经济发展带来前所未有的大好机遇。 结合所学化学知识,回答下列问题:
①图中标示的物质中属于金属材料的是
②修建铁路所需的大量钢铁是以铁矿石为主要原料冶炼而得。用赤铁矿炼铁的化学方程式为
③高铁酸钠(Na2FeO4)是高铁列车上常用的一种“绿色环保高效”消毒剂。其铁元素化合价为
(2)2019年4月23日,庆祝中国人民解放军海军成立70周年海上阅兵活动在青岛附近海空域举行。图为我国首号001A 型国产航母。根据所学知识填空。

①建造航母用到了钛合金。构成金属钛的粒子是
 ,X 的化学式为
,X 的化学式为②为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验, 其中能达到目的是
A、稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B、ZnCl2溶液中加入足量铁粉后,再加入 CuCl2溶液
C、ZnCl2溶液中加入足量铁粉后,再加入 Cu 粉
③在 FeCl2和 CuCl2的混合溶液中加入 Zn 粉,下列说法错误的是
A、若反应完成后Zn无剩余,溶液中若有 CuCl2,则一定有 FeCl2
B、若反应完成后Zn无剩余,溶液中若无 CuCl2,则可能有 FeCl2
C、若反应完成后Zn有剩余,则溶液中有 ZnCl2,无 CuCl2和 FeCl2
D、若反应完成后Zn有剩余,则溶液中有 ZnCl2,无 CuCl2可能有 FeCl2
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
【推荐1】向硝酸亚铁、硝酸银、硝酸镁的混合溶液中加入一定量的锌粉,充分反应后过滤,得到滤液和滤渣。
(1)若向滤渣中加稀盐酸无气泡,则滤液中一定含有的金属离子为_____________ (填符号)。要进一步确定可能含有的溶质,可在滤液中加入_____________ 溶液。
(2)若反应前后溶液的质量不变,则分别与硝酸亚铁、硝酸银反应的锌的质量比为______________ 。
(1)若向滤渣中加稀盐酸无气泡,则滤液中一定含有的金属离子为
(2)若反应前后溶液的质量不变,则分别与硝酸亚铁、硝酸银反应的锌的质量比为
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】向一定质量的AgNO3、Cu(NO3)2和Al(NO3)3的混合溶液中加入26g锌粉,充分反应后过滤,得到滤渣和滤液,将所得滤渣进行干燥并称量,所得滤渣质量为56g。向所得滤渣上滴加稀盐酸时无气泡产生。
(1)滤液中一定含有的溶质是_______ (写化学式,下同),一定不含有的溶质是______ 。
(2)所得滤渣中铜的质量为_________ 。
(1)滤液中一定含有的溶质是
(2)所得滤渣中铜的质量为
您最近一年使用:0次



