“九秋风露越窑开,夺得千峰翠色来”描述的是著名的青瓷。
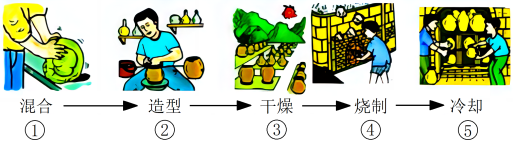
(1)手工制作陶瓷的过程如图,其中主要发生化学变化的过程是_______ (填序号)。
(2)青瓷的“翠色”来源十分复杂,涉及窑体内的CO和瓷器表面釉料中的氧化铁在高温下反应生成氧化亚铁和二氧化碳,该反应化学方程式为_______ 。
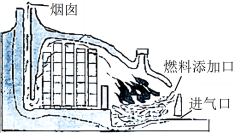
(3)如图所示的窑炉能够控制窑内CO的含量,从而实现调节釉色的目的。为了提高窑体内CO的体积分数,可以采用的措施有 (填序号)。
(1)手工制作陶瓷的过程如图,其中主要发生化学变化的过程是

(2)青瓷的“翠色”来源十分复杂,涉及窑体内的CO和瓷器表面釉料中的氧化铁在高温下反应生成氧化亚铁和二氧化碳,该反应化学方程式为
(3)如图所示的窑炉能够控制窑内CO的含量,从而实现调节釉色的目的。为了提高窑体内CO的体积分数,可以采用的措施有 (填序号)。

| A.相对增加空气鼓入 | B.相对增加燃料用量 |
| C.增大烟囱的排气量 | D.减小烟囱的排气量 |
更新时间:2023-12-29 14:50:48
|
相似题推荐
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐1】阅读下面科普短文(原文作者:杨骏等,有删改)
即使艳阳高照、天气晴好,有时人们也会出现眼睛刺痛、咳嗽等不良症状。专家认为,这很可能与臭氧(O3)有关。
臭氧原本是大气中自然产生的一种具有特殊臭味的微量气体。在常温常压下可缓慢反应生成氧气,当温度达到165℃迅速反应。绝大部分臭氧存在于离地面25公里左右处的大气平流层中,这就是人们通常所说的臭氧层。臭氧量往往随纬度、季节和天气等因素的变化而不同。研究人员发现,天空中的臭氧层能吸收99%以上的太阳紫外线,为地球上的生物提供了天然的保护屏障。为何它又成了危害健康的污染物?
地表臭氧并非自然产生的,而是由石油产品(如汽油)等矿物燃料燃烧产生的氮氧化物(如二氧化氮)与空气中的氧气结合而形成的。强烈的阳光照射会加速这一化学反应。
地表空气中的臭氧对人体极为有害,一些易于过敏的人长时间暴露在臭氧含量超过每立方米180微克的环境中,会产生上述不良症状。研究表明,空气中每立方米臭氧含量增加100微克,人的呼吸功能就会减弱3%。对于运动员来说,空气中的臭氧含量可以直接影响到他们的耐力和比赛成绩。
自2013年中国执行新《环境空气质量标准》,监测6种污染物以来,臭氧便成为一些城市夏季空气质量“超标日”的首要污染物。下图为某地夏季某日昼时(7:00~18:00)臭氧、二氧化氮(NO2)浓度随时间的变化图。

依据文章内容,回答下列问题。
(1)写出臭氧的一条物理性质_______ 。
(2)写出臭氧迅速生成氧气反应的文字表达式_______ 。
(3)如上图,某地夏季某日昼时,臭氧污染最严重的时间段是_______ (填序号)。
A 8:00~10:00 B 10:00~12:00 C 12:00~14:00 D 14:00~16:00
(4)下列说法错误的是_______ (填序号)。
A 氧气和臭氧化学性质不同的原因是因为分子构成不同
B 臭氧层具有吸收紫外线的作用
C 地表空气中臭氧的含量与天气阴晴无关
D 空气中臭氧浓度不同会对人体造成不同程度的影响
(5)为了减少臭氧污染,请你向市民提出一条生活中可行的倡议_______ 。
即使艳阳高照、天气晴好,有时人们也会出现眼睛刺痛、咳嗽等不良症状。专家认为,这很可能与臭氧(O3)有关。
臭氧原本是大气中自然产生的一种具有特殊臭味的微量气体。在常温常压下可缓慢反应生成氧气,当温度达到165℃迅速反应。绝大部分臭氧存在于离地面25公里左右处的大气平流层中,这就是人们通常所说的臭氧层。臭氧量往往随纬度、季节和天气等因素的变化而不同。研究人员发现,天空中的臭氧层能吸收99%以上的太阳紫外线,为地球上的生物提供了天然的保护屏障。为何它又成了危害健康的污染物?
地表臭氧并非自然产生的,而是由石油产品(如汽油)等矿物燃料燃烧产生的氮氧化物(如二氧化氮)与空气中的氧气结合而形成的。强烈的阳光照射会加速这一化学反应。
地表空气中的臭氧对人体极为有害,一些易于过敏的人长时间暴露在臭氧含量超过每立方米180微克的环境中,会产生上述不良症状。研究表明,空气中每立方米臭氧含量增加100微克,人的呼吸功能就会减弱3%。对于运动员来说,空气中的臭氧含量可以直接影响到他们的耐力和比赛成绩。
自2013年中国执行新《环境空气质量标准》,监测6种污染物以来,臭氧便成为一些城市夏季空气质量“超标日”的首要污染物。下图为某地夏季某日昼时(7:00~18:00)臭氧、二氧化氮(NO2)浓度随时间的变化图。

依据文章内容,回答下列问题。
(1)写出臭氧的一条物理性质
(2)写出臭氧迅速生成氧气反应的文字表达式
(3)如上图,某地夏季某日昼时,臭氧污染最严重的时间段是
A 8:00~10:00 B 10:00~12:00 C 12:00~14:00 D 14:00~16:00
(4)下列说法错误的是
A 氧气和臭氧化学性质不同的原因是因为分子构成不同
B 臭氧层具有吸收紫外线的作用
C 地表空气中臭氧的含量与天气阴晴无关
D 空气中臭氧浓度不同会对人体造成不同程度的影响
(5)为了减少臭氧污染,请你向市民提出一条生活中可行的倡议
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】空气是我们赖以生存的宝贵资源。如图是以空气等为原料合成农业上一种重要的化肥--尿素的工艺流程。请按要求回答相关问题:
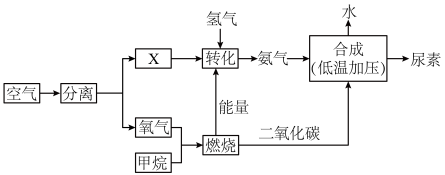
(1)X是空气中含量最多的气体______ 。
(2)氧气有很多用途。下列不属于氧气用途的是(单选,填字母序号)______。
(3)空气分离出X气体和氧气的变化属于(选填“物理”或“化学”)______ 变化。
(4)从环保角度看,下列保护空气措施合理的有(填标号)______。
(5)写出甲烷燃烧的化学方程式______ 。

(1)X是空气中含量最多的气体
(2)氧气有很多用途。下列不属于氧气用途的是(单选,填字母序号)______。
| A.医疗急救 | B.食物防腐 | C.航天火箭 | D.气焊气割 |
(3)空气分离出X气体和氧气的变化属于(选填“物理”或“化学”)
(4)从环保角度看,下列保护空气措施合理的有(填标号)______。
| A.将会排放大量污染气体的工厂搬到人烟稀少的地方 |
| B.提倡步行、骑自行车等出行方式 |
| C.在重大节日燃放烟花爆竹增强节日气氛 |
| D.加强大气监测,使用新型清洁能源 |
(5)写出甲烷燃烧的化学方程式
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】如下图是以经过除尘,除二氧化碳、除水的空气为原料生产尿素的流程(部分生成物已省略),请回答有关问题:
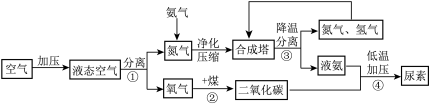
(1)①中从液态空气中分离出氮气、氧气,该过程中只涉及物理变化,判断的依据是______ 。
(2)该流程中,可以循环利用的物质是______ 。
(3)氨气液化可得液氨。根据③分析,氢气、氮气和氨气三种气体中,氨气沸点比氢气和氮气的沸点都要______ (填“高”或“低”)。
(4)该流程①中若要制得143g氧气(已知在标准状况下,氧气的密度为1.43g/L),理论上需要空气的体积为______ 。(空气中氧气体积按五分之一计算)

(1)①中从液态空气中分离出氮气、氧气,该过程中只涉及物理变化,判断的依据是
(2)该流程中,可以循环利用的物质是
(3)氨气液化可得液氨。根据③分析,氢气、氮气和氨气三种气体中,氨气沸点比氢气和氮气的沸点都要
(4)该流程①中若要制得143g氧气(已知在标准状况下,氧气的密度为1.43g/L),理论上需要空气的体积为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】化学实验中常常使用火柴,已知火柴头含有 单质X、氯酸钾、二氧化锰等,火柴盒侧面含有红磷、三硫化二锑等,试回答以下问题:
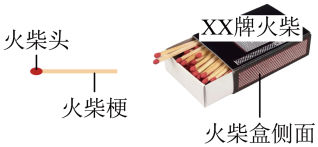
(1)___________ 的高锰酸钾溶液遇单质 X 燃烧生成的气体褪为无色,该气体还是形成硫酸型酸雨的主要污染物,则单质X是 ___________ ,它在空气中燃烧的化学方程式为 ___________ ,防止酸雨的形成的措施有 ___________ 。 ( 只写一种 )
(2)某同学取一支试管,加入10%的___________ 溶液,放入三根火柴头,溶液中产生大量气泡,将一根带火星的木条伸入试管内,木条复燃。产生气泡的化学方程式为 ___________ ,二氧化锰在该反应中起 ___________ 作用。
(3)已知氯酸钾中氯原子与氧原子个数比为1:3,其中氯元素的化合价为+5,则氯酸钾的化学式为___________ 。

(1)
(2)某同学取一支试管,加入10%的
(3)已知氯酸钾中氯原子与氧原子个数比为1:3,其中氯元素的化合价为+5,则氯酸钾的化学式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】如图:已知甲、乙、丙是初中化学常见的三种物质,且三种物质中均含有相同的某种元素。乙、丙是组成元素相同的气体,丙是一种有毒气体。它们的转化关系如图所示。(“→”表示一种物质能转化为另一种物质,部分反应物、生成物及反应条件已略去)

(1)甲可能是______ (填化学式)。
(2)写出乙转化为丙的化学方程式____________ ,该反应___ (填“放出”或“吸收”)热量。
(3)请你设计一种鉴别乙和丙的方法:_________ 。

(1)甲可能是
(2)写出乙转化为丙的化学方程式
(3)请你设计一种鉴别乙和丙的方法:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐3】铝土矿的主要成分是 ,含有杂质
,含有杂质 、
、 。下图为工业上从铝土矿中提取铝的工艺流程图:
。下图为工业上从铝土矿中提取铝的工艺流程图:
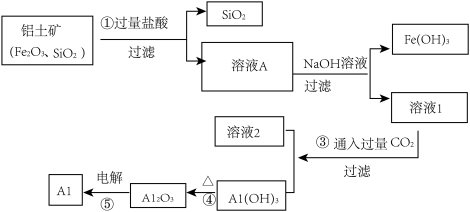
请回答下列问题:
(1)溶液 中的溶质成分是
中的溶质成分是______ (写化学式)。
(2)请写出反应①中发生的一个反应的化学方程式______ 。
(3)反应②除生成Fe(OH)3外,还生成了偏铝酸钠(NaAlO2),偏铝酸钠属于______ (填“酸”、“碱”或“盐”),溶液1中通入过量二氧化碳,生成氢氧化铝和另一种生活中常见的盐,已知两种生成物的质量比为78:84,写出该反应生成的这种盐的化学式______ 。
(4)反应 中还生成了一种气体单质,请写出该气体的一种用途
中还生成了一种气体单质,请写出该气体的一种用途______ 。
 ,含有杂质
,含有杂质 、
、 。下图为工业上从铝土矿中提取铝的工艺流程图:
。下图为工业上从铝土矿中提取铝的工艺流程图:
请回答下列问题:
(1)溶液
 中的溶质成分是
中的溶质成分是(2)请写出反应①中发生的一个反应的化学方程式
(3)反应②除生成Fe(OH)3外,还生成了偏铝酸钠(NaAlO2),偏铝酸钠属于
(4)反应
 中还生成了一种气体单质,请写出该气体的一种用途
中还生成了一种气体单质,请写出该气体的一种用途
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
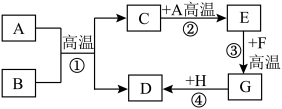
【推荐1】 是初中化学常见的物质。已知A为红棕色粉末,
是初中化学常见的物质。已知A为红棕色粉末, 为有毒气体,F为红色固体单质,它们的转化关系如下图所示,回答问题。
为有毒气体,F为红色固体单质,它们的转化关系如下图所示,回答问题。
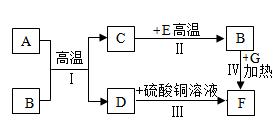
(1)写出下列物质的化学式
_____ ;
_____ 。
(2)反应Ⅱ的化学方程式为_____ 。
(3)反应Ⅲ的化学方程式为_____ 。
(4)反应Ⅳ的化学方程式为_____ 。
 是初中化学常见的物质。已知A为红棕色粉末,
是初中化学常见的物质。已知A为红棕色粉末, 为有毒气体,F为红色固体单质,它们的转化关系如下图所示,回答问题。
为有毒气体,F为红色固体单质,它们的转化关系如下图所示,回答问题。
(1)写出下列物质的化学式


(2)反应Ⅱ的化学方程式为
(3)反应Ⅲ的化学方程式为
(4)反应Ⅳ的化学方程式为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
【推荐2】如图是初中科学常见的一些氧化物和单质之间的相互转化关系。其中单质Ⅰ为红色固体,氧化物Ⅰ和单质Ⅲ 均为黑色固体,氧化物Ⅲ能使澄清石灰水变浑浊。则:
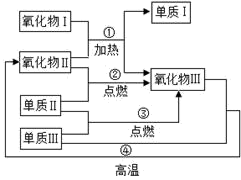
(1)氧化物I是________ ,单质III是_________ 。(填化学式)
(2)反应①中_______ (填化学式)发生了还原反应;
(3)氧化物Ⅱ除图中所示的化学性质外,还具有__________ 性,对人体有危害。
(4)根据题意,写出反应④的化学方程式________________________________ 。

(1)氧化物I是
(2)反应①中
(3)氧化物Ⅱ除图中所示的化学性质外,还具有
(4)根据题意,写出反应④的化学方程式
您最近一年使用:0次
【推荐1】中国古代很多发明创造与化学工艺有关。西汉海昏侯墓出土的青铜雁鱼灯造型优美,设计精妙,其剖面图如图。
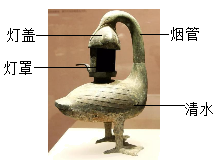
(1)先秦《考工记》中有关青铜成分记载:“六分其金而锡居其一”(注:此处“金”指铜),由此可知,雁鱼灯灯体的材质硬度比纯铜______ (选填“大”或“小”)。
(2)点燃雁鱼灯古人使用的“火折子”吹气即可燃。简易的火折子是将纸卷点燃后,使其半灭(仅剩火星),装入竹筒中保存。需要点火时打开竹筒盖,向其中吹气,使纸复燃。
①从燃烧条件角度分析,吹气可以使纸复燃的原因是______ 。
②火折子中含有火硝(KNO3),受热后可分解为氧气和亚硝酸钾(KNO2),该反应的化学方程式为______ 。
(3)雁鱼灯的灯罩可自由开合,以调节进风量的大小。当看到有大量黑烟产生时,应该______ (选填“扩大”或“减小”)进风口从而促进燃料充分燃烧。
(4)雁鱼灯的烟管可将燃烧产生的废气引入水中以减少对室内环境的污染。《汉书·地理志》中记载:“高奴,有淆水可燃”(注:“高奴”为地名,“淆水”指的是石油)。如果雁鱼灯采用淆水为燃料,燃烧产生的废气中含有的污染性气体如______ (填化学式)会使水体呈______ 性,需要经常换水。

(1)先秦《考工记》中有关青铜成分记载:“六分其金而锡居其一”(注:此处“金”指铜),由此可知,雁鱼灯灯体的材质硬度比纯铜
(2)点燃雁鱼灯古人使用的“火折子”吹气即可燃。简易的火折子是将纸卷点燃后,使其半灭(仅剩火星),装入竹筒中保存。需要点火时打开竹筒盖,向其中吹气,使纸复燃。
①从燃烧条件角度分析,吹气可以使纸复燃的原因是
②火折子中含有火硝(KNO3),受热后可分解为氧气和亚硝酸钾(KNO2),该反应的化学方程式为
(3)雁鱼灯的灯罩可自由开合,以调节进风量的大小。当看到有大量黑烟产生时,应该
(4)雁鱼灯的烟管可将燃烧产生的废气引入水中以减少对室内环境的污染。《汉书·地理志》中记载:“高奴,有淆水可燃”(注:“高奴”为地名,“淆水”指的是石油)。如果雁鱼灯采用淆水为燃料,燃烧产生的废气中含有的污染性气体如
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】我国煤炭资源丰富。目前人们除了将煤作为燃料外,更是重要的化工原料。工业上以煤和空气为原料生产尿素[CO(NH2)2]的一种流程如下:
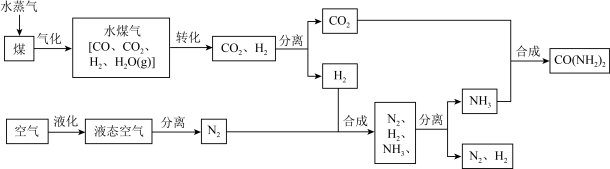
(1)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是______ 。
(2)水煤气在铜催化下实现 CO 的转化: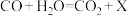 ,其中 X 的化学式为
,其中 X 的化学式为______ 。
(3)上述流程中合成尿素的同时还有水生成,该反应的化学方程式为______ 。
(4)实际生产中,N2和 H2不可能全部化为 NH3。上述流程中可以环利用的物质有______ 。
(5)以 CO2和 H2为原料还可合成液体燃料乙醇(C2H6O),该过程可用化学方程式表示为: 。已知:每克燃料完全燃烧数出的热量叫做热值
。已知:每克燃料完全燃烧数出的热量叫做热值
若将含 12g 的碳的煤为原料合成的乙醇完全燃烧。理论上最多可放出______ kJ的热量,从而提高了煤的利用效率。

(1)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是
(2)水煤气在铜催化下实现 CO 的转化:
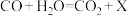 ,其中 X 的化学式为
,其中 X 的化学式为(3)上述流程中合成尿素的同时还有水生成,该反应的化学方程式为
(4)实际生产中,N2和 H2不可能全部化为 NH3。上述流程中可以环利用的物质有
(5)以 CO2和 H2为原料还可合成液体燃料乙醇(C2H6O),该过程可用化学方程式表示为:
 。已知:每克燃料完全燃烧数出的热量叫做热值
。已知:每克燃料完全燃烧数出的热量叫做热值| 物质 | 煤 | 乙醇 |
| 热值/kJ·g-1 | 约 33 | 30 |
您最近一年使用:0次