某兴趣小组拟选用鸡蛋壳作为实验室制取二氧化碳的原料。为了测定鸡蛋壳中CaCO3的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图:
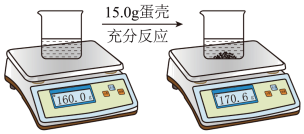
(说明:①忽略二氧化碳溶于水对实验结果的影响;②假设其它物质不溶于水,也不与稀盐酸反应)
(1)捣碎鸡蛋壳的目的是______ 。
(2)根据图示判断:蛋壳中的CaCO3与盐酸反应生成二氧化碳的质量是______ g;
(3)根据此数据计算鸡蛋壳中CaCO3的质量分数。(请写出计算过程,结果保留到0.1%)

(说明:①忽略二氧化碳溶于水对实验结果的影响;②假设其它物质不溶于水,也不与稀盐酸反应)
(1)捣碎鸡蛋壳的目的是
(2)根据图示判断:蛋壳中的CaCO3与盐酸反应生成二氧化碳的质量是
(3)根据此数据计算鸡蛋壳中CaCO3的质量分数。(请写出计算过程,结果保留到0.1%)
23-24九年级上·山东枣庄·阶段练习 查看更多[2]
更新时间:2023-12-23 10:27:01
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】冬天捞的纯碱中常含有较多的氯化钠,某中学化学兴趣小组为测定某纯碱样品中碳酸钠的含量,进行了如下实验。
(1)纯碱样品中碳酸钠的质量分数为多少?(保留一位小数)
(2)溶液 A 中溶质的质量分数为多少?

(1)纯碱样品中碳酸钠的质量分数为多少?(保留一位小数)
(2)溶液 A 中溶质的质量分数为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某品牌“暖宝宝”的发热包主要成分是铁粉、水、活性炭、食盐等。为测定发热包中铁粉的质量分数,兴趣小组的同学进行如图实验:(已知发热包中其他成分不与盐酸反应)

请分析并计算:
(1)生成氢气的质量为_______ 。
(2)该品牌“暖宝宝”发热包中铁粉的质量分数_______ 。

请分析并计算:
(1)生成氢气的质量为
(2)该品牌“暖宝宝”发热包中铁粉的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】为测定碳酸钠和氯化钠的混合物中两种物质的质量比,进行如下实验,实验流程和数据记录如图所示,回答下列问题:
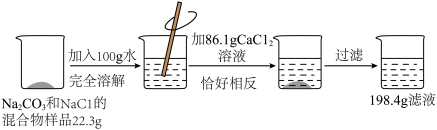
(1)写出上述过程中发生反应的化学方程式:__________________________________ ;
(2)根据质量守恒定律,分析数据可知,过滤所得滤渣的质量为__________ ;
(3)根据沉淀质量列出参加反应的氯化钙质量(x)的比例式为__________________ ;
(4)样品中碳酸钠与氯化钠的质量比为_________________ ;
(5)向反应后的滤液中加入1.6g水后所得溶液中溶质的质量分数为___________ 。

(1)写出上述过程中发生反应的化学方程式:
(2)根据质量守恒定律,分析数据可知,过滤所得滤渣的质量为
(3)根据沉淀质量列出参加反应的氯化钙质量(x)的比例式为
(4)样品中碳酸钠与氯化钠的质量比为
(5)向反应后的滤液中加入1.6g水后所得溶液中溶质的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某固体为CaCl2和CaCO3的混合物粉末,用该固体粉末与稀盐酸反应,进行了三次实验,所得相关的实验数据记录如下,
(1)根据上表数据分析,当固体的质量与该稀盐酸的质量比为_____ 时,实验恰好完全反应。
(2)稀盐酸的溶质质量分数。
| 第一次 | 第二次 | 第三次 | |
| 混合物的质量/g | 20 | 20 | 30 |
| 所用稀盐酸的质量/g | 120 | 140 | 100 |
| 充分反应后,剩余物总质量/g | 135.6 | 155.6 | 125.6 |
(1)根据上表数据分析,当固体的质量与该稀盐酸的质量比为
(2)稀盐酸的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】工业废水需处理达到标准后再排放,以免造成水体污染。某造纸厂欲排放200t含NaOH的废水,用溶质质量分数为20%的废硫酸来处理,实验过程中,溶液pH的变化如图所示。请计算:____ t。
(2)该废水中氢氧化钠的质量分数。
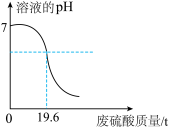
(2)该废水中氢氧化钠的质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】为确定某蛋壳中碳酸钙的质量分数,化学兴趣小组进行如下实验:称取该蛋壳(主要成分是CaCO3,杂质不反应)加入烧杯中,向其中逐渐加入稀盐酸至完全反应。反应结束后,称量烧杯及其中物质总质量(溶解的气体忽略不计),有关数据记录如下表。
(1)实验中产生的二氧化碳质量为______ g。
(2)请计算该蛋壳中碳酸钙的质量分数。(写出计算过程,计算结果精确到0.1%)
| 烧杯 | 蛋壳 | 稀盐酸 | 反应后烧杯及其中物质总质量 | |
| 质量/g | 105 | 7.8 | 60 | 169.5 |
(2)请计算该蛋壳中碳酸钙的质量分数。(写出计算过程,计算结果精确到0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
真题
【推荐1】某兴趣小组拟选用鸡蛋壳作为实验室制取二氧化碳的原料。为了测定鸡蛋壳中CaCO3的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图:
(1)捣碎鸡蛋壳的目的是_______ 。
(2)根据图示判断:蛋壳中的CaCO3与盐酸反应生成二氧化碳的质量是_______ g,根据此数据计算CaCO3的质量分数为_______ (结果保留到0.1%);
(3)对此计算结果,兴趣小组认为满足实验要求。但有同学认为该结果有可能偏低,理由是_______ 。
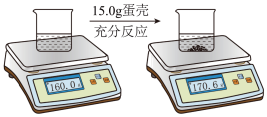
(1)捣碎鸡蛋壳的目的是
(2)根据图示判断:蛋壳中的CaCO3与盐酸反应生成二氧化碳的质量是
(3)对此计算结果,兴趣小组认为满足实验要求。但有同学认为该结果有可能偏低,理由是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组拟选用鸡蛋壳作为实验室制取二氧化碳的原料。为了测定鸡蛋壳中 的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图:
的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图:
(1)捣碎鸡蛋壳的目的是______ 。
(2)根据图示判断:蛋壳中的 与盐酸反应生成二氧化碳的质量是
与盐酸反应生成二氧化碳的质量是______ 。
(3)计算蛋壳中 的质量分数(写出计算过程,结果保留到0.1%)。
的质量分数(写出计算过程,结果保留到0.1%)。
(4)对此计算结果,兴趣小组认为满足实验要求。但有同学认为该结果有可能偏高,理由是______ 。
 的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图:
的质量分数是否满足实验要求,该小组同学进行如下实验,将鸡蛋壳洗净、捣碎后准确称量15.0g,全部投入足量稀盐酸中,电子秤的示数变化情况如图: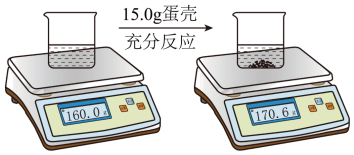
(1)捣碎鸡蛋壳的目的是
(2)根据图示判断:蛋壳中的
 与盐酸反应生成二氧化碳的质量是
与盐酸反应生成二氧化碳的质量是(3)计算蛋壳中
 的质量分数(写出计算过程,结果保留到0.1%)。
的质量分数(写出计算过程,结果保留到0.1%)。(4)对此计算结果,兴趣小组认为满足实验要求。但有同学认为该结果有可能偏高,理由是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】海蛎子壳的主要成分是碳酸钙,为了测定某海蛎子壳中碳酸钙的含量,甲同学进行了如下实验:将海蛎子壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得烧杯中物质的总质量为97.8g。(假设海蛎子壳中的其它物质不与盐酸反应)。
(1)实验过程中将海蛎子壳捣碎的目的是______ 。
(2)充分反应后产生二氧化碳气体的质量是______ 。
(3)计算该海蛎子壳中碳酸钙的质量分数,要求写出完整的解题步骤。
(1)实验过程中将海蛎子壳捣碎的目的是
(2)充分反应后产生二氧化碳气体的质量是
(3)计算该海蛎子壳中碳酸钙的质量分数,要求写出完整的解题步骤。
您最近一年使用:0次



