计算:无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。某种品牌茄子的无土栽培营养液中含有6%的KNO3。
(1)KNO3中钾、氮、氧元素的质量比为______ ;
(2)KNO3的化学式量为______ ;
(3)要配制150kg该营养液,需要KNO3多少千克?______ 要使该溶液的质量分数增一倍,则应将该溶液蒸发掉______ 千克水。
(1)KNO3中钾、氮、氧元素的质量比为
(2)KNO3的化学式量为
(3)要配制150kg该营养液,需要KNO3多少千克?
更新时间:2024-01-10 20:09:36
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】苹果中富含苹果酸,具有增强消化,降低胆固醇等作用,苹果酸的分子式为C4H6O5.请计算:
(1)苹果酸由___ 种元素组成。
(2)一个苹果酸分子由___ 个原子构成。
(3)苹果酸的相对分子质量是___ 。
(4)苹果酸中碳、氢、氧三种元素的质量比是___ (最简整数比)。
(5)13.4g苹果酸中含C元素质量___ 克?(写出计算过程,答案精确到0.1)
(1)苹果酸由
(2)一个苹果酸分子由
(3)苹果酸的相对分子质量是
(4)苹果酸中碳、氢、氧三种元素的质量比是
(5)13.4g苹果酸中含C元素质量
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】红葡萄酒中因含有花色苷而呈红色,花色苷是一种天然色素,对人体有抗癌减肥等保健功能,它的化学式是C16H16O6。
(1)花色苷由_____种元素组成。
(2)花色苷中C、H、O三种元素的原子个数比是____________。
(3)花色苷中的碳、氢元素的质量比为______________。
(4)花色苷的相对分子质量为__________。
(5)60.8g花色苷中含有_____g氧元素。
(1)花色苷由_____种元素组成。
(2)花色苷中C、H、O三种元素的原子个数比是____________。
(3)花色苷中的碳、氢元素的质量比为______________。
(4)花色苷的相对分子质量为__________。
(5)60.8g花色苷中含有_____g氧元素。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】2008年9月份曝光的引起国人共愤的“结石宝宝”事件,与婴幼儿服用含有三聚氰胺的奶粉有关。已知三聚氰胺为白色晶体,将它用作食品添加剂可提高食品中蛋白质的检测值,俗称“蛋白精”,化学式为C3H6N6。据此请计算:(比值要求最简比)
(1)三聚氰胺的相对分子质量_____;
(2)三聚氰胺中碳、氢、氮原子的个数比_____。
(3)三聚氰胺中碳元素、氢元素与氮元素的质量比_____。
(4)三聚氰胺中氮元素的质量分数。(结果精确到0.1%)
(5)若有42克的三聚氰胺,则氮元素的质量为_____。
(1)三聚氰胺的相对分子质量_____;
(2)三聚氰胺中碳、氢、氮原子的个数比_____。
(3)三聚氰胺中碳元素、氢元素与氮元素的质量比_____。
(4)三聚氰胺中氮元素的质量分数。(结果精确到0.1%)
(5)若有42克的三聚氰胺,则氮元素的质量为_____。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】氯化铁常用于蚀刻铜电路板,其主要反应原理为: 。经检测,溶质的质量分数为35%的氯化铁溶液蚀刻效果最佳,当其浓度降至28%以下时蚀刻效果不达标。现用溶质的质量分数为32.5%的氯化铁300g溶液进行蚀刻铜电路板,一段时间后溶液质量变为306.4g,请据此回答下列问题:
。经检测,溶质的质量分数为35%的氯化铁溶液蚀刻效果最佳,当其浓度降至28%以下时蚀刻效果不达标。现用溶质的质量分数为32.5%的氯化铁300g溶液进行蚀刻铜电路板,一段时间后溶液质量变为306.4g,请据此回答下列问题:
(1)氯化铁中铁、氯元素的质量比为______ (填最简整数比)。
(2)经过上述反应后溶液所增加的质量为______ g。
(3)试通过计算判断经过上述蚀刻后剩余溶液的蚀刻效果是否达标。(精确至0.1%)
 。经检测,溶质的质量分数为35%的氯化铁溶液蚀刻效果最佳,当其浓度降至28%以下时蚀刻效果不达标。现用溶质的质量分数为32.5%的氯化铁300g溶液进行蚀刻铜电路板,一段时间后溶液质量变为306.4g,请据此回答下列问题:
。经检测,溶质的质量分数为35%的氯化铁溶液蚀刻效果最佳,当其浓度降至28%以下时蚀刻效果不达标。现用溶质的质量分数为32.5%的氯化铁300g溶液进行蚀刻铜电路板,一段时间后溶液质量变为306.4g,请据此回答下列问题:(1)氯化铁中铁、氯元素的质量比为
(2)经过上述反应后溶液所增加的质量为
(3)试通过计算判断经过上述蚀刻后剩余溶液的蚀刻效果是否达标。(精确至0.1%)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】乙醇俗称酒精,化学式为:C2H5OH,可用作医用消毒,也常作燃料。其完全燃烧的化学方程式可表示为: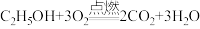 。
。
(1)乙醇由________ 种元素组成,碳元素和氢元素的质量比__________ 。
(2)23g乙醇完全燃烧需消耗多少克氧气?(写出计算过程)
(3)乙醇不完全燃烧会产生一氧化碳,某实验测得反应前后各物质的质量如下表:
①中a的值为__________ 。
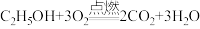 。
。(1)乙醇由
(2)23g乙醇完全燃烧需消耗多少克氧气?(写出计算过程)
(3)乙醇不完全燃烧会产生一氧化碳,某实验测得反应前后各物质的质量如下表:
| 物质 | 乙醇 | 氧气 | 二氧化碳 | 水 | 一氧化碳 |
| 反应前质量(g) | 4.6 | 8.8 | 0 | 0 | 0 |
| 反应后质量(g) | 0 | 0 | 6.6 | 5.4 | a |
①中a的值为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】2017年5月中国自主知识产权抗癌新药“西达苯胺”全球上市。我国有了自己原创的抗癌新药。某种西达苯胺(化学式为C22H19FN4O2)药片中,除了含有西达苯胺外,还含有淀粉。
(1)西达苯胺中所含元素的种类是___________ 种;
(2)西达苯胺的化学式量(即相对分子质量)为_________ ;
(3)药厂检验室对该西达苯胺药片进行检验,若测得药片中氟元素的含量为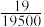 ,则该药片中含西达苯胺的质量分数是
,则该药片中含西达苯胺的质量分数是_________ 。
(1)西达苯胺中所含元素的种类是
(2)西达苯胺的化学式量(即相对分子质量)为
(3)药厂检验室对该西达苯胺药片进行检验,若测得药片中氟元素的含量为
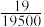 ,则该药片中含西达苯胺的质量分数是
,则该药片中含西达苯胺的质量分数是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】现有20mL质量分数为98%的浓硫酸。
(1)要想计算其质量大小,还需要知道的条件是____________;
(2)向盛放有该浓硫酸的锥形瓶中,滴加蒸馏水,能够看到的现象是____________?
(1)要想计算其质量大小,还需要知道的条件是____________;
(2)向盛放有该浓硫酸的锥形瓶中,滴加蒸馏水,能够看到的现象是____________?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】某碳酸钠样品含有少量的硫酸钠,取12g的该样品,完全溶解在水中配制成100g溶液,将其全部加入到100g一定质量分数的硫酸溶液中,恰好完全反应,生成的气体全部逸出后,所得溶液质量是195.6g。计算:
(1)加入的硫酸溶液的溶质质量分数;
(2)将反应后滤液蒸干,可得固体多少克?
(1)加入的硫酸溶液的溶质质量分数;
(2)将反应后滤液蒸干,可得固体多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】如图为某钙片的商品标签,为测定该钙片中碳酸钙的质量分数(假设钙片中其他物质不溶于水,也不与任何物质发生反应),某同学取10片钙片,进行如下实验:


(1)请计算该钙片中碳酸钙的质量分数(写出具体计算过程)。______
(2)用36.5%的浓盐酸配制50g上述稀盐酸,所需浓盐酸的质量为 g。
(3)该钙片中钙元素的质量分数为 。


(1)请计算该钙片中碳酸钙的质量分数(写出具体计算过程)。______
(2)用36.5%的浓盐酸配制50g上述稀盐酸,所需浓盐酸的质量为 g。
(3)该钙片中钙元素的质量分数为 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】2020年新型冠状病毒席卷全球,开学以后做好防护是我们大家应该必备的常识。学校新进一批84消毒液,84消毒液是一种常用的含氯消毒剂,主要成分就是次氯酸钠,可用于各种物体表面和环境等的消毒。84消毒液有刺激性和腐蚀性,一定要稀释以后使用。下面请大家配置使用。(配置溶液时体积变化忽略不计)

(1)配置教室消毒液100升,则需要84消毒液 ;
(2)卫生间消毒,有84消毒液20升,可配溶液_____。

(1)配置教室消毒液100升,则需要84消毒液 ;
(2)卫生间消毒,有84消毒液20升,可配溶液_____。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】XH 中学九年级化学实验兴趣小组的同学在实验室找到一瓶未标注质量分数的氢氧化钠溶液,为测定这瓶氢氧化钠溶液的质量分数,取 50g 氢氧化钠溶液于烧杯中,分两次加入硫酸铜溶液,过滤后所得溶液质量如图所示。请回答下列问题:

(1)上述实验过程中发生反应的化学方程式为_____ ;
(2)根据已知条件列出求解 100g 硫酸铜溶液中溶质质量(X)的比例式_____ ;
(3)第二次反应结束后烧杯内溶液中的溶质为______ ;
(4)该瓶氢氧化钠溶液的溶质质量分数为_____ ;
(5)若要配制 150g16%的氢氧化钠溶液,需要该瓶中的氢氧化钠溶液_____ g。

(1)上述实验过程中发生反应的化学方程式为
(2)根据已知条件列出求解 100g 硫酸铜溶液中溶质质量(X)的比例式
(3)第二次反应结束后烧杯内溶液中的溶质为
(4)该瓶氢氧化钠溶液的溶质质量分数为
(5)若要配制 150g16%的氢氧化钠溶液,需要该瓶中的氢氧化钠溶液
您最近一年使用:0次



