两种金属Mg和Al分别投入质量相等且足量的稀硫酸中,充分反应后所得两种溶液的质量相等,则投入Mg和Al的质量比是_____ ;现有一定量的乙醇与氧气混合于密闭容器内,在一定条件下恰好完全反应生成5.4gH2O,同时得到CO和CO2得混合物7.2g,该反应的化学方程式为___________ 。
更新时间:2024-01-15 18:09:37
|
相似题推荐
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐1】碳酸钙广泛应用于塑料、造纸、日化等行业,下图是用电石渣废渣制备纳米碳酸钙的工艺流程,回答问题。
(资料卡片):①NH3极易溶于水,溶于水生成NH3﹒H2O。
②电石渣浸取液碳化的反应化学方程式为: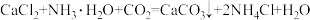 。
。
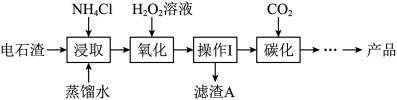
(1)浸取时,电石渣中Ca(OH)2和NH4Cl溶液反应的化学方程式为______ 。
(2)操作Ⅰ的名称是______ ,实验室完成此操作所需的仪器有烧杯、漏斗、玻璃棒、______ ,玻璃棒的作用是______ 。滤渣A含多种物质,其中一种为红褐色碱类,该物质是______ (填化学式)。
(3)“……”为一系列操作,包含过滤、洗涤及干燥。洗涤(蒸馏水洗涤)时,为检验产品是否洗净,最适合的检验试剂为______ 。
A.AgNO3溶液 B.BaCl2溶液 C.NaOH溶液与湿润的红色石蕊试纸
(4)生产中,浸取逸出的少量NH3应该回收利用,此外,还可以循环使用的物质有______ 。有同学指出,“……”系列操作中过滤后的滤液及产品洗涤后的洗液不宜直接循环使用,结合下图分析,理由是______ ,改进的方法是______ 。从物质循环利用角度考虑,碳化时,可用______ 代替CO2。
A.NH4HCO3溶液 B.Na2CO3溶液 C.CO
(5)电石渣浸取时,最适合的浸取温度为40℃,结合下图分析,理由是______ 。
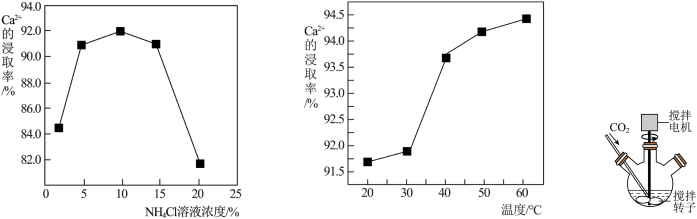
(6)上如图是电石渣浸取液碳化时的实验装置图,碳化时,需打开搅拌器搅拌,这既能搅拌反应液,还能______ ,使碳化更充分。
(7)现有10吨电石渣,经测定其中Ca(OH)2含量为90%,Ca2+的浸取率为95%(假设电石渣中其他物质中不含钙元素,其他生产环节Ca元素无损失),则理论上可得______ 吨纳米碳酸钙,(精确到小数点后2位)。
(资料卡片):①NH3极易溶于水,溶于水生成NH3﹒H2O。
②电石渣浸取液碳化的反应化学方程式为:
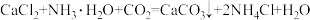 。
。
(1)浸取时,电石渣中Ca(OH)2和NH4Cl溶液反应的化学方程式为
(2)操作Ⅰ的名称是
(3)“……”为一系列操作,包含过滤、洗涤及干燥。洗涤(蒸馏水洗涤)时,为检验产品是否洗净,最适合的检验试剂为
A.AgNO3溶液 B.BaCl2溶液 C.NaOH溶液与湿润的红色石蕊试纸
(4)生产中,浸取逸出的少量NH3应该回收利用,此外,还可以循环使用的物质有
A.NH4HCO3溶液 B.Na2CO3溶液 C.CO
(5)电石渣浸取时,最适合的浸取温度为40℃,结合下图分析,理由是

(6)上如图是电石渣浸取液碳化时的实验装置图,碳化时,需打开搅拌器搅拌,这既能搅拌反应液,还能
(7)现有10吨电石渣,经测定其中Ca(OH)2含量为90%,Ca2+的浸取率为95%(假设电石渣中其他物质中不含钙元素,其他生产环节Ca元素无损失),则理论上可得
您最近一年使用:0次
填空与简答-简答题
|
较难
(0.4)
解题方法
【推荐2】质量守恒定律的发现对化学的发展做出了重要贡献。
(一)质量守恒定律的验证。
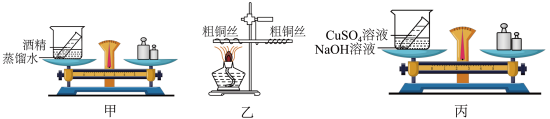
(1)①如图所示,不遵守质量守恒定律的是_______ (填“甲”、“乙”或“丙”)。
②乙中产生的实验现象是______ (填“左端下沉”、“右端下沉”或“保持平衡”),原因是________ 。
③写出丙中发生反应的化学方程式_________ 。
(二)质量守恒定律的应用。
(2)一定条件下,在一密闭容器内有A、B、C、D四种物质发生化学反应。其中A、B、C的微观示意图和反应前后各物质的质量如下表所示:
则x的值为________ ,D的元素组成为_________ 。
(一)质量守恒定律的验证。

(1)①如图所示,不遵守质量守恒定律的是
②乙中产生的实验现象是
③写出丙中发生反应的化学方程式
(二)质量守恒定律的应用。
(2)一定条件下,在一密闭容器内有A、B、C、D四种物质发生化学反应。其中A、B、C的微观示意图和反应前后各物质的质量如下表所示:
| 物质 | A | B | C | D |  |
| 微观示意图 |  |  |  | ||
| 反应前质量/g | 100 | 1 | 1 | 46 | |
| 反应后质量/g | 4 | 89 | 55 | x |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐1】在一定条件下,一氧化碳和氢气可以在固体催化剂的作用下转化为气体 A,其反应的微观粒子示意图如下所示:
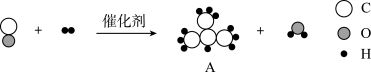
(1)写出该反应的化学方程式________ 。
(2)在密闭容器中加入一定量的一氧化碳和氢气,一定条件下发生上述反应。反应结束后恢复至室温,测得容器内气态物质中氢元素的质量分数为 20%,则起始时加入的一氧化碳与氢气的质量比为________ 。

(1)写出该反应的化学方程式
(2)在密闭容器中加入一定量的一氧化碳和氢气,一定条件下发生上述反应。反应结束后恢复至室温,测得容器内气态物质中氢元素的质量分数为 20%,则起始时加入的一氧化碳与氢气的质量比为
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐2】氧化镁在医药、建筑等行业应用广泛。以菱镁矿(主要成分为MgCO3,含少量FeCO3和不溶性杂质)为原料制备高纯氧化镁的实验流程如下图:
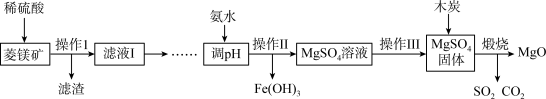
(1)FeCO3读作___________ 。
(2)“酸溶”过程主要发生复分解反应,推断溶液I中主要的金属阳离子有___________ 。
(3)通过加入氨水使溶液的pH___________ (填“增大”“减小”或“不变”),将杂质离子沉淀除去。
(4)“高温煅烧”生成的SO2和CO2质量比为___________ 。
(5)100t含杂质16%(杂质不含镁元素)的菱镁矿经过此流程,理论上可制得氧化镁的质量为___________ t。
(6)为了探究工业生产中最佳的实验条件,提升硫酸镁固体的转化率,实验小组进行了以下实验,并得到如下数据:
分析以上数据,工业生产中采用实验___________ (填编号)的条件更合理。

(1)FeCO3读作
(2)“酸溶”过程主要发生复分解反应,推断溶液I中主要的金属阳离子有
(3)通过加入氨水使溶液的pH
(4)“高温煅烧”生成的SO2和CO2质量比为
(5)100t含杂质16%(杂质不含镁元素)的菱镁矿经过此流程,理论上可制得氧化镁的质量为
(6)为了探究工业生产中最佳的实验条件,提升硫酸镁固体的转化率,实验小组进行了以下实验,并得到如下数据:
| 编号 | 矿石质量/g | 温度/℃ | m(MgSO4):m(C) | 时间/h | 硫酸镁的转化率/% |
| 1 | 85.71 | 600 | 1:1 | 0.5 | 49.98 |
| 2 | 85.71 | 650 | 2:1 | 0.5 | 65.34 |
| 3 | 85.71 | 600 | 2:1 | 0.5 | 56.39 |
| 4 | 85.71 | 650 | 2:1 | 1 | 80.76 |
| 5 | 85.71 | 800 | 8:1 | 2 | 98.12 |
| 6 | 85.71 | 850 | 8:1 | 3 | 98.48 |
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
名校
解题方法
【推荐3】2016年1月29日《科技日报》报道:科学家首次将从空气捕获的二氧化碳用氢气将其转化为甲醇,该研究即可除去大气中的温室气体二氧化碳,生成的甲醇还能作为汽油的替代燃料。二氧化碳转化成甲醇的微观示意图,如下图所示。

(1)请写出这一反应的化学方程式________ ,反应物中单质和化合物的质量比为_______ 。
(2)取4.8g的甲醇和6.4gO2在密闭容器中点燃,恰好完全反应,生成4.4gCO2,5.4gH2O和Xg物质W,请写出该反应的化学方程式______ 。

(1)请写出这一反应的化学方程式
(2)取4.8g的甲醇和6.4gO2在密闭容器中点燃,恰好完全反应,生成4.4gCO2,5.4gH2O和Xg物质W,请写出该反应的化学方程式
您最近一年使用:0次
【推荐1】由于高铁列车车厢是密闭的空间,因此需要提供清洁的空气和保持车厢的卫生。高铁酸钠(Na2FeOx)是高铁上常用的一种“绿色、环保、高效”的消毒剂。
(1)已知高铁酸钠的相对分子质量为166,则x的值为____________ 。
(2)____________ 克的高铁酸钠中含有4.6克的钠元素。
(3)C2H4和C2H6O的混合物中,碳元素的质量分数为60%,则混合物中氧元素的质量分数为____________ 。(保留小数点后一位)
(1)已知高铁酸钠的相对分子质量为166,则x的值为
(2)
(3)C2H4和C2H6O的混合物中,碳元素的质量分数为60%,则混合物中氧元素的质量分数为
您最近一年使用:0次
填空与简答-填空题
|
较难
(0.4)
解题方法
【推荐2】我国航空航天事业取得令人瞩目的成就。
(1)长征五号B运载火箭的推进剂中有液氢和液氧。写出氢气在氧气中燃烧的化学方程式:_________ 。
(2)中国天宫空间站中常用水气整合系统实现CO2的清除和O2的再生(简易流程如下图)。
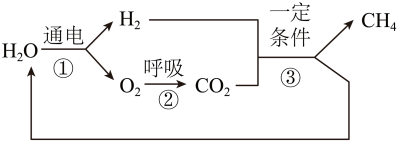
写出反应③的化学方程式:_______ 。分析流程可知,可循环利用的化合物有__________ (填一种即可)。
(3)在月球建设基地的一个前提就是在月球上大规模制造O2,在月球上可以电解熔融月壤(含SiO2、FeO、CaO、Al2O3等)制造氧气。理论上,电解等质量的下列氧化物,产生氧气最多的是 。
(1)长征五号B运载火箭的推进剂中有液氢和液氧。写出氢气在氧气中燃烧的化学方程式:
(2)中国天宫空间站中常用水气整合系统实现CO2的清除和O2的再生(简易流程如下图)。

写出反应③的化学方程式:
(3)在月球建设基地的一个前提就是在月球上大规模制造O2,在月球上可以电解熔融月壤(含SiO2、FeO、CaO、Al2O3等)制造氧气。理论上,电解等质量的下列氧化物,产生氧气最多的是 。
| A.SiO2 | B.FeO | C.CaO | D.Al2O3 |
您最近一年使用:0次
填空与简答-流程题
|
较难
(0.4)
名校
解题方法
【推荐3】某校兴趣小组欲利用Mg(OH)2和Cu2O的混合物制备MgCl2和金属铜。该小组设计了如图的实验流程,回答下列有关问题:
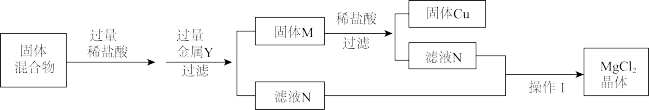
(1)Cu2O是红色固体,它与稀盐酸反应产生红色固体单质和蓝色溶液,则该反应的化学方程式为__ 。
(2)加入过量的金属Y时,发生的化学方程式为____ 。(写1个)固体M的成分____ (填名称)。
(3)MgCl2的溶解度受温度的影响较小,则操作Ⅰ为_____ 。实际操作时会向固体M中加入过量的稀盐酸,这一操作并不会让最终产品MgCl2里出现新杂质,请说明理由____ 。
(4)若混合物中Cu2O的质量为2.88g,则理论上得到Cu的质量为_____ g。
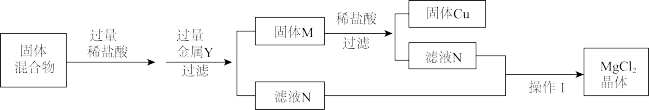
(1)Cu2O是红色固体,它与稀盐酸反应产生红色固体单质和蓝色溶液,则该反应的化学方程式为
(2)加入过量的金属Y时,发生的化学方程式为
(3)MgCl2的溶解度受温度的影响较小,则操作Ⅰ为
(4)若混合物中Cu2O的质量为2.88g,则理论上得到Cu的质量为
您最近一年使用:0次



