化学是一门以实验为基础的科学。请回答以下问题。
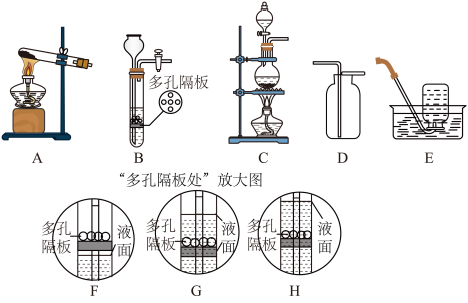
(1)图1中A作为高锰酸钾制氧气发生装置,在试管口塞一团棉花,其作用是________ ,此反应出现的物质中,锰元素化合价有________ 种。根据物质的命名规则,CaMnO4的名称为________ 。
(2)加热KClO3制氧气(取1.5gMnO2作催化剂),分离KClO3完全分解后的残留固体。
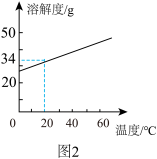
①KCl溶解度曲线如图2所示。将上述残留固体冷却至室温(20℃),称得其质量为4.9g。将KCl全部溶解,至少应加入该温度下蒸馏水的体积约________ (填序号,水的密度看成是1g/mL)。
a.5 mL b.10 mL c.20 mL d.30 mL
②对溶解后所得混合物进行过滤,从滤液中获得KCl晶体的最佳方法是________ 。
(3)实验室制二氧化碳的化学方程式为________ ;用B装置制二氧化碳气体时,关闭活塞,多孔隔板处会依次观察到的现象是________ (用图3中F、G、H排序)。某同学操作时发现关闭活塞后,固液无法分离,原因可能是________ (填序号)。
A.装置气密性不好
B.盐酸浓度偏大
C.大理石颗粒变小掉到多孔隔板以下
(4)实验室制氯气的原理是: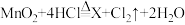 ,推测X的化学式为
,推测X的化学式为________ ,实验室制氯气的发生装置可选用________ (填字母,装置从A至E中选)。

(1)图1中A作为高锰酸钾制氧气发生装置,在试管口塞一团棉花,其作用是
(2)加热KClO3制氧气(取1.5gMnO2作催化剂),分离KClO3完全分解后的残留固体。

①KCl溶解度曲线如图2所示。将上述残留固体冷却至室温(20℃),称得其质量为4.9g。将KCl全部溶解,至少应加入该温度下蒸馏水的体积约
a.5 mL b.10 mL c.20 mL d.30 mL
②对溶解后所得混合物进行过滤,从滤液中获得KCl晶体的最佳方法是
(3)实验室制二氧化碳的化学方程式为
A.装置气密性不好
B.盐酸浓度偏大
C.大理石颗粒变小掉到多孔隔板以下
(4)实验室制氯气的原理是:
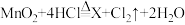 ,推测X的化学式为
,推测X的化学式为
更新时间:2024-02-05 02:00:14
|
相似题推荐
实验题
|
适中
(0.65)
真题
解题方法
【推荐1】盐酸、硫酸和硝酸都是重要的酸,下列是探究酸性质的实验。

(1)能区分稀盐酸和稀硫酸的是____ (选填“实验一”“实验二”),此实验中观察到的现象是___ ;
(2)若实验二中稀硫酸和硝酸钡溶液恰好完全反应,反应的化学方程式为___ ;如图是装有稀硫酸的试管中加入硝酸钡溶液前后主要离子种类及个数比变化示意图,则“ ”代表的离子是
”代表的离子是___ (填离子符号);

(3)实验三稀盐酸中无明显现象;稀硝酸中的现象为铜片逐渐溶解,溶液变蓝,并有气泡产生,反应为3Cu+8HNO3===3Cu(NO3)2+2X↑+4H2O,则X的化学式为___ ;
(4)实验室利用氢气还原氧化铜后,试管内壁上常附着一些铜,清洗方法是____ 。

(1)能区分稀盐酸和稀硫酸的是
(2)若实验二中稀硫酸和硝酸钡溶液恰好完全反应,反应的化学方程式为
 ”代表的离子是
”代表的离子是
(3)实验三稀盐酸中无明显现象;稀硝酸中的现象为铜片逐渐溶解,溶液变蓝,并有气泡产生,反应为3Cu+8HNO3===3Cu(NO3)2+2X↑+4H2O,则X的化学式为
(4)实验室利用氢气还原氧化铜后,试管内壁上常附着一些铜,清洗方法是
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐2】气焊和气割都需要用到乙炔。乙炔俗称电石气(化学式为C2H2),是一种无色无味的气体,密度比空气略小,难溶于水。实验室常用块状固体碳化钙(CaC2)与水反应制备乙炔,该反应比二氧化锰催化过氧化氢分解更加剧烈。请回答:
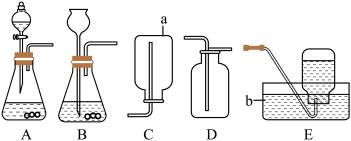
(1)图中仪器a的名称是____ ,b的名称是____ 。
(2)写出乙炔的物理性质之一:_____ 。
(3)从图中选择实验室制备乙炔所用仪器的最佳组合是____ (填序号)。
(4)碳化钙(CaC2)与水反应的化学方程式为CaC2+2H2O=X+C2H2↑,X是一种碱,则X的化学式为_____ 。

(1)图中仪器a的名称是
(2)写出乙炔的物理性质之一:
(3)从图中选择实验室制备乙炔所用仪器的最佳组合是
(4)碳化钙(CaC2)与水反应的化学方程式为CaC2+2H2O=X+C2H2↑,X是一种碱,则X的化学式为
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐3】甲、乙、丙三位同学在活动课上探究气体的制备。利用下图所示装置制取常见的气体,并对它们的有关性质进行研究,请根据题意回答下列问题。
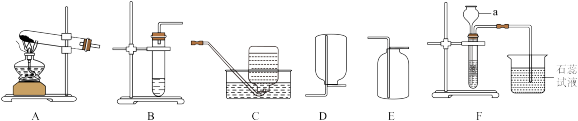
(1)实验仪器a的名称是___________
(2)甲同学用KMnO4固体制取O2,发生装置应选用上图中的___________ 装置(填编号),该反应的化学方程式为 _____________ ;排水法,当O2收集满并取出集气瓶后,停止该实验的正确操作方法是 ___________ 。
(3)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象解释不合理的是_______ (填序号)
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(4)丙同学在实验室氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。
①制取氨气反应的化学方程式 2NH4Cl + Ca(OH)2 CaCl2 + 2NH3↑+ 2X。X的化学式为:
CaCl2 + 2NH3↑+ 2X。X的化学式为:_______________ 。
②制取并收集NH3,应该从上图中选择的收集装置是_______________ 。

(1)实验仪器a的名称是
(2)甲同学用KMnO4固体制取O2,发生装置应选用上图中的
(3)乙同学用浓盐酸与大理石在F装置中反应,制取CO2并检验其有关性质,观察到烧杯中紫色石蕊试液变红,对这一现象解释不合理的是
a.产生的CO2直接使石蕊变红
b.产生的CO2与H2O反应生成H2CO3,使石蕊试液变红
c.挥发出的氯化氢溶于水,使石蕊试液变红
(4)丙同学在实验室氯化铵固体与碱石灰固体共热来制取氨气(NH3)。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水。
①制取氨气反应的化学方程式 2NH4Cl + Ca(OH)2
 CaCl2 + 2NH3↑+ 2X。X的化学式为:
CaCl2 + 2NH3↑+ 2X。X的化学式为:②制取并收集NH3,应该从上图中选择的收集装置是
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】化学是一门以实验为基础的科学。请根据实验装置图,回答下列问题。
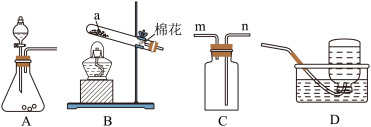
(1)图中标有 的仪器名称为
的仪器名称为______ 。
(2)实验室用装置____ 制取CO2,若用装置C进行收集,气体应从____ (填 “m”或“n”)端进入。
(3)实验室用装置B制取氧气的化学反应原理是_______________ (用化学方程式表示)。

(1)图中标有
 的仪器名称为
的仪器名称为(2)实验室用装置
(3)实验室用装置B制取氧气的化学反应原理是
您最近一年使用:0次
【推荐2】根据下图所示装置回答问题:

(1)写出有标号的仪器名称:①_____ ②_____ ③_____ 。
(2)实验室用大理石和稀盐酸反应制取二氧化碳,该反应的化学方程式为_____ 。应选用的发生装置是_____ ,收集装置是_____ ,请写出用该装置收集二氧化碳时的验满方法:_____ 。
(3)实验室用A装置加热高锰酸钾的方法制取氧气,需要改进的是_____ ,反应的化学方程式为_____ 。若用F收集并测量制得氧气的体积,需在瓶内先装满水,气体从_____ (填“a”或“b”)处导管通入。
(4)下列反应可使用A装置进行实验的是(填序号)_____ 。
①锌和稀硫酸制氢气 ②一氧化碳还原氧化铁 ③木炭还原氧化铜

(1)写出有标号的仪器名称:①
(2)实验室用大理石和稀盐酸反应制取二氧化碳,该反应的化学方程式为
(3)实验室用A装置加热高锰酸钾的方法制取氧气,需要改进的是
(4)下列反应可使用A装置进行实验的是(填序号)
①锌和稀硫酸制氢气 ②一氧化碳还原氧化铁 ③木炭还原氧化铜
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐3】实验室利用高锰酸钾加热制取氧气,并用排水集气法收集。根据实验要求和可供选择的仪器,回答下列问题。
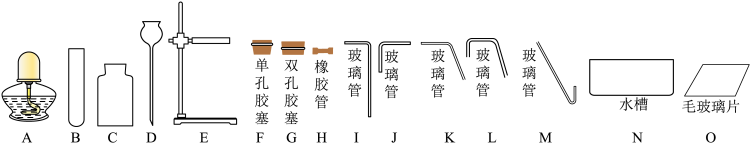
(1)仪器B 的名称是_____ 。仪器E的名称是_____ 。
(2)发生反应的化学方程式为:_____ 。
(3)组装整套装置时,需选用图中的B、C、E、F、H、K、M、O以及_____ 和_____ ;装入药品后,还需在试管口放_____ 。
(4)收集氧气的操作如下,其正确顺序为_____ 。
a.当气泡连续并比较均匀地放出时,再将导管口伸入盛满水的集气瓶
b.当气体收集满时,在水面下用玻璃片盖住瓶口,移出水面正放在桌面上
C.将集气瓶盛满水,用玻璃片盖住瓶口,倒立在盛水的水槽内

(1)仪器B 的名称是
(2)发生反应的化学方程式为:
(3)组装整套装置时,需选用图中的B、C、E、F、H、K、M、O以及
(4)收集氧气的操作如下,其正确顺序为
a.当气泡连续并比较均匀地放出时,再将导管口伸入盛满水的集气瓶
b.当气体收集满时,在水面下用玻璃片盖住瓶口,移出水面正放在桌面上
C.将集气瓶盛满水,用玻璃片盖住瓶口,倒立在盛水的水槽内
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐1】请根据下列装置图,回答有关问题。

(1)用高锰酸钾制取氧气可选用装置_____ (填字母)和E组合,反应的化学方程式为_____ ,可选装置E来收集氧气的原因是_____ 。
(2)实验室用大理石与稀盐酸制取二氧化碳的化学方程式为_____ 。选用装置C相对B的优点是_____ 。
(3)稀盐酸(1:2)是指浓盐酸与水按体积比1:2进行混合所得的盐酸。已知所用浓盐酸的溶质的质量分数为37%,密度为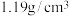 ;水的密度为
;水的密度为 。用50mL此浓盐酸最多能制得稀盐酸(1:2)的质量为
。用50mL此浓盐酸最多能制得稀盐酸(1:2)的质量为_____ 克,配制时该操作步骤顺序为_____ (填字母)。
a.称量b.混匀c.计算d.量取e.溶解f.装瓶并贴上标签

(1)用高锰酸钾制取氧气可选用装置
(2)实验室用大理石与稀盐酸制取二氧化碳的化学方程式为
(3)稀盐酸(1:2)是指浓盐酸与水按体积比1:2进行混合所得的盐酸。已知所用浓盐酸的溶质的质量分数为37%,密度为
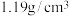 ;水的密度为
;水的密度为 。用50mL此浓盐酸最多能制得稀盐酸(1:2)的质量为
。用50mL此浓盐酸最多能制得稀盐酸(1:2)的质量为a.称量b.混匀c.计算d.量取e.溶解f.装瓶并贴上标签
您最近一年使用:0次
实验题
|
适中
(0.65)
解题方法
【推荐2】根据下图中的实验装置回答问题。

(1)若组合A和D装置制取氧气,试管中发生反应的化学方程式为______ ,装置中棉花团的作用是______ ;当观察到______ 时,便可开始收集;实验结束后应首先进行的操作是______ (填“将导管从水槽中移出”或“熄灭酒精灯”)。
(2)B和C都可以作制取二氧化碳发生装置,C与B相比,其优点是______ ;通常不用D装置收集二氧化碳的原因是______ ;若用E装置收集二氧化碳,验满时,燃着木条应放在______ 端(填“a”或“b”)。

(1)若组合A和D装置制取氧气,试管中发生反应的化学方程式为
(2)B和C都可以作制取二氧化碳发生装置,C与B相比,其优点是
您最近一年使用:0次
【推荐3】实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
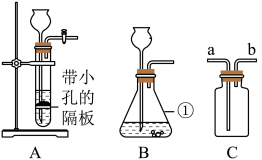
(1)仪器①的名称为__________________ 。
(2)装置A、B均可用来制取CO2气体,比较两个装置,指出A装置的一个突出优点________________________________________ 。
(3)写出用恰当试剂制取CO2气体的化学方程式________________________ 。
(4)C装置充满水时,可作为O2的收集装置,则O2应从______ 端通入。若采用排空气法收集O2,则O2应从 ______ 端通入。

(1)仪器①的名称为
(2)装置A、B均可用来制取CO2气体,比较两个装置,指出A装置的一个突出优点
(3)写出用恰当试剂制取CO2气体的化学方程式
(4)C装置充满水时,可作为O2的收集装置,则O2应从
您最近一年使用:0次
实验题
|
适中
(0.65)
【推荐1】如图是NaCl和KNO3的溶解度曲线图,根据图回答:
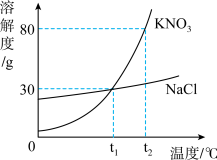
(1)t1℃时, NaCl的溶解度是_______ g;
(2)t2℃时,在100g水中加入50g KNO3晶体,充分溶解后,得到的是KNO3的____________ (填“饱和”或“不饱和”)溶液;
(3)要使NaCl溶液析出大量晶体,适宜的方法是________ 结晶法(填“蒸发”或“降温”)。

(1)t1℃时, NaCl的溶解度是
(2)t2℃时,在100g水中加入50g KNO3晶体,充分溶解后,得到的是KNO3的
(3)要使NaCl溶液析出大量晶体,适宜的方法是
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
【推荐2】R是硝酸钾或氯化铵中的一种,硝酸钾和氯化铵的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验。

(1)t2℃时,比较硝酸钾和氯化铵的饱和溶液中溶质质量分数的大小关系是硝酸钾____________ 氯化铵(选填“大于”、“小于”或“等于”)。
(2)根据以上图 1、图 2 信息可推出 R 是_____________ (填“KNO3”或“NH4Cl”)。
(3)关于图 2 中烧杯内的物质,以下几种说法正确的有____ (填字母)。
A ①和②的溶液中,溶质质量相等
B 若使③中的固体溶解,可采用加水或升温的方法
C ①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
(4)欲将 100g 溶质质量分数为 20%的硝酸钾溶液稀释为 10%的硝酸钾溶液备用,所需水的体积为_________ mL。

(1)t2℃时,比较硝酸钾和氯化铵的饱和溶液中溶质质量分数的大小关系是硝酸钾
(2)根据以上图 1、图 2 信息可推出 R 是
(3)关于图 2 中烧杯内的物质,以下几种说法正确的有
A ①和②的溶液中,溶质质量相等
B 若使③中的固体溶解,可采用加水或升温的方法
C ①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数小
(4)欲将 100g 溶质质量分数为 20%的硝酸钾溶液稀释为 10%的硝酸钾溶液备用,所需水的体积为
您最近一年使用:0次
实验题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室里有一瓶标签残缺的盐酸。为了粗略测定该盐酸的溶质质量分数,需要配制4%的氢氧化钠与盐酸进行中和反应的滴定实验。
(1)其中配制100g的4%的NaOH溶液的基本步骤是:称取氢氧化钠固体一量取水→溶解→装瓶→_____ 。
①称取氢氧化钠固体的质量是_____ 。
②用托盘天平称量(称量前已经调平衡)所需的氢氧化钠质量时,如果发现托盘天平的指针偏向左盘,此时应该_____ 直至天平平衡为止。
A 向左盘加入适量的氢氧化钠固体
B 减少左盘中适量的氢氧化钠固体
C 向右盘添加砝码
D 调节游码
③已知水的密度为1g/cm3,用100mL量筒量取所需的水,如图量筒内画出了水的液面。
(2)中和反应,要中和10g盐酸需要上述NaOH溶液20g,则该盐酸的溶质质量分数是_____ 。

(3)如图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线。

①当温度_____ 时,氯化钠的溶解度大于碳酸钠的溶解度。
②生活在盐湖附近的人们习惯“夏日晒盐,冬天捞碱”。请你解释原因:“冬日捞碱”_____ 。
(1)其中配制100g的4%的NaOH溶液的基本步骤是:称取氢氧化钠固体一量取水→溶解→装瓶→
①称取氢氧化钠固体的质量是
②用托盘天平称量(称量前已经调平衡)所需的氢氧化钠质量时,如果发现托盘天平的指针偏向左盘,此时应该
A 向左盘加入适量的氢氧化钠固体
B 减少左盘中适量的氢氧化钠固体
C 向右盘添加砝码
D 调节游码
③已知水的密度为1g/cm3,用100mL量筒量取所需的水,如图量筒内画出了水的液面。
(2)中和反应,要中和10g盐酸需要上述NaOH溶液20g,则该盐酸的溶质质量分数是

(3)如图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线。

①当温度
②生活在盐湖附近的人们习惯“夏日晒盐,冬天捞碱”。请你解释原因:“冬日捞碱”
您最近一年使用:0次



