海水是巨大的资源宝库。
Ⅰ、利用海水提取粗盐,流程如下。

(1)装置M是______ (填“蒸发池”或“过滤池”)。
(2)根据海水晒盐的原理,下列说法中不正确的是______(填序号)。
Ⅱ、利用从海水中提取出来的粗盐(杂质为不溶性泥沙),先进行提纯,后将得到的氯化钠来配制100g质量分数为12%的氯化钠溶液。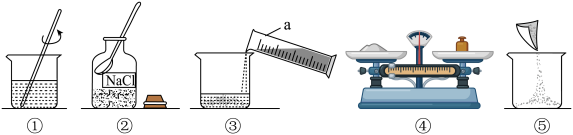
(3)需称取氯化钠的质量为______ 。
(4)图示实验中,正确的操作顺序为______(填序号)。
(5)仪器a的名称是______ ,步骤①中玻班棒的作用是______ 。
(6)①若称量氯化钠固体时托盘天平指针向右偏转,则应______ 直到天平平衡。
②下列错误操作可能导致溶质质量分数小于12%的是______ (填序号)。
A.所称取的氯化钠固体不纯 B.向烧杯中倒水溶解时部分水酒出
C.装瓶时部分溶液洒出 D.量取水时仰视读数
(7)医疗上常用0.9%的氯化钠溶液作为生理盐水。现要配制该生理盐水1000g,需要质量分数为12%的氯化钠溶液______ g,加水______ mL(水的密度为1g/mL)。
Ⅰ、利用海水提取粗盐,流程如下。

(1)装置M是
(2)根据海水晒盐的原理,下列说法中不正确的是______(填序号)。
| A.海水进入贮水池,海水的成分基本不变 | B.在M中,海水中氯化钠的质量逐渐增加 |
| C.在M中,海水中水的质盘逐渐减少 | D.析出晶体后的母液是氯化钠的不饱和溶液 |
Ⅱ、利用从海水中提取出来的粗盐(杂质为不溶性泥沙),先进行提纯,后将得到的氯化钠来配制100g质量分数为12%的氯化钠溶液。

(3)需称取氯化钠的质量为
(4)图示实验中,正确的操作顺序为______(填序号)。
| A.④②③⑤① | B.②④③⑤① | C.②④⑤③① | D.③②④⑤① |
(5)仪器a的名称是
(6)①若称量氯化钠固体时托盘天平指针向右偏转,则应
②下列错误操作可能导致溶质质量分数小于12%的是
A.所称取的氯化钠固体不纯 B.向烧杯中倒水溶解时部分水酒出
C.装瓶时部分溶液洒出 D.量取水时仰视读数
(7)医疗上常用0.9%的氯化钠溶液作为生理盐水。现要配制该生理盐水1000g,需要质量分数为12%的氯化钠溶液
更新时间:2024-02-05 19:50:26
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】下列各图是【实验一】“除去粗盐中难溶性杂质”和【实验二】“配制一定溶质质量分数的氯化钠溶液”两个实验的部分实验操作的示意图。请完成下列问题:
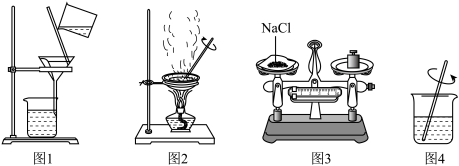
(1)以上两个实验操作过程中,都用到的实验操作是___________ (写操作名称);
(2)图1中,若过滤后发现滤液仍然浑浊,可能的原因是(仪器是洁净的)_____ (回答一点即可);
(3)图2中,玻璃棒的作用是___________ 。在进行蒸发操作时,当蒸发皿中___________ 时停止加热,用蒸发皿的余热使剩余水分蒸干;
(4)某小组同学要配制100g溶质质量分数是10%的氯化钠溶液,在量取所需水量时,应选择___________ (10、20、50、100、200)mL的量筒。要把所需氯化钠固体放在质量为22.9g的烧杯中称量,在托盘天平的托盘上已放有30g的砝码,则游码位置应拨到下图中的___________ (填字母代号);
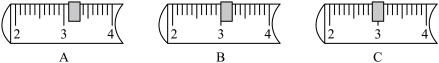
(5)用提纯后得到的氯化钠配制溶液,经检测发现配制得到的溶液溶质质量分数偏小。你认为可能的原因是下列中的___________ (填写代号)(每步操作不影响其他操作);
①将称好的氯化钠固体转移到烧杯中时有洒落 ②量取水的体积读数时俯视
③转移氯化钠溶液后发现烧杯底部有少量未溶固体 ④转移溶液时有少许溶液洒落

(1)以上两个实验操作过程中,都用到的实验操作是
(2)图1中,若过滤后发现滤液仍然浑浊,可能的原因是(仪器是洁净的)
(3)图2中,玻璃棒的作用是
(4)某小组同学要配制100g溶质质量分数是10%的氯化钠溶液,在量取所需水量时,应选择

(5)用提纯后得到的氯化钠配制溶液,经检测发现配制得到的溶液溶质质量分数偏小。你认为可能的原因是下列中的
①将称好的氯化钠固体转移到烧杯中时有洒落 ②量取水的体积读数时俯视
③转移氯化钠溶液后发现烧杯底部有少量未溶固体 ④转移溶液时有少许溶液洒落
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】溶液在日常生活中应用广泛,请根据下图回答相关问题。

(1) P点表示____________ 。
(2) t3℃时,若将40g甲物质完全溶解于水,所得溶液的质量至少为___________ 。
(3) 现根据需要,配制t2℃时25%的丙溶液,操作方法是_____________ 。最终发现质量分数小于25%,原因可能是_______________ (只写一条即可)。
(4)若要从甲、乙的混合物中获得固体甲物质,可采用的方法是_____________ 。
(5)t3℃时,将等质量的甲、乙、丙三种固体物质分别溶于水,配成饱和溶液则三种溶液质量大小关系为_______________ (填“甲”、“乙”或“丙”,下同)。将t3℃时等质量的甲、乙、丙三种饱和溶液降温到t1℃,没有明显现象的是________________ ,溶质质量分数关系为_________________ 。

(1) P点表示
(2) t3℃时,若将40g甲物质完全溶解于水,所得溶液的质量至少为
(3) 现根据需要,配制t2℃时25%的丙溶液,操作方法是
(4)若要从甲、乙的混合物中获得固体甲物质,可采用的方法是
(5)t3℃时,将等质量的甲、乙、丙三种固体物质分别溶于水,配成饱和溶液则三种溶液质量大小关系为
您最近一年使用:0次
【推荐3】“南风之时兮,可以阜吾民之财兮”这首上古歌谣说的是夏季南风一吹,盐池隔宿成盐,带来巨大财富。
(1)从盐水中得到食盐,需进行蒸发结晶。下图中能反映水在该操作中发生变化的微观示意图是 (填字母,“•”表示氧原子,“。”表示氢原子)
(2)劳动致富过程中,用溶质质量分数为16%的NaCl溶液来选种。其原理是:饱满种子的密度比16%NaCl溶液的密度略大,而干瘪种子的密度比16%NaCl 溶液的密度小得多。

①某同学将若干南瓜种子放入配制好的溶液中进行选种。如果观察到大多数南瓜种子_________ ,说明大多数种子都不够饱满。
②若配制5kg 16%的 NaCl 溶液,需要 NaCl 固体的质量为_________ g。根据 NaCl 溶解度曲线判断,此溶液_________ (填“是”或“不是”)  时NaCl的饱和溶液。
时NaCl的饱和溶液。
(1)从盐水中得到食盐,需进行蒸发结晶。下图中能反映水在该操作中发生变化的微观示意图是 (填字母,“•”表示氧原子,“。”表示氢原子)
A. | B. | C. | D. |
(2)劳动致富过程中,用溶质质量分数为16%的NaCl溶液来选种。其原理是:饱满种子的密度比16%NaCl溶液的密度略大,而干瘪种子的密度比16%NaCl 溶液的密度小得多。

①某同学将若干南瓜种子放入配制好的溶液中进行选种。如果观察到大多数南瓜种子
②若配制5kg 16%的 NaCl 溶液,需要 NaCl 固体的质量为
 时NaCl的饱和溶液。
时NaCl的饱和溶液。
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】硫酸是工农业生产中使用非常广泛的一种试剂,实验室用质量分数为98%的浓硫酸(密度为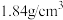 )配制49g质量分数为20%的硫酸。
)配制49g质量分数为20%的硫酸。
(1)经计算,所需水的质量为______ g,所需98%的浓硫酸的体积为______ mL(保留一位小数)。
(2)量取上述体积的浓硫酸选用的仪器为______(填选项)。
(3)如果不慎将浓硫酸沾到皮肤上,应立即______ ,然后涂上3%的小苏打溶液。
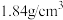 )配制49g质量分数为20%的硫酸。
)配制49g质量分数为20%的硫酸。(1)经计算,所需水的质量为
(2)量取上述体积的浓硫酸选用的仪器为______(填选项)。
| A.10mL量筒 | B.100mL烧杯 | C.100mL量筒 | D.胶头滴管 |
(3)如果不慎将浓硫酸沾到皮肤上,应立即
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】配制80g质量分数10%的氯化钠溶液实验步骤:
(1)计算:按配制要求计算所需溶质和溶剂的质量或体积,需要氯化钠的质量为_____ g,水的质量为_____ g,即_____ mL。
(2)称量:用__________ 称取所需的氯化钠,再用_____ 量取所需的水。
(3)溶解:将称量好的氯化钠倒入__________ 的烧杯中,再加入量好的水,用__________ 充分搅拌,直至氯化钠全部溶解。
(4)装瓶:把配制好的溶液装入试剂瓶中,盖好瓶塞,贴上标签,标签注明__________ 和__________ ,放入试剂柜中。
(1)计算:按配制要求计算所需溶质和溶剂的质量或体积,需要氯化钠的质量为
(2)称量:用
(3)溶解:将称量好的氯化钠倒入
(4)装瓶:把配制好的溶液装入试剂瓶中,盖好瓶塞,贴上标签,标签注明
您最近一年使用:0次
【推荐3】结合如图有关实验,回答问题。


(1)图一中,电源正极连接的电极产生的气体是____ (填化学式),该反应的符号表达式为____ ,该反应的基本反应类型是_____ 。电源负极连接的电极产生的气体具有的化学性质是_________ .
(2)图二中,过滤操作中玻璃棒的作用是_____________ .
(3)农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如图三所示。实验操作顺序为_____________ .用量筒量取水时仰视读数所得溶液的溶质质量分数______ (填“偏大”、“偏小”或“没影响”)。


(1)图一中,电源正极连接的电极产生的气体是
(2)图二中,过滤操作中玻璃棒的作用是
(3)农业上常用溶质质量分数为16%的NaCl溶液选种。实验室配制100g该溶液的过程如图三所示。实验操作顺序为
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】我国冶铜文明源远流长,凝聚了劳动人民的智慧。
Ⅰ.冶铜的发展
(1)用铜矿石与锡矿石冶铜,可得到硬度大于铜的铜锡合金。铜锡合金的熔点和硬度随其中锡含量的变化如图所示。图中表示熔点的曲线是_____ (填“a”或“b”)。铜锡合金属于_____ (填“金属”或“合成”)材料。

Ⅱ.冶铜的创新
(2)①细菌冶炼是湿法炼铜的方法之一,其原理可表示为CuFeS2+4O2 CuSO4+X,其中X的化学式为
CuSO4+X,其中X的化学式为_____ 。
②现代工业上常用电解硫酸铜溶液来制备铜,同时生成硫酸和一种能供给呼吸的气体,该反应的化学方程式为_____ 。采用恒温蒸发的方法将100kg20%的硫酸铜溶液浓缩为25%的硫酸铜溶液,需要蒸发水的质量为_____ kg。
Ⅲ.铜制品的锈蚀与防锈
(3)铜制品使用一段时间后会生锈,铜锈的主要成分为Cu2(OH)2CO3.铜生锈可能是铜与空气中氧气、水和_____ (填化学式)长时间接触导致的。请写出一种防止铜等金属制品生锈的具体方法:_____ 。
Ⅰ.冶铜的发展
(1)用铜矿石与锡矿石冶铜,可得到硬度大于铜的铜锡合金。铜锡合金的熔点和硬度随其中锡含量的变化如图所示。图中表示熔点的曲线是

Ⅱ.冶铜的创新
(2)①细菌冶炼是湿法炼铜的方法之一,其原理可表示为CuFeS2+4O2
 CuSO4+X,其中X的化学式为
CuSO4+X,其中X的化学式为②现代工业上常用电解硫酸铜溶液来制备铜,同时生成硫酸和一种能供给呼吸的气体,该反应的化学方程式为
Ⅲ.铜制品的锈蚀与防锈
(3)铜制品使用一段时间后会生锈,铜锈的主要成分为Cu2(OH)2CO3.铜生锈可能是铜与空气中氧气、水和
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】溶液与人类生产、生活密切相关。
(1)把少量下列物质分别放入水中,充分搅拌,能得到溶液的是_______ 。(填序号)
A 硝酸钾 B 植物油 C 面粉 D 蔗糖
(2)如图为甲、乙、丙三种固体物质的溶解度曲线。

①t2℃时,甲的溶解度为_______ ,该温度下,浓度最大的甲溶液溶质质量分数为_______ (保留小数点后一位)。
②m点含义_______ 。
③甲的溶解度随温度变化的规律是_______ 。
④t2℃时,甲物质饱和溶液中溶质与溶剂的质量比为_______ (填最简比)。
⑤现有t1℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是_______ (填序号):所得溶液中,溶质质量大小关系是_______ 。
A 甲>乙>丙 B 甲=乙<丙 C 甲=乙>丙 D 不能确定
(3)甲中混有少量丙,提纯甲的方法是_______ ;丙中混有少量乙,提纯丙的方法是_______ 。
(4)若用50g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为_______ g。
(1)把少量下列物质分别放入水中,充分搅拌,能得到溶液的是
A 硝酸钾 B 植物油 C 面粉 D 蔗糖
(2)如图为甲、乙、丙三种固体物质的溶解度曲线。

①t2℃时,甲的溶解度为
②m点含义
③甲的溶解度随温度变化的规律是
④t2℃时,甲物质饱和溶液中溶质与溶剂的质量比为
⑤现有t1℃时甲、乙、丙三种物质的饱和溶液,将这三种溶液分别升温到t2℃,所得溶液中溶质质量分数大小关系是
A 甲>乙>丙 B 甲=乙<丙 C 甲=乙>丙 D 不能确定
(3)甲中混有少量丙,提纯甲的方法是
(4)若用50g溶质质量分数为6%的氯化钠溶液配制溶质质量分数为3%的氯化钠溶液,需要加水的质量为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
【推荐1】同规格海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质,为了有效将粗盐提纯,实验的各步操作流程如图所示:

根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是_____ .
(2)操作Ⅰ和操作Ⅱ的名称是_____ ,该操作中需要将圆形滤纸折叠处理,下列图示中不该出现的情形是_____ (填序号).

(3)在实验过程中加入过量的NaOH溶液①的有关化学方程式是_____ .
(4)操作Ⅱ完成后产生的沉淀物的化学式是_____ 、_____ .
(5)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌 外还可采取_____ 等措施.
(6)判断加入的盐酸“适量”的方法是_____ .
(7)实验所得精盐的质量_____ (填“大于”、“小于”或“等于”)粗盐中NaCl的质量.

根据以上信息回答:
(1)在完成操作Ⅰ之前,必须加入的X物质是
(2)操作Ⅰ和操作Ⅱ的名称是

(3)在实验过程中加入过量的NaOH溶液①的有关化学方程式是
(4)操作Ⅱ完成后产生的沉淀物的化学式是
(5)在蒸发操作中容易造成食盐固体飞溅,为尽量减少飞溅,除连续搅拌 外还可采取
(6)判断加入的盐酸“适量”的方法是
(7)实验所得精盐的质量
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
【推荐2】氯化钠是重要的化工原料,氯碱工业生产的一种流程如图:

(1)从“海水→粗盐→精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是__ (填名称)。
(2)“食盐水”中常含有NaCl、MgCl2、CaCl2等物质,“精制”过程中加入NaOH的目的是__ 。
(3)写出“电解槽“中发生反应的化学方程式__ ,流程中可以循环使用的物质有__ (填化学式)。
(4)氯碱工业生产的碱样品中常含有Na2CO3和NaCl等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示
①你认为碱样品中含有Na2CO3的原因是__ ,检验碱样品中是否含有Na2CO3,下列试剂中可选择使用的是__ 。
a.酚酞 b.稀盐酸c。澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
称取20.3g碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤,干燥得到碳酸钡(BaCO3)固体0.197g;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸365g。该碱样品的等级是__ (不考虑其他杂质参加反应)。

(1)从“海水→粗盐→精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是
(2)“食盐水”中常含有NaCl、MgCl2、CaCl2等物质,“精制”过程中加入NaOH的目的是
(3)写出“电解槽“中发生反应的化学方程式
(4)氯碱工业生产的碱样品中常含有Na2CO3和NaCl等杂质,用“离子交换膜法”生产的碱样品质量主要标准如下表所示
| 等级 | 氢氧化钠含量 | 碳酸钠含量 |
| 优等品 | ≥99.0% | ≤0.5% |
| 一等品 | ≥98.5% | ≤0.8% |
| 合格品 | ≥98.0% | ≤1.0% |
a.酚酞 b.稀盐酸c。澄清石灰水
②李老师设计和完成了如下实验来判断碱样品的等级。
称取20.3g碱样品,加足量水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤,干燥得到碳酸钡(BaCO3)固体0.197g;向滤液中加入几滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5%的稀盐酸365g。该碱样品的等级是
您最近一年使用:0次
【推荐3】食盐是人类生存的必需品,通过海水晒盐和井盐开采等方式能获得食盐。
(1)海水晒盐
物质 | 每100g海水中约含的质量(g) |
H2O | 96.5 |
NaCl | 2.7 |
MgCl2 | 0.4 |
MgSO4 | 0.2 |
…… | …… |
Ⅰ.表1为某地海水中主要物质的含量,该海水中NaCl的溶质量分数为
Ⅱ.图1为NaCl、MgCl2和MgSO4的溶解度曲线。10℃时,三种物质中溶解度最小的是
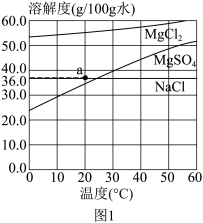
Ⅲ.我国从明代后期开始采用海滩晒盐的方法制盐,图2为某海边盐场制盐采用的主要流程。
“晒卤”的原理与粗盐提纯实验中的
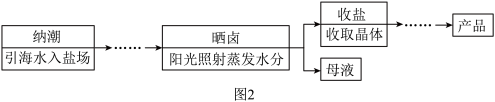
(2)井盐开采
《四川盐法志》在记载清代巴蜀之地的井盐开采时,提到获得的粗盐中含有少量的MgCl2和MgSO4等杂质。对此,古人用“花水”(饱和氯化钠溶液)洗涤粗盐以得到较纯净的食盐。请分析选择用“花水”洗涤粗盐而不用水洗涤粗盐的原因
您最近一年使用:0次




