某化学兴趣小组为测定一种石灰石样品中碳酸钙的质量分数,进行如下实验:
①分别称取两份质量为25.0g的石灰石样品,并加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的同种稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如图所示:(方程式 )。
)。
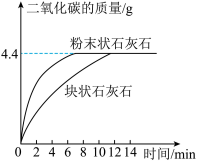
(1)由图中曲线分析得出,影响该化学反应速率的因素是_______ 。
(2)每份样品充分反应后。生成二氧化碳的质量为________ 。
(3)求该样品中碳酸钙的质量分数。
①分别称取两份质量为25.0g的石灰石样品,并加工成块状和粉末状;
②将两份样品分别投入两个锥形瓶中,各加入足量的同种稀盐酸(样品所含杂质不溶于水也不与酸反应),测得生成二氧化碳的质量与反应时间的关系如图所示:(方程式
 )。
)。
(1)由图中曲线分析得出,影响该化学反应速率的因素是
(2)每份样品充分反应后。生成二氧化碳的质量为
(3)求该样品中碳酸钙的质量分数。
更新时间:2024-02-05 23:23:57
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组的同学为了测定假黄金(铜锌合金)中铜的质量分数,取20g假黄金于烧杯中,加入100g稀盐酸,充分反应后,称得烧杯中物质的总质量为119.6g。计算:
(1)生成氢气的质量为___________ g。
(2)该假黄金中铜的质量分数。【温馨提示: 】
】
(1)生成氢气的质量为
(2)该假黄金中铜的质量分数。【温馨提示:
 】
】
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将16g含有杂质的锌粒投入到盛有足量稀硫酸的烧杯中(杂质跟稀硫酸不反应).测得加入锌粒前烧杯和稀硫酸的总质量为200g,反应停止后,烧杯和烧杯内剩余物的总质量为215.6g.求:
(1)反应中生成氢气的质量为___________ ;
(2)这16g含杂质的锌粒中金属锌的质量分数__________ .
(1)反应中生成氢气的质量为
(2)这16g含杂质的锌粒中金属锌的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】晴晴同学为测定某纯碱样品中纯碱的质量分数(杂质不与酸反应),向42.4g纯碱样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳8.8g。试计算该纯碱样品中,纯碱的质量分数是所少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取146g的稀盐酸与50g含少量杂质的石灰石恰好完全反应(杂质不与盐酸反应,也不溶于水),生成17.6g二氧化碳气体.
(1)石灰石中碳酸钙的质量分数;
(2)稀盐酸中溶质的质量分数;
(1)石灰石中碳酸钙的质量分数;
(2)稀盐酸中溶质的质量分数;
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某化学兴趣小组为测定大理石中碳酸钙的含量,将过量的稀盐酸加入到20g大理石中(其他成分不与盐酸反应),把产生的CO2气体用足量的烧碱溶液吸收,同时测量烧碱溶液增加的质量,结果如下表所示
(1)上表中,第5min时,x=________。
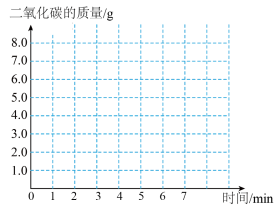
(2)请在下图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线。______
(3)计算大理石样品中碳酸钙的质量分数。______
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 增加质量/g | 0 | 3.0 | 5.0 | 6.0 | 6.6 | x | 6.6 |
(2)请在下图的坐标纸上,以时间为横坐标,以产生CO2气体的质量为纵坐标,画出能够表明产生气体的质量随时间变化规律的关系曲线。______

(3)计算大理石样品中碳酸钙的质量分数。______
您最近一年使用:0次




