酸、碱、盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出________ (填字母)。
a.H2O b.H+ c.OH- d.H2
(2)下图是实验室制取二氧化碳等常见气体的相关装置。

则实验室用稀盐酸和大理石反应制取干燥的二氧化碳,所需装置从左到右的正确连接顺序为_______ (填字母,下同)接________ 接_________ 。
(3)盐酸还能用于除铁锈,写出相关反应的化学方程式。
(4)敞口放置的氢氧化钠溶液容易变质,写出相关反应的化学方程式。
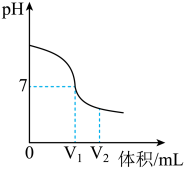
(5)利用数字化实验设备,测定氢氧化钠溶液与盐酸反应时溶液pH的变化,实验结果如图所示。该实验是将________ (填“盐酸”或“氢氧化钠溶液”)滴加到另一种溶液中:当滴入溶液为V2mL时,所得溶液中溶质的化学式为________ ;从微观角度看,该化学反应的实质是_______________ 。
(6)80g质量分数为10%的NaOH溶液与一定质量某稀硫酸恰好完全反应。请计算该一定质量稀硫酸中H2SO4的质量。
(1)酸具有相似的性质,因为不同的酸在水溶液中都能解离出
a.H2O b.H+ c.OH- d.H2
(2)下图是实验室制取二氧化碳等常见气体的相关装置。

则实验室用稀盐酸和大理石反应制取干燥的二氧化碳,所需装置从左到右的正确连接顺序为
(3)盐酸还能用于除铁锈,写出相关反应的化学方程式。
(4)敞口放置的氢氧化钠溶液容易变质,写出相关反应的化学方程式。
(5)利用数字化实验设备,测定氢氧化钠溶液与盐酸反应时溶液pH的变化,实验结果如图所示。该实验是将

(6)80g质量分数为10%的NaOH溶液与一定质量某稀硫酸恰好完全反应。请计算该一定质量稀硫酸中H2SO4的质量。
更新时间:2024-02-06 20:21:49
|
相似题推荐
综合应用题
|
适中
(0.65)
解题方法
【推荐1】实验室常利用下图所示装置完成气体制备及性质实验。请回答:

(1)指出编号仪器的名称:②_____ 。
(2)实验室制取并收集一瓶CO2,应选择的装置是_____ 。
(3)将CO2和CO的混合气体通过F装置(液体药品均足量),实验开始时关闭活塞b,打开弹簧夹a,广口瓶中观察到的现象是_____ ,此时从导管c选出的气体主要是_____ 。一段时间后,再关闭弹簧夹a,打开话塞b,将分液漏斗中的稀盐酸滴入广口瓶中,此时逸出的气体主要是_____ 。
(4)氨气(NH3)是一种无色、有刺激性气味、密度比空气的密度小、极易溶于水的气体,实验室常用氯化铵晶体与氢氧化钙粉末混合加热来制取氨气。选取上述装置,收集氨气只能选用装置_____ (填字母),其原因是_____ 。
(5)某石灰厂需要测定产品生石灰中杂质(杂质只有CaCO3)的质量分数。小刚进行了如图所示实验。请计算:

①生成CO2气体的质量_____ ;
②样品中CaCO3的质量分数_____ (要求过程)。[提示:CaO+H2O=Ca(OH)2、Ca(OH)2+2HCl=CaCl2+2H2O]

(1)指出编号仪器的名称:②
(2)实验室制取并收集一瓶CO2,应选择的装置是
(3)将CO2和CO的混合气体通过F装置(液体药品均足量),实验开始时关闭活塞b,打开弹簧夹a,广口瓶中观察到的现象是
(4)氨气(NH3)是一种无色、有刺激性气味、密度比空气的密度小、极易溶于水的气体,实验室常用氯化铵晶体与氢氧化钙粉末混合加热来制取氨气。选取上述装置,收集氨气只能选用装置
(5)某石灰厂需要测定产品生石灰中杂质(杂质只有CaCO3)的质量分数。小刚进行了如图所示实验。请计算:

①生成CO2气体的质量
②样品中CaCO3的质量分数
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】如图是几种实验室制取气体的发生装置与收集装置

(1)写出仪器名称:Ⅰ__________ ,Ⅱ__________ 。
(2)实验室用石灰石和稀盐酸制取二氧化碳,装置A比装置C好的原因是_____________ 。
(3)若用D装置收集氧气,操作的正确顺序为_________ (填编号)。
a.将导管伸入集气瓶口,气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面放置
(4)若用E装置进行排空气法收集氢气,气体应从__________ (填“a”或“b”)端通入。
(5)对于如何除去粗盐中可溶性的氯化镁和氯化钙、硫酸钠等杂质,同学们提出如图方案:

a.操作②中的物质X为_________ 。
b.操作①②顺序不能颠倒的原因是___________ 。
(6)在自来水和污水处理厂的出水阶段,广泛采用加氯消毒工艺,以杀灭水中的细菌和病毒,氯气遇水会产生次氯酸(HCIO)和盐酸,次氯酸具有净化作用,用于消毒。用71克氯气可产生多少克次氯酸?

(1)写出仪器名称:Ⅰ
(2)实验室用石灰石和稀盐酸制取二氧化碳,装置A比装置C好的原因是
(3)若用D装置收集氧气,操作的正确顺序为
a.将导管伸入集气瓶口,气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖上瓶口,将集气瓶移出水面放置
(4)若用E装置进行排空气法收集氢气,气体应从
(5)对于如何除去粗盐中可溶性的氯化镁和氯化钙、硫酸钠等杂质,同学们提出如图方案:

a.操作②中的物质X为
b.操作①②顺序不能颠倒的原因是
(6)在自来水和污水处理厂的出水阶段,广泛采用加氯消毒工艺,以杀灭水中的细菌和病毒,氯气遇水会产生次氯酸(HCIO)和盐酸,次氯酸具有净化作用,用于消毒。用71克氯气可产生多少克次氯酸?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】作为北京市区唯一新建的场馆国家速滑馆“冰丝带”,采用世界跨度最大的单层双向正交马鞍形索网屋面,用钢量仅为传统屋面的四分之一。
(1)炼钢的原材料是生铁。写出工业上用赤铁矿(主要成分是氧化铁)冶炼生铁的化学方程式______ ;
(2)为了探究铁与另外两种金属的活动性,某同学收集了包括铁在内的三种金属片,分别编号为X、Y、Z。他把X、Y 分别放入稀硫酸中,Y 溶解并产生氢气,X 不反应;把 X 和Z 分别放入硝酸银溶液中,过一会儿,在 X 表面有银析出,而 Z 没有变化。根据以上实验事实,判断铁与另外两种金属的活动性顺序______ (铁用化学式表示);
(3)国家速滑馆、五棵松体育中心等冬奥场馆,选用二氧化碳跨临界制冷系统,冰面温差控 制在 0.5℃以内,碳排量接近于零。实验室可用大理石与稀盐酸反应制取 CO2。

①选用的发生和收集装置依次是______ ;你选择上述发生装置的理由是______ ;
②向盛有 12g 大理石(杂质不参与反应)的反应容器中,加入 100g 稀盐酸,恰好完全反应后,反应容器内固体与溶液的总质量为 107.6g,则该稀盐酸的溶质质量分数为______ 。
(1)炼钢的原材料是生铁。写出工业上用赤铁矿(主要成分是氧化铁)冶炼生铁的化学方程式
(2)为了探究铁与另外两种金属的活动性,某同学收集了包括铁在内的三种金属片,分别编号为X、Y、Z。他把X、Y 分别放入稀硫酸中,Y 溶解并产生氢气,X 不反应;把 X 和Z 分别放入硝酸银溶液中,过一会儿,在 X 表面有银析出,而 Z 没有变化。根据以上实验事实,判断铁与另外两种金属的活动性顺序
(3)国家速滑馆、五棵松体育中心等冬奥场馆,选用二氧化碳跨临界制冷系统,冰面温差控 制在 0.5℃以内,碳排量接近于零。实验室可用大理石与稀盐酸反应制取 CO2。

①选用的发生和收集装置依次是
②向盛有 12g 大理石(杂质不参与反应)的反应容器中,加入 100g 稀盐酸,恰好完全反应后,反应容器内固体与溶液的总质量为 107.6g,则该稀盐酸的溶质质量分数为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐1】酸、碱、盐是几类重要化合物,它们与人类日常生活和工农业生产关系十分密切。
(1)稀盐酸和稀硫酸等酸类物质具有一些相似的性质,是因为它们在水溶液中都能解离出______ (填微粒符号)。
(2)请简述氢氧化钙(俗称熟石灰)在生产或生活中的一种用途。
(3)制取CO2后的酸性废液需处理后再排放;除去CO2常用碱液吸收法。
①检验某废液是否呈酸性,可选用的一种试剂(或用品)是_______ 。
②为探究足量NaOH溶液吸收CO2后溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH。请指出该方案中的错误并加以改正_______ 。
(4)实验室选用以下装置制取纯净、干燥的CO2,并验证其部分性质。

①装置B的作用是除去二氧化碳中混入的氯化氢气体,B装置中发生反应的化学方程式为_______ 。
②C装置中浓硫酸的作用是_______ 。
③请在D中简要补画出CO2的收集装置图_______ 。
(5)工业废水需处理达到标准后再排放,以免造成水体污染。某造纸厂欲排放200t含NaOH的废水,其中NaOH的质量分数为1.6%,用废硫酸(H2SO4的质量分数为20%)来处理该废水至中性,需要这种废硫酸的质量是多少?
(1)稀盐酸和稀硫酸等酸类物质具有一些相似的性质,是因为它们在水溶液中都能解离出
(2)请简述氢氧化钙(俗称熟石灰)在生产或生活中的一种用途。
(3)制取CO2后的酸性废液需处理后再排放;除去CO2常用碱液吸收法。
①检验某废液是否呈酸性,可选用的一种试剂(或用品)是
②为探究足量NaOH溶液吸收CO2后溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH。请指出该方案中的错误并加以改正
(4)实验室选用以下装置制取纯净、干燥的CO2,并验证其部分性质。

①装置B的作用是除去二氧化碳中混入的氯化氢气体,B装置中发生反应的化学方程式为
②C装置中浓硫酸的作用是
③请在D中简要补画出CO2的收集装置图
(5)工业废水需处理达到标准后再排放,以免造成水体污染。某造纸厂欲排放200t含NaOH的废水,其中NaOH的质量分数为1.6%,用废硫酸(H2SO4的质量分数为20%)来处理该废水至中性,需要这种废硫酸的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐2】酸、碱、盐种类繁多,与人类日常生活和工农业生产关系十分密切。
(1)稀盐酸,稀硫酸,白醋都能使紫色石蕊溶液变红,原因是它们的溶液中均含有___________ 。(填离子符号)
(2)如图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。

①根据图示判断;该实验是将___________ (填“氢氧化钠溶液”或“硫酸”)滴加到另一种溶液中。
②滴入溶液体积为V2mL,时,溶液中的溶质为___________ 。
(3)食盐(主要成分是NaCl)除可用作调味品外,还是一种重要化工原料。晾晒海水所得到的粗盐中含有不溶性杂质(泥沙)和可溶性杂质(CaCl2、MgCl2、Na2SO4);下图是某化学小组在实验室对粗盐样品进行除杂提纯的过程。

①溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是___________ 。
②加入Na2CO3溶液的作用是什么___________ ?
③固体甲的成分有哪些___________ ?(写出化学式)
(4)为探究某瓶长期敞口放置的NaOH溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH.请指出该方案中的错误并加以改正。
(5)LiOH和NaOH的化学性质相似。“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量。请计算;用LiOH完全吸收132gCO2,生成Li2CO3和H2O,理论上至少需要LiOH的质量是多少?
(1)稀盐酸,稀硫酸,白醋都能使紫色石蕊溶液变红,原因是它们的溶液中均含有
(2)如图是氢氧化钠溶液与硫酸反应时溶液pH变化的示意图。

①根据图示判断;该实验是将
②滴入溶液体积为V2mL,时,溶液中的溶质为
(3)食盐(主要成分是NaCl)除可用作调味品外,还是一种重要化工原料。晾晒海水所得到的粗盐中含有不溶性杂质(泥沙)和可溶性杂质(CaCl2、MgCl2、Na2SO4);下图是某化学小组在实验室对粗盐样品进行除杂提纯的过程。

①溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是
②加入Na2CO3溶液的作用是什么
③固体甲的成分有哪些
(4)为探究某瓶长期敞口放置的NaOH溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量Ca(OH)2溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为Na2CO3和NaOH.请指出该方案中的错误并加以改正。
(5)LiOH和NaOH的化学性质相似。“神舟”飞船内,可用盛有LiOH的过滤网吸收航天员呼出的气体,以降低CO2含量。请计算;用LiOH完全吸收132gCO2,生成Li2CO3和H2O,理论上至少需要LiOH的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
真题
解题方法
【推荐3】酸、碱、盐等物质与人类日常生活和工农业生产关系十分密切,它们的结构、性质和用途是化学学习和研究的重要内容。
(1)盐酸和硫酸具有相似的性质,是因为它们在溶液中都能解离出 (填字母序号)。
(2)某化学小组利用数字化设备,测定氢氧化钠溶液与盐酸反应时溶液pH的变化,实验结果如图所示。

①氢氧化钠和盐酸反应的化学方程式为_______ 。
②区分x点和y点所对应溶液,可选用的一种试剂为_______ 。
(3)鱼池增氧剂的主要成分是过碳酸钠(2Na2CO3•3H2O2),过碳酸钠遇热水时会分解生成碳酸钠和过氧化氢。某化学小组为研究过碳酸钠遇热水分解的性质,采用如图所示的装置进行实验。

①开始时应将过碳酸钠粉末加入_______ (填“锥形瓶”或“分液漏斗”)。
②写出A中由过氧化氢产生氧气的化学方程式_______ 。
③请在B处虚线框内画出用试管采用排空气法收集氧气的装置图____ 。
④为验证反应后A中溶液的溶质成分,某化学小组设计了如下方案:取少量A中溶液,加入足量的氢氧化钡溶液,反应后静置,取上层清液滴加酚酞溶液,发现溶液变红。请指出该方案中的错误并加以改正____ 。
(4)实验室有100一定溶质质量分数的氯化钠溶液,取该溶液于烧杯中,向其中滴加硝酸银溶液至不再产生沉淀为止,过滤、洗涤、干燥后,称得沉淀的质量为28.7g。请计算该氯化钠溶液中溶质的质量。
(1)盐酸和硫酸具有相似的性质,是因为它们在溶液中都能解离出 (填字母序号)。
| A.水分子 | B.氢离子 | C.酸根离子 | D.氢氧根离子 |

①氢氧化钠和盐酸反应的化学方程式为
②区分x点和y点所对应溶液,可选用的一种试剂为
(3)鱼池增氧剂的主要成分是过碳酸钠(2Na2CO3•3H2O2),过碳酸钠遇热水时会分解生成碳酸钠和过氧化氢。某化学小组为研究过碳酸钠遇热水分解的性质,采用如图所示的装置进行实验。

①开始时应将过碳酸钠粉末加入
②写出A中由过氧化氢产生氧气的化学方程式
③请在B处虚线框内画出用试管采用排空气法收集氧气的装置图
④为验证反应后A中溶液的溶质成分,某化学小组设计了如下方案:取少量A中溶液,加入足量的氢氧化钡溶液,反应后静置,取上层清液滴加酚酞溶液,发现溶液变红。请指出该方案中的错误并加以改正
(4)实验室有100一定溶质质量分数的氯化钠溶液,取该溶液于烧杯中,向其中滴加硝酸银溶液至不再产生沉淀为止,过滤、洗涤、干燥后,称得沉淀的质量为28.7g。请计算该氯化钠溶液中溶质的质量。
您最近一年使用:0次
【推荐1】实验室有一瓶久置的氢氧化钠固体,某同学想了解其变质情况,设计了实验,实验过程如下:
【实验一】取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是______________ (用化学方程式表 示)。
【实验二】如图过程进行实验

通过实验二,能进一步推算出氢氧化钠变质的程度,请写出计算过程(反应的化学方程式是Na2CO3+CaC12=CaCO3↓+2NaC1)
【结论】该样品属于___________ (填“全部”、“部分”)变质。
【拓展】若要获得氢氧化钠溶液,应先取一定量的固体加入足量水中充分溶解,再加入___________ ,后进行_____ 。
【实验一】取少量样品于试管中,滴加适量稀盐酸,观察到有气泡产生,说明氢氧化钠已变质,变质的原因是
【实验二】如图过程进行实验

通过实验二,能进一步推算出氢氧化钠变质的程度,请写出计算过程(反应的化学方程式是Na2CO3+CaC12=CaCO3↓+2NaC1)
【结论】该样品属于
【拓展】若要获得氢氧化钠溶液,应先取一定量的固体加入足量水中充分溶解,再加入
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐2】氢氧化钠(Sodiumhydroxide),化学式NaOH,也称苛性钠、烧碱、火碱。氢氧化钠具有强碱性,腐蚀性极强,可作酸中和剂、配合掩蔽剂、沉淀剂、沉淀掩蔽剂、显色剂、皂化剂、去皮剂、洗涤剂等,在生产和科学研究中有着广泛的应用。
(1)氢氧化钠溶液在空气中敞口放置过程中容易发生变质。
①变质的原因主要是NaOH溶液能与空气中的___________ (填化学式)发生化学反应。
②为除去该NaOH溶液中的杂质,小明同学向其中加入了适量的试剂X,出现白色沉淀,恰好完全反应后,再进行过滤,从而得到了较为纯净的NaOH溶液。
请判断他所选的试剂X是下列选项中的___________ (填选项序号之一)。
A.HCl溶液B.H2SO4溶液C.Ca(OH)2溶液D.BaCl2溶液
(2)欲测定100g某氯化镁溶液中MgCl2的质量,小明同学向其中逐滴加入溶质质量分数为8%的NaOH溶液,反应过程中产生沉淀的质量与所加入NaOH溶液的质量关系如下图所示。试回答:

①当加入NaOH溶液50g时(即图中A点),烧杯中溶液里大量存在的金属阳离子是___________ (填离子符号)。
②当加入NaOH溶液100g时(即图中B点),恰好完全反应。试通过计算求该氯化镁溶液中MgCl2的质量___________ 。(计算结果精确至0.1g)
(1)氢氧化钠溶液在空气中敞口放置过程中容易发生变质。
①变质的原因主要是NaOH溶液能与空气中的
②为除去该NaOH溶液中的杂质,小明同学向其中加入了适量的试剂X,出现白色沉淀,恰好完全反应后,再进行过滤,从而得到了较为纯净的NaOH溶液。
请判断他所选的试剂X是下列选项中的
A.HCl溶液B.H2SO4溶液C.Ca(OH)2溶液D.BaCl2溶液
(2)欲测定100g某氯化镁溶液中MgCl2的质量,小明同学向其中逐滴加入溶质质量分数为8%的NaOH溶液,反应过程中产生沉淀的质量与所加入NaOH溶液的质量关系如下图所示。试回答:

①当加入NaOH溶液50g时(即图中A点),烧杯中溶液里大量存在的金属阳离子是
②当加入NaOH溶液100g时(即图中B点),恰好完全反应。试通过计算求该氯化镁溶液中MgCl2的质量
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】氢气是高热值清洁能源,已经得到广泛研究。
I.氢气的制备
(1)实验室用锌粒与稀硫酸制取少量氢气,发生装置与收集装置如图:

①仪器a、仪器b的名称分别是__________ 、___________ 。
②锥形瓶内发生反应的化学方程式是___________ ,与装置A相比,装置B具有的优点是__________ ;可选用C装置收集氢气,可见氢气具有___________ 的性质,收集时当观察到__________ 的现象时,方可开始收集。
③氢气是一种绿色能源,点燃氢气之前需要进行验纯是因为氢气具有___________ 性。
(2)我国化学家研究出一种新型催化剂,可用水煤气(CO和水蒸气的混合气)在120℃的条件下制备氢气,该反应过程的微观示意图如下:

“解离”时,结构被破坏的分子是__________ (填化学式);请结合微观示意图,写出由水煤气制备氢气的化学方程式为___________ 。
Ⅱ.氢气的储存
(3)氢气可以直接加压储存在储氢罐中,氢气能被压缩的主要原因是_____________ 。
(4)某镁铜合金是一种储氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。
①制取镁铜合金时不能直接暴露在空气中,而是在氩气保护下进行熔炼。请以化学方程式表示原因__________ 。(任写一个)
②镁铜合金在350℃时与氢气反应生成了一种仅含镁、氢两种元素、相对分子质量为26的化合物,且其中氢元素的质量分数为7.7%,则该化合物的化学式为__________ 。
(5)氢化钙固体可用作储氢材料,其在常温下能与水反应生成氢氧化钙和氢气,因此长时间存放的氢化钙中含有的主要杂质有Ca(OH)2和___________ 。(填化学式)
I.氢气的制备
(1)实验室用锌粒与稀硫酸制取少量氢气,发生装置与收集装置如图:

①仪器a、仪器b的名称分别是
②锥形瓶内发生反应的化学方程式是
③氢气是一种绿色能源,点燃氢气之前需要进行验纯是因为氢气具有
(2)我国化学家研究出一种新型催化剂,可用水煤气(CO和水蒸气的混合气)在120℃的条件下制备氢气,该反应过程的微观示意图如下:

“解离”时,结构被破坏的分子是
Ⅱ.氢气的储存
(3)氢气可以直接加压储存在储氢罐中,氢气能被压缩的主要原因是
(4)某镁铜合金是一种储氢材料,高温时在氩气保护下,由一定质量比的Mg、Cu单质熔炼获得。
①制取镁铜合金时不能直接暴露在空气中,而是在氩气保护下进行熔炼。请以化学方程式表示原因
②镁铜合金在350℃时与氢气反应生成了一种仅含镁、氢两种元素、相对分子质量为26的化合物,且其中氢元素的质量分数为7.7%,则该化合物的化学式为
(5)氢化钙固体可用作储氢材料,其在常温下能与水反应生成氢氧化钙和氢气,因此长时间存放的氢化钙中含有的主要杂质有Ca(OH)2和
您最近一年使用:0次
综合应用题
|
适中
(0.65)
名校
解题方法
【推荐1】水与生产、生活有密切关系,我们可以从多角度认识水。
I.角度一:
(1)化合反应:郑州氢燃料公交车为绿城建设提供了助力,请写出氢气燃烧的化学方程式_____ 。
Ⅱ.角度二:
分解反应:科学家发现氢气能燃烧生成水后,又研究了水的分解实验。如图1是模拟史实探究水的组成实验。依据实验回答问题。

(2)图1为电解水的简易装置,生成的氢气在_____ (填“a”或“b”)管中。
(3)图2是电解水的微观示意图,图中保持水的化学性质的最小微粒是_____ ;由图可分析出水由氢、氧两种元素组成的理论依据是_____ 。
Ⅲ.角度三:
复分解反应:化学兴趣小组对中和反应进行了实验探究。将氢氧化钙溶液逐滴加入一定量的稀盐酸中,用数字化仪器对反应过程中溶液温度进行实时测定,得到如图3所示曲线。图4是该反应的微观示意图。
(4)请在图4虚线框内将图3b点时溶液中的微粒补画完整。
(5)取图3a点时的溶液,向其中逐滴加入碳酸钠溶液,观察到的现象是什么?
(6)若改用与该氢氧化钙溶液等质量分数的氢氧化钠溶液中和该稀盐酸,b点可能会_____ (填“左移”或“右移”)。
IV.角度四:
(7)置换反应:氨气(NH3)常温下能液化,本身也不含碳元素,其与氧气在点燃的条件下完全反应生成水和空气中含量最多的气体,这为氨作为清洁能源打下了良好的基础。若燃烧340g氨气,生成的水的质量是多少?
I.角度一:
(1)化合反应:郑州氢燃料公交车为绿城建设提供了助力,请写出氢气燃烧的化学方程式
Ⅱ.角度二:
分解反应:科学家发现氢气能燃烧生成水后,又研究了水的分解实验。如图1是模拟史实探究水的组成实验。依据实验回答问题。

(2)图1为电解水的简易装置,生成的氢气在
(3)图2是电解水的微观示意图,图中保持水的化学性质的最小微粒是
Ⅲ.角度三:
复分解反应:化学兴趣小组对中和反应进行了实验探究。将氢氧化钙溶液逐滴加入一定量的稀盐酸中,用数字化仪器对反应过程中溶液温度进行实时测定,得到如图3所示曲线。图4是该反应的微观示意图。
(4)请在图4虚线框内将图3b点时溶液中的微粒补画完整。
(5)取图3a点时的溶液,向其中逐滴加入碳酸钠溶液,观察到的现象是什么?
(6)若改用与该氢氧化钙溶液等质量分数的氢氧化钠溶液中和该稀盐酸,b点可能会
IV.角度四:
(7)置换反应:氨气(NH3)常温下能液化,本身也不含碳元素,其与氧气在点燃的条件下完全反应生成水和空气中含量最多的气体,这为氨作为清洁能源打下了良好的基础。若燃烧340g氨气,生成的水的质量是多少?
您最近一年使用:0次
综合应用题
|
适中
(0.65)
【推荐2】请回答下列问题。
(1)借助传感器对稀氢氧化钠与稀硫酸的中和反应进行研究,实验装置如图1,三颈烧瓶中盛放溶液X,匀速滴加另一溶液。_______ (填化学式),实验进行到60s时溶液中的溶质是_______ (填化学式)。
②乙同学用温度传感器测得三颈烧瓶内温度变化如图3(实验过程中热量散失忽略不计),据此可得出反应过程中_______ 能量的结论(填“吸收”“释放”之一)。
(2)某抗酸药的成分为 、
、 。某研究性学习小组利用右图装置测定抗酸药片中两种成分的质量,取1片抗酸药称量,质量为0.62g,然后加入到A装置的烧瓶中。先通一段时间氮气,再滴加稀硫酸,反应停止时装置C中质量增加0.22g,此时滴入稀硫酸的质量为80.5g。请回答:
。某研究性学习小组利用右图装置测定抗酸药片中两种成分的质量,取1片抗酸药称量,质量为0.62g,然后加入到A装置的烧瓶中。先通一段时间氮气,再滴加稀硫酸,反应停止时装置C中质量增加0.22g,此时滴入稀硫酸的质量为80.5g。请回答:_______ 。
②实验后A中烧瓶溶液里的金属阳离子是_______ (填离子符号)。
③实验后A中烧瓶里所得溶液的质量为_______ g。(只填计算结果,精确至0.1g)
④每片抗酸药中含 的质量分数为
的质量分数为_______ 。(写出计算过程,计算结果精确到0.1%)
(1)借助传感器对稀氢氧化钠与稀硫酸的中和反应进行研究,实验装置如图1,三颈烧瓶中盛放溶液X,匀速滴加另一溶液。

②乙同学用温度传感器测得三颈烧瓶内温度变化如图3(实验过程中热量散失忽略不计),据此可得出反应过程中
(2)某抗酸药的成分为
 、
、 。某研究性学习小组利用右图装置测定抗酸药片中两种成分的质量,取1片抗酸药称量,质量为0.62g,然后加入到A装置的烧瓶中。先通一段时间氮气,再滴加稀硫酸,反应停止时装置C中质量增加0.22g,此时滴入稀硫酸的质量为80.5g。请回答:
。某研究性学习小组利用右图装置测定抗酸药片中两种成分的质量,取1片抗酸药称量,质量为0.62g,然后加入到A装置的烧瓶中。先通一段时间氮气,再滴加稀硫酸,反应停止时装置C中质量增加0.22g,此时滴入稀硫酸的质量为80.5g。请回答:
②实验后A中烧瓶溶液里的金属阳离子是
③实验后A中烧瓶里所得溶液的质量为
④每片抗酸药中含
 的质量分数为
的质量分数为
您最近一年使用:0次
综合应用题
|
适中
(0.65)
解题方法
【推荐3】请回答下列问题。
(1)向硫酸中滴加氢氧化钠溶液并不断搅拌,如图为反应时溶液pH变化的示意图。

①请写出该反应的化学方程式_______ 。
②加入NaOH溶液amL时,溶液中含有哪些溶质:_________ 。
③若将bmL该氢氧化钠溶液滴入到与硫酸相同质量、相同质量分数的盐酸中,请判断反应后溶液的酸碱性。_________
(2)如图是模拟工业炼铁的微型实验装置。

①写出a处发生反应的化学方程式________ 。
②b处可以观察到的实验现象是:___________ 。
(3)碳酸氢钠受热易分解,生成碳酸钠、水和二氧化碳,反应的化学方程式为______ 。充分加热10g含碳酸钠的碳酸氢钠固体,反应前后固体中钠元素的质量分数之比为7:10,则生成水和二氧化碳的质量之和为______ g。
(4)用100t含氧化铁80%的赤铁矿石(主要成分是Fe2O3)理论上可以炼出含铁96%的生铁的质量是多少?(精确到0.1)
(1)向硫酸中滴加氢氧化钠溶液并不断搅拌,如图为反应时溶液pH变化的示意图。

①请写出该反应的化学方程式
②加入NaOH溶液amL时,溶液中含有哪些溶质:
③若将bmL该氢氧化钠溶液滴入到与硫酸相同质量、相同质量分数的盐酸中,请判断反应后溶液的酸碱性。
(2)如图是模拟工业炼铁的微型实验装置。

①写出a处发生反应的化学方程式
②b处可以观察到的实验现象是:
(3)碳酸氢钠受热易分解,生成碳酸钠、水和二氧化碳,反应的化学方程式为
(4)用100t含氧化铁80%的赤铁矿石(主要成分是Fe2O3)理论上可以炼出含铁96%的生铁的质量是多少?(精确到0.1)
您最近一年使用:0次



