央视栏目《典籍里的中国》展现了中国智慧,其中有许多古今对比。
(1)净水:明代《天工开物》一书记载了明矾净水,其净水原理是___ ;如今使用高铁酸钾(K2FeO4)净水,其净水原理为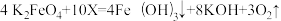 ,则X的化学式为
,则X的化学式为____ ,K2FeO4中铁元素的化合价为______ ;生活中将硬水软化的方法是______ 。
(2)冶金:我国古代就发明了湿法冶金技术。用铁和硫酸铜溶液为原料进行湿法炼铜的化学反应方程式为______ ;如今人们掌握了多种金属的冶炼技术,例如工业上常采用电解氯化镁的方式冶炼镁,同时生成氯气(Cl2),该反应条件为通电,化学方程式为______ 。
(3)出行:明朝从泰州到北京约需几个月时间,如今乘坐高铁几小时便可到达,制造高铁使用了铝合金。铝合金比纯铝的硬度______ ,铝制品耐腐蚀是因为_____ 。
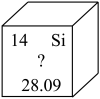
(4)记录:古代用墨书写的典籍保存至今而不变色,如今可将信息存储在芯片上,芯片中含有的某元素在元素周期表中的部分信息如图,该元素的名称是_____ ,该元素的相对原子质量为_____ 。
(1)净水:明代《天工开物》一书记载了明矾净水,其净水原理是
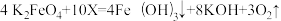 ,则X的化学式为
,则X的化学式为(2)冶金:我国古代就发明了湿法冶金技术。用铁和硫酸铜溶液为原料进行湿法炼铜的化学反应方程式为
(3)出行:明朝从泰州到北京约需几个月时间,如今乘坐高铁几小时便可到达,制造高铁使用了铝合金。铝合金比纯铝的硬度
(4)记录:古代用墨书写的典籍保存至今而不变色,如今可将信息存储在芯片上,芯片中含有的某元素在元素周期表中的部分信息如图,该元素的名称是

更新时间:2024-02-07 20:54:01
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】元素周期表是学习和研究化学的重要工具。请分析图1中的信息并回答下列问题。

(1)地壳中含量最多的金属元素是_______ (写元素符号),其质子数为_______ ,形成的阳离子的符号为_______ 。
(2)第三周期中具有相对稳定结构的原子的原子序数为_______ 。
(3)原子序数为14的元素属于_______ (填“金属”或“非金属”)元素,氮元素和磷元素的化学性质相似,是因为氮原子和磷原子的_______ 相同。
(4)若碳的相对原子质量为12,则该原子的原子核内中子数为_______ 。
(5)R+结构示意图如图2所示,R元素位于元素周期表中第_______ 周期,它的化学性质与第三周期中的_______ 元素相似。
(6)同周期的元素原子的核外电子排布的特点是_______ 。

(1)地壳中含量最多的金属元素是
(2)第三周期中具有相对稳定结构的原子的原子序数为
(3)原子序数为14的元素属于
(4)若碳的相对原子质量为12,则该原子的原子核内中子数为
(5)R+结构示意图如图2所示,R元素位于元素周期表中第
(6)同周期的元素原子的核外电子排布的特点是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】元素周期表和原子结构示意图是学习和研究化学的重要工具。根据图中所示信息,回答下列问题:

(1)图一中溴元素的相对原子质量为______ ,溴元素属于______ (填“金属元素”或“非金属元素”)。
(2)图二中A、B粒子具有相似的化学性质,原因是______ 。
(3)图三中乙所代表元素位于元素周期表的第______ 周期,图三中的S元素和图二中A粒子的元素组成的化合物的化学式为______ 。

(1)图一中溴元素的相对原子质量为
(2)图二中A、B粒子具有相似的化学性质,原因是
(3)图三中乙所代表元素位于元素周期表的第
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】“天宫二号”与在轨运行的“天宫一号”空间实验室首次交会成功,有力推动了我国空间站建设的进程,空间站中含有许多高科技元素。
(1)空间站里的氧气来自电解水,氧气由______ (填“分子”“原子”或“离子”)构成;电解水时,发生反应的化学方程式为______ 。
(2)在“空间实验室”中加工出了铥锗、铅锌、铝铜等合金。铅元素的相关信息如图所示。铅元素的原子序数为______ ,相对原子质量为______ 。

(3)太空垃圾危害大,可用盛有氢氧化锂的过滤网来除去舱内的二氧化碳,反应的化学方程式为 ,则X的化学式为
,则X的化学式为______ 。
(4)空间站上太阳能板中含有金属镓(Ga),镓的化学性质与铝相似,镓元素在化合物中一般显+3价,则可知氧化镓的化学式为______ 。
(1)空间站里的氧气来自电解水,氧气由
(2)在“空间实验室”中加工出了铥锗、铅锌、铝铜等合金。铅元素的相关信息如图所示。铅元素的原子序数为

(3)太空垃圾危害大,可用盛有氢氧化锂的过滤网来除去舱内的二氧化碳,反应的化学方程式为
 ,则X的化学式为
,则X的化学式为(4)空间站上太阳能板中含有金属镓(Ga),镓的化学性质与铝相似,镓元素在化合物中一般显+3价,则可知氧化镓的化学式为
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】利用氢气(H2)和空气中分离出的氮气(N2)可以合成氨气(NH3),下列是合成氨的工艺流程图:

第一步:分离空气
分离空气的常用方法有以下两种:
方法I.将空气液化后再气化。
(1)液态空气汽化时首先分离出氮气,则沸点:N2____ O2(选填“高于”、“等于”、“低于”)。
方法II.用分子筛分离。
(2)分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:N2_________ O2(选填“大于”或“等于”或“小于”)。
第二步:合成氨气
(3)写出氮气(N2)和氢气(H2)在高温、高压和催化剂的作用下反应生成氨气(NH3)的文字(或符号)表达式_______ ;用“〇”表示氢原子,“ ”表示氮原子,“
”表示氮原子,“ ”表示 催化剂,观察下列微观图,合成氨气的化学反应过程中微观粒子变化顺序为
”表示 催化剂,观察下列微观图,合成氨气的化学反应过程中微观粒子变化顺序为_______ (将下面三张图用序号排列)。反应前后氮元素的化合价_________ (填“升高”、“降低”或“不变”)
A B
B  C
C 
(4)氮气和氢气合成氨气,当容器中氨气的含量不再发生变化时,测得氨的含量分别与温度和压强的关系如图所示。那么按下列条件进行合成氨反应,氨的含量较高的是__________(填字母)。

(5)实际生产中氮气、氢气不可能全部转化为氨气。将降温分离出的N2、H2送回合成塔目的是______(填字母序号)

第一步:分离空气
分离空气的常用方法有以下两种:
方法I.将空气液化后再气化。
(1)液态空气汽化时首先分离出氮气,则沸点:N2
方法II.用分子筛分离。
(2)分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分子筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小:N2
第二步:合成氨气
(3)写出氮气(N2)和氢气(H2)在高温、高压和催化剂的作用下反应生成氨气(NH3)的文字(或符号)表达式
 ”表示氮原子,“
”表示氮原子,“ ”表示 催化剂,观察下列微观图,合成氨气的化学反应过程中微观粒子变化顺序为
”表示 催化剂,观察下列微观图,合成氨气的化学反应过程中微观粒子变化顺序为A
 B
B  C
C 
(4)氮气和氢气合成氨气,当容器中氨气的含量不再发生变化时,测得氨的含量分别与温度和压强的关系如图所示。那么按下列条件进行合成氨反应,氨的含量较高的是__________(填字母)。

| A.200大气压和300℃ | B.200大气压和500℃ |
| C.400大气压和300℃ | D.400大气压和500℃ |
(5)实际生产中氮气、氢气不可能全部转化为氨气。将降温分离出的N2、H2送回合成塔目的是______(填字母序号)
| A.充分利用原料 | B.防止氮气污染空气 |
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐2】阅读下列材料,回答下列问题
过氧化氢(H2O2)可用于消毒杀菌,具有不稳定性。将水蒸气冷凝在硅、玻璃、塑料、金属等材料表面,均发现了过氧化氢的存在。
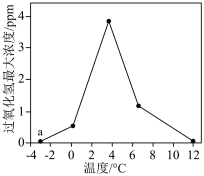
研究显示:水蒸气冷凝为粒径小于10微米的液滴时,部分水分子会转化为过氧化氢分子。水微滴中形成的过氧化氢含量随液滴尺寸的增大而减少。过氧化氢的产生量与温度、湿度等环境条件密切相关。当使用硅材料、相对湿度为55%时,得到过氧化氢的最大浓度随温度变化关系如图所示。
(1)过氧化氢中氧元素的化合价为
(2)下列说法正确的是
(3)下列说法错误的是
过氧化氢(H2O2)可用于消毒杀菌,具有不稳定性。将水蒸气冷凝在硅、玻璃、塑料、金属等材料表面,均发现了过氧化氢的存在。
研究显示:水蒸气冷凝为粒径小于10微米的液滴时,部分水分子会转化为过氧化氢分子。水微滴中形成的过氧化氢含量随液滴尺寸的增大而减少。过氧化氢的产生量与温度、湿度等环境条件密切相关。当使用硅材料、相对湿度为55%时,得到过氧化氢的最大浓度随温度变化关系如图所示。

(1)过氧化氢中氧元素的化合价为
| A.-2 | B.-1 | C.0 | D.+1 |
(2)下列说法正确的是
| A.过氧化氢属于氧化物 |
| B.过氧化氢由氢气和氧气组成 |
| C.过氧化氢中氢、氧元素的质量比为1:1 |
| D.过氧化氢的相对分子质量为34g |
(3)下列说法错误的是
| A.水蒸气在冷凝过程中可能发生化学变化 |
| B.水蒸气在玻璃表面冷凝得到的液滴一定为纯净物 |
| C.图中a点(-2.8℃)未生成过氧化氢的原因可能是形成水滴粒径大于10微米 |
| D.水蒸气冷凝为水流时,水分子间的间隔减小 |
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】纳米材料具有特殊的性质和功能。将纳米二氧化钛(TiO2)添加到墙面涂料中,可降低空气中甲醛等有害物质的浓度。根据要求回答下列问题:
(1)TiO2中钛元素的化合价是_____ 。
(2)甲醛(CH2O)中碳元素的质量分数是_____ (只需列式)。
(3)纳米二氧化钛(TiO2)可通过正钛酸(H4TiO4)在一定条件下分解得到,反应原理可表示为: ,其中X的化学式是
,其中X的化学式是_____ 。
(4)在光照条件下,甲醛以纳米二氧化钛作为催化剂,与氧气反应生成二种无毒的氧化物,起到净化空气的作用。该反应的化学方程式是_____ 。
(1)TiO2中钛元素的化合价是
(2)甲醛(CH2O)中碳元素的质量分数是
(3)纳米二氧化钛(TiO2)可通过正钛酸(H4TiO4)在一定条件下分解得到,反应原理可表示为:
 ,其中X的化学式是
,其中X的化学式是(4)在光照条件下,甲醛以纳米二氧化钛作为催化剂,与氧气反应生成二种无毒的氧化物,起到净化空气的作用。该反应的化学方程式是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】在日常生活中,餐具中的勺子、叉子等经常用到。请回答下列问题并填写相关空白。

(1)餐具中的勺子、叉子等都是用不锈钢材料制成的。这主要是利用不锈钢材料的______性能(填字母)。
(2)不锈钢材料中含铁、铬(Cr)、镍(Ni)等。金属铬(Cr)的冶炼是用铝作还原剂和三氧化二铬反应生产金属铬,称为铝热法。反应在高温下进行。请写出该反应的化学方程式______ ,该反应前后铬元素的化合价分别为______ 。
(3)铝和三氧化二铬在电加热至高温反应生成金属铬的过程中的能量转化为______ ;(用“→”表示转化)
(4)上述方法和用焦炭作还原剂生成金属铬相比可以减少一些污染物的排放,如一氧化碳和炭粒等。其中一氧化碳是目前计入空气质量评价的主要污染物,气体污染物中除一氧化碳外,还有______ 。(至少填两种)

(1)餐具中的勺子、叉子等都是用不锈钢材料制成的。这主要是利用不锈钢材料的______性能(填字母)。
| A.导电性好 | B.抗腐蚀性好 | C.硬度大 |
(3)铝和三氧化二铬在电加热至高温反应生成金属铬的过程中的能量转化为
(4)上述方法和用焦炭作还原剂生成金属铬相比可以减少一些污染物的排放,如一氧化碳和炭粒等。其中一氧化碳是目前计入空气质量评价的主要污染物,气体污染物中除一氧化碳外,还有
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
【推荐2】玉兔号月球车成功到达月球表面,让我们实现了“上九天揽月”的愿望,是我们中国人的骄傲。请回答下列问题:

(1)月球车上有两片可以展开的太阳能电池板,白天时充电,晚上月球车行走时的能量转化是____ (用“→”表示转化)
(2)月球车的制备材料中选用了铝合金,比纯铝有很多优良性能,如_____ (填字母)。
A 硬度小 B 强度高 C 熔点高
(3)月球车上的太阳能电池板主要材料为硅。工业上利用氢气和四氯化硅在高温条件下反应制取它,同时生成了一种刺激性气味的气体,该反应的化学方程式为_______ , 反应前后硅元素的化合价变化为_____ 。

(1)月球车上有两片可以展开的太阳能电池板,白天时充电,晚上月球车行走时的能量转化是
(2)月球车的制备材料中选用了铝合金,比纯铝有很多优良性能,如
A 硬度小 B 强度高 C 熔点高
(3)月球车上的太阳能电池板主要材料为硅。工业上利用氢气和四氯化硅在高温条件下反应制取它,同时生成了一种刺激性气味的气体,该反应的化学方程式为
您最近一年使用:0次
【推荐3】化学与生活息息相关。
(1)如图是某电子产品拆解图片。图中标示的材料属于有机合成材料的是___________ ;选择钛合金作为螺丝材料,是因为合金的硬度比组成金属的硬度___________ (填“大”或“小”)。

(2)制造电子芯片的主要材料是硅。工业上制取硅的主要化学反应为SiO2+2C Si+2CO↑,该化学反应的反应物中被还原的是
Si+2CO↑,该化学反应的反应物中被还原的是___________ ,该反应的基本类型属于___________ 反应。
(3)生活中某些废旧电池含有汞,如果随意丢弃,会造成污染。常用的干电池内部填有氯化铵和二氧化锰等物质,若通过分离得到氯化铵,在实验室需进行的操作是溶解、过滤和___________ ,得到的氯化铵在农业上又可用作___________ 。
(1)如图是某电子产品拆解图片。图中标示的材料属于有机合成材料的是

(2)制造电子芯片的主要材料是硅。工业上制取硅的主要化学反应为SiO2+2C
 Si+2CO↑,该化学反应的反应物中被还原的是
Si+2CO↑,该化学反应的反应物中被还原的是(3)生活中某些废旧电池含有汞,如果随意丢弃,会造成污染。常用的干电池内部填有氯化铵和二氧化锰等物质,若通过分离得到氯化铵,在实验室需进行的操作是溶解、过滤和
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐1】从废旧电脑的某些零部件中回收金属银,设计流程如图所示:
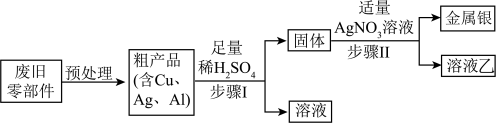
(1)从垃圾分类的角度,该厂加工的废旧电子产品属于______。
(2)步骤Ⅰ和步骤Ⅱ都涉及的实验操作是______ 。
(3)步骤Ⅰ中加入足量稀硫酸后发生反应的化学方程式为______ 。
(4)溶液乙中只含有一种溶质,该溶质的化学式为______ 。
(5)据此判断,铜、银、铝的金属活动性由强到弱的顺序是______ (填元素符号)。

(1)从垃圾分类的角度,该厂加工的废旧电子产品属于______。
| A.有害垃圾 | B.可回收垃圾 | C.厨余垃圾 | D.其他垃圾 |
(3)步骤Ⅰ中加入足量稀硫酸后发生反应的化学方程式为
(4)溶液乙中只含有一种溶质,该溶质的化学式为
(5)据此判断,铜、银、铝的金属活动性由强到弱的顺序是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
解题方法
【推荐2】人类文明进步与金属材料发展关系十分密切。
(1)下列金属制品的主要用途,利用金属异电性的是________________ 。

(2)2018年10月24日,港珠澳大桥正式通车运营。港珠澳大桥是世界最长的跨海钢桥,施工中用了大量的钢材并采用了先进的防锈技术,钢铁制品在空气中容易与_________________ 等物质接触而生锈,请写出一种生活中防止钢铁制品生锈的方法________________ 。
(3)铝制品在空气中具有优良的抗腐蚀性能,原因是_________________ (用化学方程式表示)。
(4)将一定量的金属R加入硝酸锌和硝酸银的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列说法正确的是___________ 。
A若滤液有颜色,则R一定是Cu
B若滤渣中加入稀盐酸产生气泡,则滤渣中一定有Zn
C若滤渣中只有2种金属,则滤液中一定有2种溶质
D若向滤液中加入稀盐酸,无明显现象,则滤渣中一定有Ag,可能有R
(1)下列金属制品的主要用途,利用金属异电性的是

(2)2018年10月24日,港珠澳大桥正式通车运营。港珠澳大桥是世界最长的跨海钢桥,施工中用了大量的钢材并采用了先进的防锈技术,钢铁制品在空气中容易与
(3)铝制品在空气中具有优良的抗腐蚀性能,原因是
(4)将一定量的金属R加入硝酸锌和硝酸银的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列说法正确的是
A若滤液有颜色,则R一定是Cu
B若滤渣中加入稀盐酸产生气泡,则滤渣中一定有Zn
C若滤渣中只有2种金属,则滤液中一定有2种溶质
D若向滤液中加入稀盐酸,无明显现象,则滤渣中一定有Ag,可能有R
您最近一年使用:0次




