某学习小组利用锈蚀严重的废铜屑(铜锈的主要成分是碱式碳酸铜【Cu2(OH)2CO3】)为原料回收铜,
分别采用图1的两种方案。请回答下列问题。
资料1: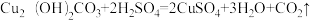
资料2:回收铜的两种实验方案。
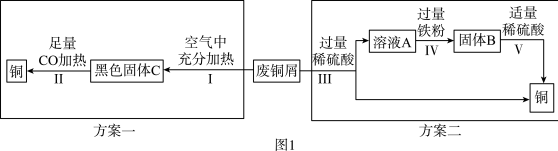
(1)方案一中步骤Ⅱ是利用了CO的___________ 性(填“氧化”或“还原”),生成的二氧化碳不能直接排放到空气中,需要将其回收后再与碳粉作用,又可以生成CO,写出该过程的化学反应方程式:___________ 。
(2)方案二中步骤Ⅲ、Ⅳ、V都涉及到的操作名称是___________ ,该操作所需的玻璃仪器有:玻璃棒、烧杯和___________ 。
(3)方案二中步骤Ⅳ加入过量铁粉的目的是___________ 。
分别采用图1的两种方案。请回答下列问题。
资料1:
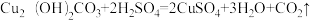
资料2:回收铜的两种实验方案。

(1)方案一中步骤Ⅱ是利用了CO的
(2)方案二中步骤Ⅲ、Ⅳ、V都涉及到的操作名称是
(3)方案二中步骤Ⅳ加入过量铁粉的目的是
更新时间:2024/02/13 08:07:25
|
相似题推荐
填空与简答-推断题
|
适中
(0.65)
解题方法
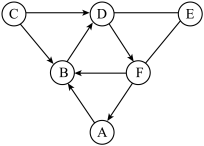
【推荐1】已知A、B、C、D、E是初中化学中常见的五种物质。其中A、D是黑色固体,D具有磁性,B、C、E是无色气体,B的相对分子质量小于C,它们在一定条件下的转化关系如图所示(其他反应物和生成物已略去)。请回答下列问题:
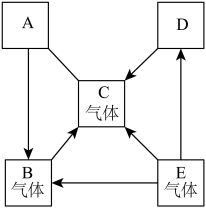
(1)C是________ (填化学式);
(2)写出E转化成D的化学方程式________ ;
(3)写出B在高温条件下还原D的化学方程式________ ;
(4)评述B物质的“利”________ 与“弊” ________ (各举一例)。

(1)C是
(2)写出E转化成D的化学方程式
(3)写出B在高温条件下还原D的化学方程式
(4)评述B物质的“利”
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】积极应对气候变化,展现大国担当,中国向世界宣布2030年前实现碳达峰、2060年前实现碳中和的国家目标。
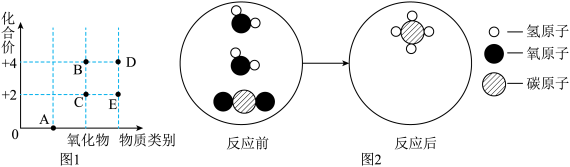
①二氧化碳中碳元素的化合价对应的是图中的______ (填字母)。写出A和B在高温条件下转化成C的化学方程式______ 。
②造成CO2排放过多的主要原因是煤、石油和______ (填名称)等化石燃料的过度使用。
(2)CO2的吸收:自然界有多种途径吸收CO2
①绿色植物通过______ 吸收CO2。
②风化的岩石如CaCO3粉末可吸收空气中的CO2和水转化为Ca(HCO3)2,反应的化学方程式为______ 。
(3)CO2的利用:将CO2作为资源是实现碳中和的有效乃法。我国某科研小组正在研究将二氧化碳与水在一定条件下转化为甲烷,其化学反应的微观示意图如图2。
①反应后除甲烷外,还有一种气体单质,请按上图补全反应后的粒子模型______ 。
②固态CO2俗称干冰,常用于______ 。
①二氧化碳中碳元素的化合价对应的是图中的
②造成CO2排放过多的主要原因是煤、石油和
(2)CO2的吸收:自然界有多种途径吸收CO2
①绿色植物通过
②风化的岩石如CaCO3粉末可吸收空气中的CO2和水转化为Ca(HCO3)2,反应的化学方程式为
(3)CO2的利用:将CO2作为资源是实现碳中和的有效乃法。我国某科研小组正在研究将二氧化碳与水在一定条件下转化为甲烷,其化学反应的微观示意图如图2。
①反应后除甲烷外,还有一种气体单质,请按上图补全反应后的粒子模型
②固态CO2俗称干冰,常用于
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
真题
解题方法
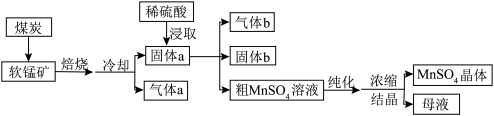
【推荐3】硫酸锰广泛用于医药、电子工业等领域.以软锰矿(主要成分是MnO2,含少量Fe2O3、SiO2等杂质)为原料生产硫酸锰的工艺流程如图所示。回答问题: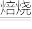 2MnO+CO2↑、2Fe2O3+3C
2MnO+CO2↑、2Fe2O3+3C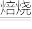 4Fe+3CO2↑。
4Fe+3CO2↑。
资料2:SiO2不溶于水,也不溶于稀硫酸。
(1)焙烧前将软锰矿和煤炭粉碎的目的是______ 。
(2)加入过量的煤炭可保证软锰矿中的MnO2充分转化为MnO,生成的气体a中除了CO2外,还可能含有______ 。
(3)用稀硫酸浸取MnO时发生反应的化学方程式是______ 。
(4)固体a中的某物质可与稀硫酸反应生成气体b,该物质是______ 。
(5)为了提高原料的利用率,浓缩结晶后剩下的母液应该_______ (填“回收利用”或“直接排放”)。
 2MnO+CO2↑、2Fe2O3+3C
2MnO+CO2↑、2Fe2O3+3C 4Fe+3CO2↑。
4Fe+3CO2↑。资料2:SiO2不溶于水,也不溶于稀硫酸。
(1)焙烧前将软锰矿和煤炭粉碎的目的是
(2)加入过量的煤炭可保证软锰矿中的MnO2充分转化为MnO,生成的气体a中除了CO2外,还可能含有
(3)用稀硫酸浸取MnO时发生反应的化学方程式是
(4)固体a中的某物质可与稀硫酸反应生成气体b,该物质是
(5)为了提高原料的利用率,浓缩结晶后剩下的母液应该
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
名校
解题方法
【推荐1】“复兴号”化学动车给五节车厢A~E分别代表初中化学教材中五种常见物质,如图所示“→”表示相邻车厢的物质间转化关系(所涉及反应均为初中常见的化学反应)。其中A、B所属的物质类别和组成元素都相同,C是用于医疗急救的气体,E是紫红色金属。
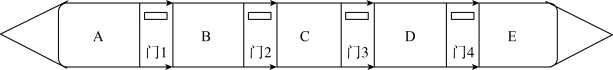
(1)请写出下列物质的化学式:A_________ ,D_________ ;
(2)A→B反应的化学方程式为_________ ,属于_________ 反应(填基本反应类型)。
(3)只有能与着两边的“车厢”都反应的“旅客”才可从此门上车,则“旅客”氢气可以从_________ 顺利上车(填序号)。
①门1 ②门2 ③门3 ④门4

(1)请写出下列物质的化学式:A
(2)A→B反应的化学方程式为
(3)只有能与着两边的“车厢”都反应的“旅客”才可从此门上车,则“旅客”氢气可以从
①门1 ②门2 ③门3 ④门4
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某样品是由铁粉和氧化铜粉末均匀混合而成,将该样品等质量分为两份,进行以下实验回收铜,若每一步都充分反应,得到的固体2是两种金属的混合物。
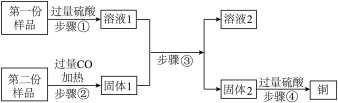
(1)步骤①中观察到的实验现象为_______ 。溶液1和溶液2中都含有的溶质是_______ (填物质的名称)。
(2)步骤②在下图所示的装置(夹持仪器已省略)中进行
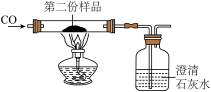
点燃酒精灯前,先要通一段时间CO,目的是_______ 。请写出硬质玻璃管中发生反应的化学方程式_______ 。用该装置做实验的不足之处是_______ 。
(3)根据上述实验流程,能得出样品中铁和氧化铜的物质的量大小有怎样的关系?____ 请说明理由。_______ 。

(1)步骤①中观察到的实验现象为
(2)步骤②在下图所示的装置(夹持仪器已省略)中进行

点燃酒精灯前,先要通一段时间CO,目的是
(3)根据上述实验流程,能得出样品中铁和氧化铜的物质的量大小有怎样的关系?
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2021年5月22日10时40分,中国制造的火星车“祝融号”安全驶离着陆平台,到达火星表面,开始巡视探测。火星车采用了铝蜂窝夹层、铝基碳化硅等多种新材料。请根据题意回答下列问题:
(1)铝能制作成铝箔,是利用了铝的___________ 性;
(2)铝合金中主要含有铝、铜、镁三种金属。为验证这三种金属的活动顺序,某同学设计了如下图的3个实验。实验甲中发生反应的化学方程式:___________ ,另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是___________ (填字母序号);
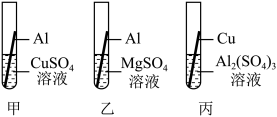
A 乙、丙都可以省去
B 乙、丙都不能省去
C 乙可以省去,丙不能省
D 丙可以省去,乙不能省
(3)取一定量的Mg放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到固体和滤液。下列说法错误的是__________ (填字母序号)。
A 固体中只有Ag时,滤液一定呈蓝色
B 固体中有Cu时,滤液一定呈无色
C 当固体只有Ag时,滤液中一定没有AgNO3
D 当固体中有Cu时,滤液中一定有Mg(NO3)2
(1)铝能制作成铝箔,是利用了铝的
(2)铝合金中主要含有铝、铜、镁三种金属。为验证这三种金属的活动顺序,某同学设计了如下图的3个实验。实验甲中发生反应的化学方程式:

A 乙、丙都可以省去
B 乙、丙都不能省去
C 乙可以省去,丙不能省
D 丙可以省去,乙不能省
(3)取一定量的Mg放入Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,得到固体和滤液。下列说法错误的是
A 固体中只有Ag时,滤液一定呈蓝色
B 固体中有Cu时,滤液一定呈无色
C 当固体只有Ag时,滤液中一定没有AgNO3
D 当固体中有Cu时,滤液中一定有Mg(NO3)2
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】向硝酸镁、硝酸铜和硝酸银的混合溶液中,加入一定质量的铁粉和锌粒,充分反应后过滤,得到滤渣和滤液。回答下列问题:
(1)写出一定发生反应的化学方程式:_____ ;
(2)滤渣中可能含有的物质的化学式是_____ ;
(3)滤液中一定含有的离子符号是_____ 。
(1)写出一定发生反应的化学方程式:
(2)滤渣中可能含有的物质的化学式是
(3)滤液中一定含有的离子符号是
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐1】物质间的转化关系图所示(注:图中各路线均为一步完成的化学反应)。
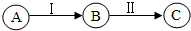
回答下列问题:
(1)A B C三种物质同属于氧化物,B是二氧化碳。若变化Ⅰ属于化合反应,变化Ⅱ的化学方程式为:______ 。
(2)A B C三种物质同属于单质,B是氢气写出变化Ⅱ的化学方程式:______ ,其基本反应类型属于______ 。
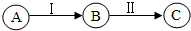
回答下列问题:
(1)A B C三种物质同属于氧化物,B是二氧化碳。若变化Ⅰ属于化合反应,变化Ⅱ的化学方程式为:
(2)A B C三种物质同属于单质,B是氢气写出变化Ⅱ的化学方程式:
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】某科学兴趣小组,用废渣(主要为CaCO3,还含有C、Fe2O3、MgO三种少量杂质)去制作CaCl2,反应过程如图所示。

(1)Ⅰ过程中加过量稀盐酸的目的是______ 。
(2)Ⅰ过程中MgO发生反应的化学反应方程式______ ,此反应为______ 反应(填基本反应类型)。
(3)滤渣一的成分为______ (填化学式)。
(4)X溶液为______ (填化学式)。
(5)NaCl在生活中的用途:______ (写一例)。

(1)Ⅰ过程中加过量稀盐酸的目的是
(2)Ⅰ过程中MgO发生反应的化学反应方程式
(3)滤渣一的成分为
(4)X溶液为
(5)NaCl在生活中的用途:
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】小琴同学设计了图所示的A、B两个实验.

(1)实验时,她为了除去铁丝和银丝表面的氧化物或污物,其操作是________________ .
(2)A实验的目的是________________________ ;实验时,将铁丝和银丝同时插入稀硫酸中,可观察到的现象是________________________________________________________ ;所发生反应的化学方程式为________________________________________ .
(3)B实验中,当烧杯内盛有________ 溶液时,可验证Fe、________________ 、Ag三种金属的活动性强弱.

(1)实验时,她为了除去铁丝和银丝表面的氧化物或污物,其操作是
(2)A实验的目的是
(3)B实验中,当烧杯内盛有
您最近一年使用:0次