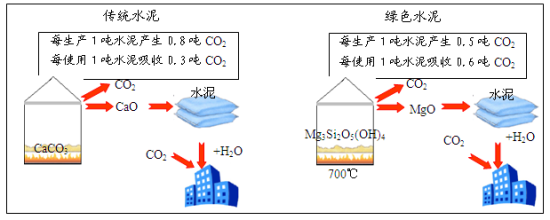
为了节能减排,科学家发明了一种以某种镁硅酸盐矿石[主要成分Mg3Si2O5(OH)4]为原料的新型绿色水泥。全球镁硅酸盐储量丰富,新型绿色水泥不必担心原材料,推广潜力很大。新型绿色水泥与传统水泥对比如图。
(1)传统水泥和绿色水泥的生产过程分别涉及以下反应:
CaCO3 CaO+ CO2↑ Mg3Si2O5(OH)4
CaO+ CO2↑ Mg3Si2O5(OH)4 3MgO + 2SiO2 + 2H2O↑
3MgO + 2SiO2 + 2H2O↑
以上两个反应都属于___ (填写基本反应类型)。
(2)与传统水泥相比,每生产和使用1吨绿色水泥能够减少排放___ 吨二氧化碳。
(3)传统水泥生产中,高温煅烧某种石灰石50吨,可产生二氧化碳多少吨?已知该石灰石中碳酸钙含量为80%,杂质不反应。

(1)传统水泥和绿色水泥的生产过程分别涉及以下反应:
CaCO3
 CaO+ CO2↑ Mg3Si2O5(OH)4
CaO+ CO2↑ Mg3Si2O5(OH)4 3MgO + 2SiO2 + 2H2O↑
3MgO + 2SiO2 + 2H2O↑以上两个反应都属于
(2)与传统水泥相比,每生产和使用1吨绿色水泥能够减少排放
(3)传统水泥生产中,高温煅烧某种石灰石50吨,可产生二氧化碳多少吨?已知该石灰石中碳酸钙含量为80%,杂质不反应。
2014·浙江台州·中考真题 查看更多[2]
更新时间:2016-11-28 12:16:55
|
相似题推荐
【推荐1】《功勋》讲述了共和国勋章获得者的精彩故事——黄旭华的潜艇梦。

(1)黄旭华被誉为中国核潜艇之父。“氧烛”常用作潜艇紧急供氧设备(如图)。使用时,产氧药块中的氯酸钠(NaClO3)受热并在二氧化锰的催化下生成氯化钠并放出氧气。该反应的符号表达式为:_______ ,属于_______ (填基本反应类型)反应。
(2)某型号“氧烛"中约含氯酸钠(NaClO3)10.65 kg,宪全反应后氯酸钠中氧元素全部转化为氧气,理论上可生成_______ kg 氧气。

(1)黄旭华被誉为中国核潜艇之父。“氧烛”常用作潜艇紧急供氧设备(如图)。使用时,产氧药块中的氯酸钠(NaClO3)受热并在二氧化锰的催化下生成氯化钠并放出氧气。该反应的符号表达式为:
(2)某型号“氧烛"中约含氯酸钠(NaClO3)10.65 kg,宪全反应后氯酸钠中氧元素全部转化为氧气,理论上可生成
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将一定质量的高锰酸钾固体充分加热,冷却后称量剩余固体质量比反应前减少了3.2g,请完成下列分析及计算:
(1)该反应属于_____________ 反应(填基本反应类型)。
(2)高锰酸钾的质量是多少?(写出计算过程)
(1)该反应属于
(2)高锰酸钾的质量是多少?(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】《礼记》等文献中记载古人用草木灰(主要成分是 )与石灰石灼烧后的固体、水混合制取碱,用作纺织品漂洗剂。小组同学以“古法制碱”为主题开展了项目式学习。
)与石灰石灼烧后的固体、水混合制取碱,用作纺织品漂洗剂。小组同学以“古法制碱”为主题开展了项目式学习。
项目一:实验室模拟古法制碱
【实验设计】制碱的主要流程如图所示。___________ (填“化合反应”或“分解反应”)。
②请写出步骤二反应的化学方程式:___________ 。
③资料显示,步骤三反应的化学方程式:
项目二:如何测定草木灰中碳酸钾的含量?
1 常见草木灰钾含量(以碳酸钾表示)如下表:
2 提取碳酸钾主要过程是:秸秆→草木灰→滤液→固体
(2)表格中钾含量最高的草木灰是___________ ,同学们选用这种秸秆灰提取碳酸钾。
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。___________ 。
(4)根据图2,搅拌器转速控制在每分钟___________ 转,浸取时间为___________ 分钟,比较适宜。
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。
(5)实验中需缓慢滴入稀硫酸,原因是___________ 。
(6)装置B的作用是___________ 。
【数据与解释】
(7)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为___________ %(保留小数点后两位),与表格中数据相比明显偏低,原因可能是___________ (填序号)。
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
 )与石灰石灼烧后的固体、水混合制取碱,用作纺织品漂洗剂。小组同学以“古法制碱”为主题开展了项目式学习。
)与石灰石灼烧后的固体、水混合制取碱,用作纺织品漂洗剂。小组同学以“古法制碱”为主题开展了项目式学习。项目一:实验室模拟古法制碱
【实验设计】制碱的主要流程如图所示。

②请写出步骤二反应的化学方程式:
③资料显示,步骤三反应的化学方程式:

项目二:如何测定草木灰中碳酸钾的含量?
1 常见草木灰钾含量(以碳酸钾表示)如下表:
| 草木灰种类 | 小灌木灰 | 稻草灰 | 小麦秆灰 | 棉壳灰 | 棉秆灰 | 向日葵杆灰 |
| K2CO3(%) | 8.66 | 2.63 | 20.26 | 32.28 | 16.44 | 51.97 |
(2)表格中钾含量最高的草木灰是
【设计与实验】
实验一:提取碳酸钾
第一步:燃烧秸秆,收集草木灰,称取20.00g。
第二步:用60℃水浸洗草木灰(如图1)并过滤,浸洗滤渣2次,合并滤液。
第三步:蒸发滤液,烘干得到9.90g固体。


(4)根据图2,搅拌器转速控制在每分钟
实验二:测定碳酸钾含量
取实验一中所得固体3.30g进行图3实验。
(5)实验中需缓慢滴入稀硫酸,原因是
(6)装置B的作用是
【数据与解释】
(7)称量图3中反应前后烧杯和其中溶液的总质量,增重0.92g。计算草木灰中碳酸钾的质量分数为
a.烧杯中溶液与空气接触 b.固体含有其它钾盐 c.固体含有氯化钠
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】小明同学在实验室发现一瓶纯碱,标签上写有含少量氯化钠,为了弄清该瓶纯碱的含量。他取该纯碱样品14g放入烧杯中,然后把100g稀盐酸平均分5次加入其中,测得相关数据如下表。
试求:
(1)生成二氧化碳的质量为________ g。
(2)该纯碱样品中碳酸钠的质量?
(3)两物质恰好完全反应时所得溶液的溶质质量分数。
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | |
| 加入稀盐酸的质量/g | 20 | 20 | 20 | 20 | 20 |
| 烧杯中物质的质量/g | 32.9 | 51.8 | 70.7 | 89.6 | 109.6 |
(1)生成二氧化碳的质量为
(2)该纯碱样品中碳酸钠的质量?
(3)两物质恰好完全反应时所得溶液的溶质质量分数。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】我国约在南北朝时就开始冶炼黄铜。黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中锌的质量分数(不考虑黄铜中的其他杂质),现将30g稀硫酸分三次加入到5g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
试求:
(1)m=_____ 。
(2)此黄铜样品中锌的质量分数是多少?
| 第一次 | 第二次 | 第三次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 |
| 生成氢气的质量(g) | 0.04 | m | 0.02 |
(1)m=
(2)此黄铜样品中锌的质量分数是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】实验室测定一瓶变质的熟石灰中氢氧化钙的含量,取样品10g于锥形瓶中,向锥形瓶中滴加稀盐酸,充分反应后,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示。请计算样品中氢氧化钙的质量分数。


您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】向10g大理石样品中分两次加入一定溶质质量分数的稀盐酸(杂质不溶于水,也不与稀盐酸反应),充分反应后烧杯内物质总质量的变化如图所示。

请计算:
(1)生成二氧化碳的质量为_____ g;
(2)求10g大理石样品中CaCO3的实际质量(写出计算过程);
(3)图2中,x=_____ g。

请计算:
(1)生成二氧化碳的质量为
(2)求10g大理石样品中CaCO3的实际质量(写出计算过程);
(3)图2中,x=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】好奇的同学们为了探测贝壳中碳酸钙的含量,从海边收集了贝壳清洗干燥后带到学校实验室。
同学们进行了下图的实验(贝壳中的杂质不溶于水,也不与其他物质反应:生成气体全部逸出,有关反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑)。

请计算:
(1)生成二氧化碳的质量为_______ g。
(2)10.4g贝壳中碳酸钙的质量是多少?
同学们进行了下图的实验(贝壳中的杂质不溶于水,也不与其他物质反应:生成气体全部逸出,有关反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑)。

请计算:
(1)生成二氧化碳的质量为
(2)10.4g贝壳中碳酸钙的质量是多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用2g石灰石样品,把20g稀盐酸(氯化氢的水溶液)分4次加入样品中(样品中除碳酸钙外,其它成分既不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,得实验数据如下:
(1)上表中M的数值应为________
(2) 从以上数据可知,这四次试验中第_________ 次试验后石灰石样品中的碳酸钙已完全反应
(3)此石灰石样品与稀盐酸充分反应能生成气体多少克________
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5 g |
| 第二次加入5g | M |
| 第三次加入5g | 0.5 g |
| 第四次加入5g | 0.3 g |
(2) 从以上数据可知,这四次试验中第
(3)此石灰石样品与稀盐酸充分反应能生成气体多少克
您最近一年使用:0次



