航母舰体需要定期除锈维护,为实现对除锈废液(溶质主要成分为HCl、 ,其他杂质忽略)的综合利用,需测定废液中HCl的质量分数。取200g废液样品,依次加入100g溶质质量分数相同的NaOH溶液,过滤,称重,相关数据如图。
,其他杂质忽略)的综合利用,需测定废液中HCl的质量分数。取200g废液样品,依次加入100g溶质质量分数相同的NaOH溶液,过滤,称重,相关数据如图。
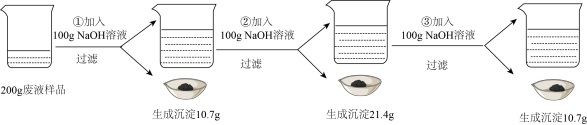
回答下列问题。
(1)第③次过滤后,滤液中溶质的成分为_______ (用化学式表示)。
(2)所用100gNaOH溶液中溶质的质量。
(3)废液样品中HCl的质量分数。(结果精确至0.1%)
 ,其他杂质忽略)的综合利用,需测定废液中HCl的质量分数。取200g废液样品,依次加入100g溶质质量分数相同的NaOH溶液,过滤,称重,相关数据如图。
,其他杂质忽略)的综合利用,需测定废液中HCl的质量分数。取200g废液样品,依次加入100g溶质质量分数相同的NaOH溶液,过滤,称重,相关数据如图。
回答下列问题。
(1)第③次过滤后,滤液中溶质的成分为
(2)所用100gNaOH溶液中溶质的质量。
(3)废液样品中HCl的质量分数。(结果精确至0.1%)
更新时间:2024-03-13 08:02:59
|
相似题推荐
计算题
|
困难
(0.15)
名校
【推荐1】为测定石灰石样品中碳酸钙的含量,小明取25g石灰石样品与一定质量的14.6%的稀盐酸恰好完全反应,将反应所得混合物蒸干得到固体27.2 g(不含结晶水,假设样品中的杂质既不与稀盐酸反应)。试计算:
(1)参加反应的盐酸的质量______。
(2)石灰石样品中碳酸钙的含量______。
(1)参加反应的盐酸的质量______。
(2)石灰石样品中碳酸钙的含量______。
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
【推荐2】取15g碳酸钠(Na2CO3)样品(假设其中杂质不参与反应,也不溶于水)加入到盛有足量的稀盐酸的烧杯中,充分反应后,得到4.4g二氧化碳气体。请回答下列问题:
(1)写出发生反应的化学方程式________ 。
(2)写出求解生成水质量(X)的比例式________ 。
(3)生成的氯化钠质量为________ 。
(4)原碳酸钠样品中碳酸钠纯度为________ 。
(1)写出发生反应的化学方程式
(2)写出求解生成水质量(X)的比例式
(3)生成的氯化钠质量为
(4)原碳酸钠样品中碳酸钠纯度为
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐1】某粗盐样品中含有氯化钠、氯化镁和不溶性杂质,希溪同学取该样品进行如下实验:

(1) 加入氢氧化钠溶液时发生反应的化学方程式_______________;
(2)根据产生沉淀质量求解参加反应的氢氧化钠质量(X)的比例式为_______________;
(3) 原粗盐固体中氯化镁的质量是________________;
(4)粗盐样品中氯化钠的含量是_______________(保留一位小数);
(5) 为了使最后得到10%的氯化钠溶液,加入氢氧化钠溶液的质量是______________。

(1) 加入氢氧化钠溶液时发生反应的化学方程式_______________;
(2)根据产生沉淀质量求解参加反应的氢氧化钠质量(X)的比例式为_______________;
(3) 原粗盐固体中氯化镁的质量是________________;
(4)粗盐样品中氯化钠的含量是_______________(保留一位小数);
(5) 为了使最后得到10%的氯化钠溶液,加入氢氧化钠溶液的质量是______________。
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
解题方法
【推荐2】氧化亚铜(Cu 2O)可用于船底防污漆,防止海生物对船舶设备的污损,现将Cu2O和Cu的固体混合物6.8g放入烧杯中,加入过量的质量分数为20%的稀硫酸30g,充分反应后,过滤、洗涤、干燥,得到4.8g固体。
已知:Cu2O+H2SO4=CuSO4+Cu+H2O
计算:(1)所加稀硫酸中溶质的质量为 g。
(2)原混合物中的Cu2O和Cu质量比(写出过程,结果用最简整数比表示)。
已知:Cu2O+H2SO4=CuSO4+Cu+H2O
计算:(1)所加稀硫酸中溶质的质量为 g。
(2)原混合物中的Cu2O和Cu质量比(写出过程,结果用最简整数比表示)。
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
解题方法
【推荐3】为分析某由氧化铜和铜组成的混合物中氧化铜的质量分数,现取3份该混合物各20g,分别缓慢加入到50g、100g、150g某稀硫酸中,测得三组实验数据如下表:
根据实验及有关数据进行分析与计算:
(1)20g样品中含氧化铜的质量为_______ g,样品中铜元素的质量分数为_______ 。
(2)计算所用的稀硫酸溶质的质量分数是______ ?(写出计算过程)
(3)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%的NaOH溶液 的质量与生成沉淀质量变化关系的曲线图______ 。

| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |
| 稀硫酸的质量/g | 50 | 100 | 150 |
| 溶解固体的质量/g | 10.0 | 16.0 | 16.0 |
(1)20g样品中含氧化铜的质量为
(2)计算所用的稀硫酸溶质的质量分数是
(3)将第Ⅱ组混合物过滤,在滤液中滴加10%的NaOH溶液,画出在该混合溶液中加入10%的NaOH溶液 的质量与生成沉淀质量变化关系的曲线图

您最近一年使用:0次
计算题
|
困难
(0.15)
真题
解题方法
【推荐1】向含10g NaOH的溶液中通入一定量的CO2,然后在低压条件下蒸干得12.6g白色固体,通过计算确定该白色固体的成分及其各组成成分的质量(写出计算过程)_____________ 。
[查阅资料]1、Na2CO3+CO2+H2O═2NaHCO3
2、NaHCO3溶液在低压蒸干条件下得到的固体不分解.
[查阅资料]1、Na2CO3+CO2+H2O═2NaHCO3
2、NaHCO3溶液在低压蒸干条件下得到的固体不分解.
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
解题方法
【推荐2】将20.0g NaOH、Ca(OH)2、NaCl组成的固体混合物溶于水配成溶液,向混合液中缓慢通入CO2气体(气体的溶解忽略不计),生成沉淀的质量与通入CO2气体的质量关系如图所示,请根据题意回答问题:
已知:Na2CO3+CO2+H2O═2NaHCO3
NaHCO3+NaOH═Na2CO3+H2O
(1)经分析,A点溶液中所含溶质为 (填化学式)。
(2)在B点时,溶液里碳元素均存在于NaHCO3中,若B点后继续通入足量的CO2气体,请将图象补充完整。
(3)该混合物中NaCl的质量分数为多少?(写出计算过程,计算结果精确至0.1%)

已知:Na2CO3+CO2+H2O═2NaHCO3
NaHCO3+NaOH═Na2CO3+H2O
(1)经分析,A点溶液中所含溶质为 (填化学式)。
(2)在B点时,溶液里碳元素均存在于NaHCO3中,若B点后继续通入足量的CO2气体,请将图象补充完整。
(3)该混合物中NaCl的质量分数为多少?(写出计算过程,计算结果精确至0.1%)

您最近一年使用:0次
计算题
|
困难
(0.15)
真题
【推荐3】实验室有一瓶硫酸铵(含杂质氯化镁)样品。化学兴趣小组的同学为了测定该样品中氯化镁的含量,取该样品17.95g全部溶于152.35g水中,向所得溶液中滴加溶质质量分数为10%的氢氧化钠溶液,实验数据如表所示:
求:
(1)表中m的值为___________。
(2)该样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%)。
(3)当恰好完全反应时所得溶液中硫酸钠的质量分数(写出计算过程)。
| 时间/s | 30 | 60 | 90 | 120 | 150 |
| 产生沉淀的质量/g | 0.725 | m | 2.175 | 2.9 | 2.9 |
求:
(1)表中m的值为___________。
(2)该样品中氯化镁的质量分数(写出计算过程,结果精确到0.1%)。
(3)当恰好完全反应时所得溶液中硫酸钠的质量分数(写出计算过程)。
您最近一年使用:0次
计算题
|
困难
(0.15)
解题方法
【推荐1】向碳酸钠和氯化钠的混合物15.6 g中加入100 g稀盐酸,恰好完全反应后,得到111.2 g溶液。试计算:
(1)产生二氧化碳多少克?
(2)所得溶液中溶质的质量分数是多少?
(1)产生二氧化碳多少克?
(2)所得溶液中溶质的质量分数是多少?
您最近一年使用:0次
计算题
|
困难
(0.15)
名校
解题方法
【推荐2】某次实验考试结束后,某同学对制取二氧化碳后的废液产生了兴趣,为探究废液中溶质的成分,该同学做了如下实验,请根据所示的实验过程和提供的信息作答:

(1)实验结束后溶液中的溶质为_____ 。
(2)实验所用K2CO3溶液的溶质质量分数为_____ 。
(3)废液中的溶质为_____ ,其在废液中的质量分数为_____ (若溶质不止一种,溶质和其质量分数的前后顺序要对应)。

(1)实验结束后溶液中的溶质为
(2)实验所用K2CO3溶液的溶质质量分数为
(3)废液中的溶质为
您最近一年使用:0次
计算题
|
困难
(0.15)
真题
解题方法
【推荐3】某腐蚀印刷电路板的废液经处理后只含有CuCl2和FeCl2两种溶质,为了分析处理后废液的组成,取200g该废液加入40g废铁屑(杂质不溶于水,也不参与反应),恰好完全反应,过滤经处理得到16g铜,往滤液中加入足量的硝酸银溶液,经过滤、干燥、称量,最终得到114.8gAgCl固体。回答下列问题:
(1)往废液中加入废铁屑发生反应的化学方程式为_______________,往滤液中加入硝酸银溶液发生反应的化学方程式为___________________。
(2)求滤液中溶质的质量分数为________________(精确到1%)。
(3)求200g废液中FeCl2的质量分数为________________(精确到1%)。
(1)往废液中加入废铁屑发生反应的化学方程式为_______________,往滤液中加入硝酸银溶液发生反应的化学方程式为___________________。
(2)求滤液中溶质的质量分数为________________(精确到1%)。
(3)求200g废液中FeCl2的质量分数为________________(精确到1%)。
您最近一年使用:0次



