小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
(1)用实际参加反应的粒子表示锌与稀盐酸反应的实质___________ 。
(2)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有___________ 、___________ 。其中,实验1和实验2进行对照实验,探究的影响反应速率的因素是___________ 。
(3)可以通过比较___________ 实验数据来确定金属和酸反应的快慢。
(4)根据其他测定方法,实验小组的同学绘制了锌粒与稀盐酸反应产生氢气的速率随时间变化的曲线,如图所示。请据图分析:
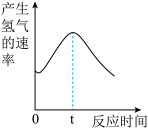
时间0-t内,反应速率逐渐加快的主要原因是___________ ,时间t以后,反应速率逐渐减慢的主要原因是___________ 。
某金属与同体积盐酸溶液反应实验数据表
| 实验编号 | 盐酸溶液浓度 | 反应开始时酸溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 1 | 10% | 20℃ | 19ml | 118ml |
| 2 | 15% | 20℃ | 28ml | 175ml |
| 3 | 10% | 35℃ | 72ml | 118ml |
| 4 | 15% | 35℃ | 103ml | 175ml |
(1)用实际参加反应的粒子表示锌与稀盐酸反应的实质
(2)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有
(3)可以通过比较
(4)根据其他测定方法,实验小组的同学绘制了锌粒与稀盐酸反应产生氢气的速率随时间变化的曲线,如图所示。请据图分析:

时间0-t内,反应速率逐渐加快的主要原因是
更新时间:2024-03-13 09:36:10
|
相似题推荐
【推荐1】化学社团开展“研究钢铁防护的方法”的实践性作业。
【查阅资料】
钢铁膜化处理是钢铁防护的重要方法,其目的是在钢铁表面形成致密、均匀的保护膜。检验膜的抗腐蚀性能要做“滴铜实验”,即往钢铁表面滴加含硫酸铜的腐蚀剂,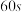 后钢铁表面才出现红色物质,表明抗腐蚀性能达标,且越迟出现红色物质的越好。
后钢铁表面才出现红色物质,表明抗腐蚀性能达标,且越迟出现红色物质的越好。
Ⅰ、验证膜的抗腐蚀性能
【实验1】将有膜化和未膜化的薄钢片分别进行滴铜实验,有膜化的薄钢片出现红色物质的时间明显推迟。
(1)出现红色物质的原因是______ (用化学方程式表示)。
(2)有膜化的薄钢片出现红色物质的时间明显推迟,其原因是______ 。
Ⅱ、探究不同pH的膜化剂对膜层外观的影响
已知: 时,膜化剂不稳定。
时,膜化剂不稳定。
【实验2】膜化剂浓度相同时,将薄钢片放入 、不同pH的膜化剂中浸泡
、不同pH的膜化剂中浸泡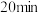 ,观察钢片表面形成的膜层外观。结果如下:
,观察钢片表面形成的膜层外观。结果如下:
(3)根据实验结果,膜层外观符合要求的pH的范围为______ 。
(4)反思上述活动,影响钢铁膜化处理效果的因素还有:______ (写一条)。
【查阅资料】
钢铁膜化处理是钢铁防护的重要方法,其目的是在钢铁表面形成致密、均匀的保护膜。检验膜的抗腐蚀性能要做“滴铜实验”,即往钢铁表面滴加含硫酸铜的腐蚀剂,
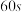 后钢铁表面才出现红色物质,表明抗腐蚀性能达标,且越迟出现红色物质的越好。
后钢铁表面才出现红色物质,表明抗腐蚀性能达标,且越迟出现红色物质的越好。Ⅰ、验证膜的抗腐蚀性能
【实验1】将有膜化和未膜化的薄钢片分别进行滴铜实验,有膜化的薄钢片出现红色物质的时间明显推迟。
(1)出现红色物质的原因是
(2)有膜化的薄钢片出现红色物质的时间明显推迟,其原因是
Ⅱ、探究不同pH的膜化剂对膜层外观的影响
已知:
 时,膜化剂不稳定。
时,膜化剂不稳定。【实验2】膜化剂浓度相同时,将薄钢片放入
 、不同pH的膜化剂中浸泡
、不同pH的膜化剂中浸泡 ,观察钢片表面形成的膜层外观。结果如下:
,观察钢片表面形成的膜层外观。结果如下:| pH | 1.5 | 2.0 | 2.5 | 3.0 |
| 膜层外观 | 易脱落 | 粗糙 | 致密、均匀 | 致密、均匀 |
(4)反思上述活动,影响钢铁膜化处理效果的因素还有:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】某校化学兴趣小组在进行氧化铜与稀硫酸反应的实验时,观察到有红色固体出现,上层清液呈浅绿色。同学们对此异常现象进行如下探究。
【作出猜想】依据实验现象并结合所学化学知识,大家一致猜想用于实验的氧化铜不纯,其中一定混有铁。
【实验探究1】
(1)为了验证猜想,甲同学征求老师同意,重新取一份纯净的氧化铜,加入足量溶质质量分数为9.8%的稀硫酸进行实验。观察到___________ 的现象,说明纯净的氧化铜与稀硫酸反应不会出现上述异常现象。对比分析,证明用于实验的氧化铜不纯混有铁。
(2)乙同学认为无需通过化学方法,只需进行操作___________ ,就能证明猜想正确。
(3)请你写出上述不纯的氧化铜加入足量的稀硫酸充分反应,生成红色固体的化学方程式___________ 。
【提出问题】老师肯定了同学们的猜想,并提出问题:混有铁的氧化铜粉末在与稀硫酸发生反应时,反应的先后顺序是怎样的?
(4)同学们分析后认为该实验过程中可能会发生三个反应:
①氧化铜与稀硫酸反应;
②铁与___________ 反应;
③生成红色固体的反应。
【实验探究2】老师提示大家,铁和氧化铜用量的差异及硫酸的质量分数对反应先后顺序都会产生影响,在老师的指导下同学们设计下表所示的实验探究其中一个因素的影响:
(5)上表中m=___________ ,n=___________ 。
【实验结论】
(6)从上述实验可以得出,在硫酸足量且质量分数均为9.8%的情况下,反应的先后顺序为___________ (用①②③排序)。
【反思交流】
(7)①对比分析实验Ⅱ和Ⅲ,写出实验Ⅱ中无气泡产生的原因___________ 。
②要验证探究实验中稀硫酸是否过量,可测定实验后液体的pH,用pH试纸测定溶液pH的方法是在白瓷板上放一小片pH试纸,___________ 。
【作出猜想】依据实验现象并结合所学化学知识,大家一致猜想用于实验的氧化铜不纯,其中一定混有铁。
【实验探究1】
(1)为了验证猜想,甲同学征求老师同意,重新取一份纯净的氧化铜,加入足量溶质质量分数为9.8%的稀硫酸进行实验。观察到
(2)乙同学认为无需通过化学方法,只需进行操作
(3)请你写出上述不纯的氧化铜加入足量的稀硫酸充分反应,生成红色固体的化学方程式
【提出问题】老师肯定了同学们的猜想,并提出问题:混有铁的氧化铜粉末在与稀硫酸发生反应时,反应的先后顺序是怎样的?
(4)同学们分析后认为该实验过程中可能会发生三个反应:
①氧化铜与稀硫酸反应;
②铁与
③生成红色固体的反应。
【实验探究2】老师提示大家,铁和氧化铜用量的差异及硫酸的质量分数对反应先后顺序都会产生影响,在老师的指导下同学们设计下表所示的实验探究其中一个因素的影响:
| 实验 | 物质X/g | 氧化铜/g | 9.8%稀硫酸/mL | 实验现象 |
| I | 0.56 | 1.6 | n | 出现红色固体,无气泡产生,充分反应后上层清液呈蓝色 |
| Ⅱ | 1.12 | m | 100 | 出现红色固体,无气泡产生,充分反应后上层清液呈浅绿色 |
| Ⅲ | 1.68 | 1.6 | 100 | 出现红色固体,待红色固体不再增加后产生大量气泡,充分反应后上层清液呈浅绿色 |
【实验结论】
(6)从上述实验可以得出,在硫酸足量且质量分数均为9.8%的情况下,反应的先后顺序为
【反思交流】
(7)①对比分析实验Ⅱ和Ⅲ,写出实验Ⅱ中无气泡产生的原因
②要验证探究实验中稀硫酸是否过量,可测定实验后液体的pH,用pH试纸测定溶液pH的方法是在白瓷板上放一小片pH试纸,
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】M是生产、生活中常见的金属。张老师化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。
【查阅资料】MSO4溶液是无色液体。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小玉的猜想是M>Al>Cu;小静的猜想是Al>M>Cu;你的猜想是_______ 。
【设计与实验一】小影取长短、粗细相同的M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如下表的实验(试管中均盛有相同体积、相同浓度的稀盐酸)。
【交流与表达】同学们对同一实验得出两种不同结论的现象进行了讨论,明白了实验刚开始时试管③中无气泡产生的原因是铝丝表面的氧化膜与稀盐酸反应,因而无气泡产生。
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取长短、粗细相同、打磨干净的M丝、铝丝及相关溶液,又进行了如下图所示的实验:_____ 。
(2)试管丙中反应的化学方程式为_____ 。
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管______ (填试管编号)中的实验,也可以得出正确的结论。
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【拓展与延伸】实验结束,同学们积极性未减,兴趣小组的同学们又做了下面的实验。向盛有Cu(NO3)2溶液的烧杯中加入一定量的锌粉和银粉的混合物,充分反应后过滤,得到滤渣和无色滤液。请你帮助回答,下列判断正确的是______ 。(填序号)
A.滤渣中一定不含锌,一定含有铜和银
B.滤渣中含有两种或三种固体
C.滤液中一定含Zn(NO3)2,一定不含AgNO3
D.滤液中一定含Zn(NO3)2,可能含AgNO3和Cu(NO3)2
【查阅资料】MSO4溶液是无色液体。
【提出问题】M、铜、铝的金属活动性顺序是怎样的?
【猜想与假设】小玉的猜想是M>Al>Cu;小静的猜想是Al>M>Cu;你的猜想是
【设计与实验一】小影取长短、粗细相同的M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如下表的实验(试管中均盛有相同体积、相同浓度的稀盐酸)。
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu;M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 |
【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取长短、粗细相同、打磨干净的M丝、铝丝及相关溶液,又进行了如下图所示的实验:
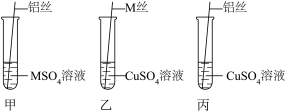
(2)试管丙中反应的化学方程式为
【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管
【解释与结论】通过以上实验,同学们得出了三种金属的活动性顺序。
【拓展与延伸】实验结束,同学们积极性未减,兴趣小组的同学们又做了下面的实验。向盛有Cu(NO3)2溶液的烧杯中加入一定量的锌粉和银粉的混合物,充分反应后过滤,得到滤渣和无色滤液。请你帮助回答,下列判断正确的是
A.滤渣中一定不含锌,一定含有铜和银
B.滤渣中含有两种或三种固体
C.滤液中一定含Zn(NO3)2,一定不含AgNO3
D.滤液中一定含Zn(NO3)2,可能含AgNO3和Cu(NO3)2
您最近一年使用:0次
【推荐1】小彬同学家新买了水龙头,从说明书上了解到该水龙头是铜质镀铬的.他想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动.
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜,铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
【回答问题】
(1)把上表填写完整①______ ;②______ ;③______ 。
(2)用砂纸打磨金属片的目的是______ 。
(3)实验一所发生反应的化学方程式是______ 。
(4)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是_______ 。
(5)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是______ 。
(6)某金属的样品(杂质不参与反应)10g与73g质量分数为10%的稀盐酸恰好完全反应,生成氢气和金属R的化合物。已知金属R的化合物中氯元素的质量分数为45%,则该样品中R的质量分数为______ ( 计算结果精确到0.1%)。
【查阅资料】铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜,铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液…
铝是银白色有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【预测】三种金属在金属活动性顺序中的相对位置关系:
①Cr Al Cu ②Al Cr Cu ③Al Cu Cr
【实验过程】取大小相同的三种金属薄片,用砂纸打磨光亮。
| 实验一 | 实验二 | 实验三 | |
| 实验方案 |  |  |  |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变蓝色。 | ①___________ | 铝片表面产生气泡较快 |
| 结论 | 铬能和稀硫酸发生反应,反应速率较慢。 | 铜不与稀硫酸反应 | ②_________ |
| 三种金属在金属活动性顺序中的相对位置关系是③__________ | |||
【回答问题】
(1)把上表填写完整①
(2)用砂纸打磨金属片的目的是
(3)实验一所发生反应的化学方程式是
(4)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是
(5)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种药品可以是
(6)某金属的样品(杂质不参与反应)10g与73g质量分数为10%的稀盐酸恰好完全反应,生成氢气和金属R的化合物。已知金属R的化合物中氯元素的质量分数为45%,则该样品中R的质量分数为
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】从2008年我国暖贴企业崛起到现在,“暖贴”一直是淘宝冬季畅销商品。今天同学们在实验室打开一片暖贴,对其中黑色粉末的有效成分及发热原理展开了探究。
【查阅资料】暖贴的主要成分是:铁粉、蛭石、活性炭、无机盐、水等。
探究 I:黑色粉末成分的探究
【进行实验】研究小组先用磁铁对黑色粉末进行分离,将分离出的样品标记为样品 1,剩余固体标记为样品 2。
【表达与交流】
(1)铁丝在空气中不能燃烧而铁粉可以,是因为反应物间的______ 反应速率越快。
(2)同学们经讨论,检验样品 1 中铁粉的存在方案还可以设计为______ 。
A.放入稀盐酸中 B.放入硫酸锌溶液中 C.用手掂一掂质量探究
Ⅱ:暖贴的发热原理
【提出猜想】“暖贴”反应原理与铁的生锈本质一致
【进行实验】研究小组将拆除包装的暖贴倒入三颈烧瓶中,密封装置,按图甲(夹持仪器已略去)采用传感器收集相关数据,并观察曲线变化(如图乙 A、B、C)。


【解释与结论】从收集到的图像看,暖贴发热是因为颗粒微小的铁粉与______ 和氧气等物质发生反应,将______ 能转变为热能,这一反应与铁生锈原理一致。
【反思与交流】某同学质疑:铁生锈是一个极其缓慢的氧化过程,而“暖贴”却可以短时间内快速放热,试结合成分分析原因:______ 。
【查阅资料】暖贴的主要成分是:铁粉、蛭石、活性炭、无机盐、水等。
探究 I:黑色粉末成分的探究
【进行实验】研究小组先用磁铁对黑色粉末进行分离,将分离出的样品标记为样品 1,剩余固体标记为样品 2。
| 实验步骤 | 实验现象 | 结论 |
| (1)用棉花球蘸取样品 1,置于酒精灯上点燃 | 黑色粉末中有铁粉 | |
| (2)取少量样品 2 于试管中,通入氧气点燃,产物通入澄清石灰水 | 黑色粉末燃烧, | 黑色粉末中有碳粉 |
(1)铁丝在空气中不能燃烧而铁粉可以,是因为反应物间的
(2)同学们经讨论,检验样品 1 中铁粉的存在方案还可以设计为
A.放入稀盐酸中 B.放入硫酸锌溶液中 C.用手掂一掂质量探究
Ⅱ:暖贴的发热原理
【提出猜想】“暖贴”反应原理与铁的生锈本质一致
【进行实验】研究小组将拆除包装的暖贴倒入三颈烧瓶中,密封装置,按图甲(夹持仪器已略去)采用传感器收集相关数据,并观察曲线变化(如图乙 A、B、C)。


【解释与结论】从收集到的图像看,暖贴发热是因为颗粒微小的铁粉与
【反思与交流】某同学质疑:铁生锈是一个极其缓慢的氧化过程,而“暖贴”却可以短时间内快速放热,试结合成分分析原因:
您最近一年使用:0次
科学探究题
|
适中
(0.65)
名校
解题方法
【推荐3】在进行酸碱中和反应的实验探究时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记添加酸碱指示剂。从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到试管中溶液不变色。于是针对此溶液的成分,进行了科学探究。
(1)猜想与假设:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三:______ 。
经过讨论后觉得猜想一不正确,其理由是:______ 。
(2)设计并进行实验:
①为了验证猜想,设计了实验方案一:
②请你另外设计两个实验方案(要与实验方案一化学反应原理不同),验证猜想三成立,并填写下表:
可选择的药品有:锌粒、铜片、碳粉、石灰石颗粒、碳酸钠粉末、二氧化锰
(1)猜想与假设:
猜想一:反应后氢氧化钠过量,溶液呈碱性;
猜想二:氢氧化钠与盐酸恰好完全中和,溶液呈中性;
猜想三:
经过讨论后觉得猜想一不正确,其理由是:
(2)设计并进行实验:
①为了验证猜想,设计了实验方案一:
| 实验步骤 | 实验现象 | 实验结论 |
| 用洁净、干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与 | pH | 猜想二不成立 猜想三成立 |
②请你另外设计两个实验方案(要与实验方案一化学反应原理不同),验证猜想三成立,并填写下表:
可选择的药品有:锌粒、铜片、碳粉、石灰石颗粒、碳酸钠粉末、二氧化锰
| 实验步骤 | 实验现象 | 实验结论 |
| 猜想三成立 | ||
| 猜想三成立 |
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐1】等质量的铁粉与过量的稀盐酸在不同的实验条件下进行反应(如表)。分别测定不同时间内产生气体体积的数据,绘制得到图1所示曲线。

(1)写出铁粉与稀盐酸反应的化学方程式:__________ 。
(2)对比实验①③,得出其他条件相同时,___________ ,铁与盐酸反应速率越快;要比较盐酸的浓度对反应速率的影响,应选择的实验是_________ (填序号)。

【进一步探究】
(3)图2中乙为用压强传感器测得的室温下足量的三种金属片分别与20mL10%的稀盐酸反应(如甲所示)产生氢气的体积与反应时间的关系曲线(产生氢气的体积用装置内压强表示,在等温条件下,产生氢气的体积与装置内压强成正比)。
①实验中还要控制的变量是_________ 。
②结合化学方程式计算,在图乙的情况下,产生相同体积的氢气,则所需三种金属的质量关系为__________ 。
【拓展提高】
(4)图3为用压强传感器测得的室温下足量的镁片与20mL10%的稀盐酸反应产生氢气的体积(用装置内压强表示)与反应时间的关系曲线,发现实验测得的数值比通过计算得到的理论值偏大,可能的原因是:①___________ ;②_________ 。
| 序号 | 盐酸的浓度/% | 温度/℃ |
| ① | 7 | 30 |
| ② | 10 | 50 |
| ③ | 7 | 20 |
| ④ | 10 | 30 |

(1)写出铁粉与稀盐酸反应的化学方程式:
(2)对比实验①③,得出其他条件相同时,

【进一步探究】
(3)图2中乙为用压强传感器测得的室温下足量的三种金属片分别与20mL10%的稀盐酸反应(如甲所示)产生氢气的体积与反应时间的关系曲线(产生氢气的体积用装置内压强表示,在等温条件下,产生氢气的体积与装置内压强成正比)。
①实验中还要控制的变量是
②结合化学方程式计算,在图乙的情况下,产生相同体积的氢气,则所需三种金属的质量关系为
【拓展提高】
(4)图3为用压强传感器测得的室温下足量的镁片与20mL10%的稀盐酸反应产生氢气的体积(用装置内压强表示)与反应时间的关系曲线,发现实验测得的数值比通过计算得到的理论值偏大,可能的原因是:①
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐2】学完金属的化学性质后,小明用下列仪器和试剂验证影响金属与盐酸反应速率的因素:
仪器:烧杯、试管夹、酒精灯、药匙、量筒。药品:锌片、铁片、铁粉、6%盐酸、25%盐酸。

Ⅰ、不同状态的金属与酸反应的速率不同
取质量相等的铁片和铁粉,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示。
(1)为完成该实验,需要补充的一种仪器是_____________ 。
(2)曲线B对应的物质是_____________ 。
(3)请写出铁与稀盐酸反应的化学方程式:_____________ 。
(4)由此实验得到的结论是_____________ 。
Ⅱ、金属与不同溶质质量分数的盐酸反应的速率不同
取质量相等的锌片,分别放入6%、25%的足量稀盐酸中。生成氢气的质量为m,反应时间为t。25%的盐酸与锌片反应的关系曲线如图2所示。
(1)请在该图上补画出6%的盐酸与锌片反应的关系曲线。_________
(2)由此实验得到的结论是_____________ 。
Ⅲ、温度对金属与盐酸的反应速率也有影响,取两个烧杯,分别加入等质量的_____________ (填“同种”或“不同种”)金属,再分别加入足量的溶质质量分数 _____________ (填“相同”或“不相同”)的稀盐酸。
(1)曲线C的温度比曲线D的温度_____________ (填“高”、“低”或“相等”)。
(2)由此实验得到的结论是_____________ 。
仪器:烧杯、试管夹、酒精灯、药匙、量筒。药品:锌片、铁片、铁粉、6%盐酸、25%盐酸。

Ⅰ、不同状态的金属与酸反应的速率不同
取质量相等的铁片和铁粉,分别放入溶质质量分数相同的足量稀盐酸中,生成氢气的质量(m)与反应时间(t)的关系曲线如图1所示。
(1)为完成该实验,需要补充的一种仪器是
(2)曲线B对应的物质是
(3)请写出铁与稀盐酸反应的化学方程式:
(4)由此实验得到的结论是
Ⅱ、金属与不同溶质质量分数的盐酸反应的速率不同
取质量相等的锌片,分别放入6%、25%的足量稀盐酸中。生成氢气的质量为m,反应时间为t。25%的盐酸与锌片反应的关系曲线如图2所示。
(1)请在该图上补画出6%的盐酸与锌片反应的关系曲线。
(2)由此实验得到的结论是
Ⅲ、温度对金属与盐酸的反应速率也有影响,取两个烧杯,分别加入等质量的
(1)曲线C的温度比曲线D的温度
(2)由此实验得到的结论是
您最近一年使用:0次
科学探究题
|
适中
(0.65)
解题方法
【推荐3】化学活动小组为探究铜、镁、铁、银等几种金属活动顺序,进行了如下实验。
【实验1】在四支装有相同大小铜、镁、铁、银的试管中,分别加入5mL的稀盐酸,观察现象,发现镁、铁能与盐酸反应,并有气泡产生,铜、银却不能。
【结论】由实验1得出______ (填字母)。
A金属活动性由强到弱顺序是:镁>铁>铜>银
B镁、铁的活动性比铜、银强
C可把四种金属分为两类,镁、铁为一类,铜、银为另一类
写出镁与盐酸发生反应的化学方程式______ 。
观察时发现:镁比铁产生气泡的速度快,回顾学过的知识,打磨后的镁条在空气中即可点燃,而铁丝需在盛有纯净氧气的集气瓶中才可被点燃,种种现象说明镁的活动性比铁强。铁在氧气中燃烧的现象为______ ,生成一种黑色固体。
【实验2】探究铜、银金属的活动性顺序。在以下的设计方案中,最好的方法是______ (填字母)。
A将铜、银分别放进相同浓度和体积的稀硫酸中
B将铜、银分别在相同条件下与氧气反应
C将铜放进硝酸银溶液中
选用上述方法的原因是______ (用化学方程式表示)。
【实验3】测定不同浓度的盐酸对反应速率的影响。将相同质量和相同形状的镁分别放入两种不同浓度的足量的盐酸溶液里,记录收集相同体积的气体所需要的时间。
【结论】镁在浓度大的盐酸中反应速率快。
【作图】将不同浓度的盐酸对反应速率的影响绘制成如下坐标图,与结论相符合的是______ (填字母)。如果用a、b分别表示镁与两种不同浓度盐酸反应形成的曲线,在符合事实的坐标图里,表示镁与浓度大的盐酸反应形成的曲线是______ (填“a”或“b”)。

【实验1】在四支装有相同大小铜、镁、铁、银的试管中,分别加入5mL的稀盐酸,观察现象,发现镁、铁能与盐酸反应,并有气泡产生,铜、银却不能。
【结论】由实验1得出
A金属活动性由强到弱顺序是:镁>铁>铜>银
B镁、铁的活动性比铜、银强
C可把四种金属分为两类,镁、铁为一类,铜、银为另一类
写出镁与盐酸发生反应的化学方程式
观察时发现:镁比铁产生气泡的速度快,回顾学过的知识,打磨后的镁条在空气中即可点燃,而铁丝需在盛有纯净氧气的集气瓶中才可被点燃,种种现象说明镁的活动性比铁强。铁在氧气中燃烧的现象为
【实验2】探究铜、银金属的活动性顺序。在以下的设计方案中,最好的方法是
A将铜、银分别放进相同浓度和体积的稀硫酸中
B将铜、银分别在相同条件下与氧气反应
C将铜放进硝酸银溶液中
选用上述方法的原因是
【实验3】测定不同浓度的盐酸对反应速率的影响。将相同质量和相同形状的镁分别放入两种不同浓度的足量的盐酸溶液里,记录收集相同体积的气体所需要的时间。
【结论】镁在浓度大的盐酸中反应速率快。
【作图】将不同浓度的盐酸对反应速率的影响绘制成如下坐标图,与结论相符合的是

您最近一年使用:0次



