石灰石是一种常见的矿石,其应用十分广泛。
(1)牙膏中含有一定量的摩擦剂(主要成分为碳酸钙),推测摩擦剂应具备的性质有_________(多选,填序号)。
(2)火力发电厂常用石灰石浆吸收废气中的二氧化硫,原理为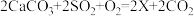 ,X的化学式为
,X的化学式为___________ 。
(3)工业煅烧石灰石制二氧化碳,化学方程式为___________ 。
(4)某实验小组用73g质量分数为20%的盐酸与足量石灰石反应制取二氧化碳,生成二氧化碳的质量是多少?(写出详细计算过程)
(1)牙膏中含有一定量的摩擦剂(主要成分为碳酸钙),推测摩擦剂应具备的性质有_________(多选,填序号)。
| A.易溶于水 | B.坚硬 | C.无毒 | D.颗粒较小 |
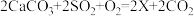 ,X的化学式为
,X的化学式为(3)工业煅烧石灰石制二氧化碳,化学方程式为
(4)某实验小组用73g质量分数为20%的盐酸与足量石灰石反应制取二氧化碳,生成二氧化碳的质量是多少?(写出详细计算过程)
更新时间:2024-04-03 18:41:15
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】如图为某品牌化肥的标签。

为测定该化肥中(NH4)2SO4的含量,小红称取5g该化肥放入烧杯中,加水至完全溶解(杂质溶于水但不参加反应),再将200gBa(OH)2溶液分4次加入其中。测得数据如下表所示:
(1)请把测定过程中反应的化学方程式补充完整:
 。
。
(2)表中m的值为___________。
(3)计算化肥中(NH4)2SO4的质量分数并判断该化肥是否合格。(写出计算过程)
(4)请在下图画出产生沉淀质量与加入Ba(OH)2溶液质量的关系图。(要标注必要的数值)


为测定该化肥中(NH4)2SO4的含量,小红称取5g该化肥放入烧杯中,加水至完全溶解(杂质溶于水但不参加反应),再将200gBa(OH)2溶液分4次加入其中。测得数据如下表所示:
| 次数 | 1 | 2 | 3 | 4 |
| 加入Ba(OH)2溶液质量/g | 50 | 50 | 50 | 50 |
| 生成沉淀质量/g | 2.33 | 4.66 | m | 6.99 |
 。
。(2)表中m的值为___________。
(3)计算化肥中(NH4)2SO4的质量分数并判断该化肥是否合格。(写出计算过程)
(4)请在下图画出产生沉淀质量与加入Ba(OH)2溶液质量的关系图。(要标注必要的数值)

您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】已知某纯净物2.3g在足量的氧气中充分燃烧后,生成4.4g二氧化碳和2.7g水。请计算该纯净物中是否含有氧元素?若有,氧元素的质量为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】某阻燃剂主要成分为碱式碳酸镁[Mga(OH)2(CO3)b•5H2O],遇热分解生成三种氧化物,分别是H2O、CO2和______ 。称取一定质量碱式碳酸镁充分灼烧,将产生的气体依次通过浓硫酸(仅吸收水蒸气)和过量澄清石灰水,浓硫酸增重0.54g,澄清石灰水中生成2g白色沉淀。则Mga(OH)2(CO3)b•5H2O中a值为______ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】氮化铝是一种重要的化工原料。已知它可以通过以下反应制备:Al2O3+N2+3C=2AlN+3X。
(1)X的化学式为_____ 。
(2)生产4.1kg的氮化铝,需要纯度为60%的氧化铝多少千克?
(1)X的化学式为
(2)生产4.1kg的氮化铝,需要纯度为60%的氧化铝多少千克?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)无土栽培是一种农业高新技术,它可以显著提高农作物的产量和质量。经检测发现某无土栽培技术所使用的营养液中含有一定量的NH4NO3。
①NH4NO3由___ 种元素组成,其相对分子质量为__________ 。
②NH4NO3中氮元素的质量分数为_________ 。
(2)“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为 。在20℃时,取200g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g,
。在20℃时,取200g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g,
请分析并计算回答:
①根据质量守恒定律可知,上述反应中x=________ 。
②上述过程中同时产生H2____ 克?(写出计算过程)
①NH4NO3由
②NH4NO3中氮元素的质量分数为
(2)“氯碱工业”是我国目前化学工业的重要支柱之一,它的主要原理是电解饱和食盐水,其化学方程式为
 。在20℃时,取200g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g,
。在20℃时,取200g饱和NaCl溶液进行电解,一段时间后测得产生氯气(Cl2)的质量为7.1g,请分析并计算回答:
①根据质量守恒定律可知,上述反应中x=
②上述过程中同时产生H2
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】随着人类现代化程度迅速提高,温室气体(CO2)排放日益增加,为降低温室气体含量,科学家正在研究一种新型的“人造树叶”,该“人造树叶”可吸收CO2并转化为乙醇(C2H5OH)燃料,化学方程式为 ,请回答:
,请回答:
(1)根据化学方程式,可知生成物M的化学式为_____。
(2)若每1升“人造树叶”每天可产生460g乙醇,请计算理论上吸收二氧化碳的质量。
 ,请回答:
,请回答:(1)根据化学方程式,可知生成物M的化学式为_____。
(2)若每1升“人造树叶”每天可产生460g乙醇,请计算理论上吸收二氧化碳的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】水泥厂是以粘土和石灰石为原料烧制水泥,为检测石灰石中碳酸钙的纯度,在实验室用6.5g样品与10g稀盐酸恰好完全反应,测得残余物的质量为14.3g(杂质不参加反应),求:
(1)生成二氧化碳 g。
(2)求该石灰石样品中碳酸钙的质量分数为多少?(写出计算过程,结果保留一位小数)
(1)生成二氧化碳 g。
(2)求该石灰石样品中碳酸钙的质量分数为多少?(写出计算过程,结果保留一位小数)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】100g质量分数为9.8%的稀硫酸中:(相对原子质量:H-1 O-16 S-32 Zn-65)
(1)最多可溶解的锌的质量为多少?
(2)同时产生氢气的质量为多少?
(3)反应后所得溶液中溶质的质量分数为多少?
(1)最多可溶解的锌的质量为多少?
(2)同时产生氢气的质量为多少?
(3)反应后所得溶液中溶质的质量分数为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】已知碳酸氢钙[Ca(HCO3)2]为白色固体,易溶于水,在加热时会分解成碳酸钙,反应原理为Ca(HCO3)2  CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:
CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:______ 。(填“酸”“碱”或“盐”)
(2)加热至______ ℃时,碳酸氢钙分解完全。
(3)利用图像数据计算生成氧化钙的质量。(写出计算过程)
(4)32.4g碳酸氢钙固体在整个加热过程中释放二氧化碳的总质量为______ g。
 CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:
CaCO3+H2O+CO2↑,碳酸钙在高温下会继续分解产生氧化钙。如图是32.4g碳酸氢钙固体加热过程中固体质量随温度的变化关系。请回答:
(2)加热至
(3)利用图像数据计算生成氧化钙的质量。(写出计算过程)
(4)32.4g碳酸氢钙固体在整个加热过程中释放二氧化碳的总质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】某中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以下信息计算:

(1)生成二氧化碳的质量为______ g。
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量是多少克?

(1)生成二氧化碳的质量为
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量是多少克?
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】为测定实验室中标签缺失的某瓶稀盐酸的溶质质量分数,小明取100g稀盐酸进行测定实验,将100g大理石分5次加入到稀盐酸中,充分反应后测得生成气体的总质量如表所示。(大理石中的杂质不参加反应)

(1)表格中m的值为_____ ;
(2)计算稀盐酸中溶质的质量分数(请写出计算过程,计算结果精确到0.1%)。

| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
| 加入大理石的质量/g | 20 | 20 | 20 | 20 | 20 |
| 生成气体的质量/g | 1.1 | 2.2 | m | 4.4 | 4.4 |
(2)计算稀盐酸中溶质的质量分数(请写出计算过程,计算结果精确到0.1%)。
您最近一年使用:0次



