牙膏中的磨料可用轻质碳酸钙制作,某同学设计了利用贝壳制取轻质碳酸钙的转化流程如图。A~G为初中化学常见物质,其中G可用于农业上选种。请回答:
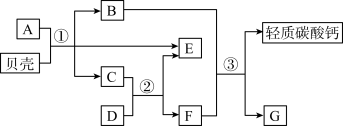
(1)G的化学式为______ 。
(2)轻质碳酸钙可制作补钙剂,可预防老年人______ 。
(3)写出①过程发生反应的化学方程式______ 。
(4)写出E物质的一种用途______ 。

(1)G的化学式为
(2)轻质碳酸钙可制作补钙剂,可预防老年人
(3)写出①过程发生反应的化学方程式
(4)写出E物质的一种用途
更新时间:2024-04-02 20:17:56
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
【推荐1】现有六种物质:甲烷、氧气、二氧化碳、水、氮气、二氧化硫,请用化学式填写:
①供给呼吸的气体是_____________ ;②干冰的成分是_________ ;③最常见的溶剂是_________ ;④天然气的主要成分是_________ ;⑤引起酸雨的气体是___________ ;⑥空气中含量最多的气体是_______ .
①供给呼吸的气体是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】把下列物质中符合题目要求的物质的化学式填在横线上。
①二氧化碳;②氧气;③水;④二氧化硫;⑤氮气;⑥空气;⑦红磷。(填化学式)
(1)供给呼吸支持燃烧的气体是______ 。
(2)有刺激性也能形成酸雨的气体是______ 。
(3)能使澄清的石灰水变浑浊的气体是________ 。
(4)常温下呈液态,被誉为“生命之源”的纯净物是________ 。
(5)空气中含量最多且化学性质不活泼的气体是______ 。
①二氧化碳;②氧气;③水;④二氧化硫;⑤氮气;⑥空气;⑦红磷。(填化学式)
(1)供给呼吸支持燃烧的气体是
(2)有刺激性也能形成酸雨的气体是
(3)能使澄清的石灰水变浑浊的气体是
(4)常温下呈液态,被誉为“生命之源”的纯净物是
(5)空气中含量最多且化学性质不活泼的气体是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】水是生命之源、万物之基,是人类宝贵的自然资源。
(1)水的净化河水净化的主要步骤如图所示。有关说法错误的是________
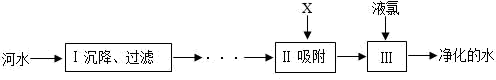
A 步骤Ⅰ可除去难溶性杂质
B X 试剂可以是活性炭
C 步骤Ⅲ可杀菌消毒
D 净化后的水是纯净物
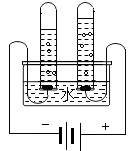
(2)水的组成如图是电解水的实验图,通过电解水的实验得出了水的组成。请写出电解水的化学方程式为________ ,电解时收集到正极、负极气体的质量比为________ 。
(3)水的用途(如图)
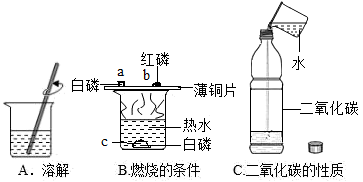
①实验 A 中水作____________ (填“溶剂”或“溶质”)。
②实验 B 中水的作用是提供热量和________ 。
③实验 C 中的水作反应物,与二氧化碳反应生成________ (写名称)。
(4)水的溶液水可以作为溶剂溶解多种物质,如图是甲、乙、丙 三种物质的溶解度曲线。
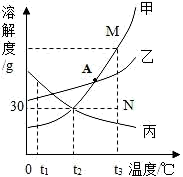
①图中甲和丙的交点的意义是________________ 。
②t1℃时,等质量的甲、乙饱和溶液,其中所含溶质的质量:甲________ 乙(填“大于”、“等于”、“小于”)。
③t2℃时,将 20g 丙溶解于 50g 水中,形成________ g 溶液,溶液的溶质质量分数为 ____________ (保留到 0.1%)。
④分别将 t2℃时甲、乙、丙三种物质的饱和溶液升温至 t3℃,所得 溶液溶质质量分数的大小关系为:____________ (从大到小排列)。
⑤M 点代表 t3℃时甲的____________ 溶液(填“饱和”或“不饱和”),若要将组成在 M 点的甲溶液转变为N 点的甲溶液,可采取____________ 方法。若将甲溶液从状态 A 改变为 N 有多种途径, 试设计并简述一操作最简单、结果最准确的实验途径:先将 A 点的甲的饱和溶液降温到 t2℃,____ ,再将溶液升温至 t3℃。
(1)水的净化河水净化的主要步骤如图所示。有关说法错误的是

A 步骤Ⅰ可除去难溶性杂质
B X 试剂可以是活性炭
C 步骤Ⅲ可杀菌消毒
D 净化后的水是纯净物
(2)水的组成如图是电解水的实验图,通过电解水的实验得出了水的组成。请写出电解水的化学方程式为

(3)水的用途(如图)

①实验 A 中水作
②实验 B 中水的作用是提供热量和
③实验 C 中的水作反应物,与二氧化碳反应生成
(4)水的溶液水可以作为溶剂溶解多种物质,如图是甲、乙、丙 三种物质的溶解度曲线。

①图中甲和丙的交点的意义是
②t1℃时,等质量的甲、乙饱和溶液,其中所含溶质的质量:甲
③t2℃时,将 20g 丙溶解于 50g 水中,形成
④分别将 t2℃时甲、乙、丙三种物质的饱和溶液升温至 t3℃,所得 溶液溶质质量分数的大小关系为:
⑤M 点代表 t3℃时甲的
您最近一年使用:0次
填空与简答-简答题
|
适中
(0.65)
解题方法
【推荐1】请写出四种鉴别稀硫酸与氢氧化钠溶液的方法。
(1)___________________________________
(2)___________________________________
(3)___________________________________
(4)___________________________________
(1)
(2)
(3)
(4)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐2】某同学在实验室中采用如图所示的装置分离 H2、CO2 的混合气体。回答:

(1)X 溶液最好选择(填序号)____________ 。
a.NaOH 浓溶液 b.饱和 Ca(OH)2 溶液 c.浓硫酸
(2)选用稀 H2SO4 而不用盐酸,可能的原因是____________ 。
(3)收集到 H2 的正确操作是____________ ;
(4)洗气瓶中先后发生的反应为(方程式表示)____________ 。

(1)X 溶液最好选择(填序号)
a.NaOH 浓溶液 b.饱和 Ca(OH)2 溶液 c.浓硫酸
(2)选用稀 H2SO4 而不用盐酸,可能的原因是
(3)收集到 H2 的正确操作是
(4)洗气瓶中先后发生的反应为(方程式表示)
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】某同学在学习中构建了“硫及其化合物的价、类关系图”。

(1)I 点物质可以表示硫化钠,写出硫化钠的化学式并注硫元素的化合价______ 。
(2)硫在氧气中燃烧生成气体C的现象是______ 。气体 C的排放会导致空气污染,实验室可以用氢氧化钠溶液吸收,写出该反应的化学方程式_______ 。
(3)①排放到大气中的气体 C 会与氧气、水反应转化为硫酸,进而形成“硫酸型酸雨”。写出化学方程式______ 。
②某学校的化学活动小组用 pH 计精确测定当地降水是否为酸雨,取刚降到地面的雨水水样,每隔几分钟测一次 pH,其数据如表所示:
所降雨水______ (填“是”或“不是”)酸雨。

(1)I 点物质可以表示硫化钠,写出硫化钠的化学式并注硫元素的化合价
(2)硫在氧气中燃烧生成气体C的现象是
(3)①排放到大气中的气体 C 会与氧气、水反应转化为硫酸,进而形成“硫酸型酸雨”。写出化学方程式
②某学校的化学活动小组用 pH 计精确测定当地降水是否为酸雨,取刚降到地面的雨水水样,每隔几分钟测一次 pH,其数据如表所示:
| 测定时间 | 5:05 | 5:10 | 5:15 | 5:20 | 5:25 | 5:30 | 5:35 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 | 4.85 |
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
【推荐1】我国承诺在2030年前CO2排放不再增长。因此,CO2的资源化利用成为研究的热点。
Ⅰ、磷石膏是磷酸生产过程的副产物,主要成分是石膏(CaSO4·2H2O)。用它吸收废气中的CO2可以回收有用的物质。
(1)吸收CO2时,先将磷石膏与氨水混合,再通入CO2,反应后生成(NH4)2SO4和CaCO3,写出化学反应方程式:______ 。
(2)反应后,要检验溶液中的Ca2+已经完全转化为CaCO3,可以向反应后的上层清液中加入______ 试剂,若______ (填现象),则Ca2+已经完全转化。
(3)不同温度下,磷石膏吸收CO2的吸收率如图1温度高于时,CO2的吸收率随温度的升高而降低,原因可能是______ 。

(4)在农业生产中,反应产物(NH4)2SO4可以用作______ 。
Ⅱ、CO2的催化加氢是其资源化利用的重要途径。查阅有关资料得到了以下一些信息:
①在化石燃料利用过程中得到的CO2、H2以及伴生的N2可在一定条件下反应生成碳酸二甲酯(DMC)、甲烷、1,3,5-均三嗪三醇等物质(见表1);
②研究表明,CO2反应的需氢量越少,生产成本越低;
③固碳理论比是指消耗的CO2与固碳产品的质量比。
表1几种CO2资源化利用产物的理论需氢量及固碳理论比
(5)酯化反应的产物碳酸二甲酯(DMC)的化学式为______ 。
(6)CO2催化加氢的转化率(消耗的CO2量与投入CO2量的比值)随温度变化如图2所示,该反应的适宜温度为______ 。
(7)氨化是CO2资源化利用的最佳方式,根据表1中的信息,分析其原因是______ 。
Ⅰ、磷石膏是磷酸生产过程的副产物,主要成分是石膏(CaSO4·2H2O)。用它吸收废气中的CO2可以回收有用的物质。
(1)吸收CO2时,先将磷石膏与氨水混合,再通入CO2,反应后生成(NH4)2SO4和CaCO3,写出化学反应方程式:
(2)反应后,要检验溶液中的Ca2+已经完全转化为CaCO3,可以向反应后的上层清液中加入
(3)不同温度下,磷石膏吸收CO2的吸收率如图1温度高于时,CO2的吸收率随温度的升高而降低,原因可能是

(4)在农业生产中,反应产物(NH4)2SO4可以用作
Ⅱ、CO2的催化加氢是其资源化利用的重要途径。查阅有关资料得到了以下一些信息:
①在化石燃料利用过程中得到的CO2、H2以及伴生的N2可在一定条件下反应生成碳酸二甲酯(DMC)、甲烷、1,3,5-均三嗪三醇等物质(见表1);
②研究表明,CO2反应的需氢量越少,生产成本越低;
③固碳理论比是指消耗的CO2与固碳产品的质量比。
表1几种CO2资源化利用产物的理论需氢量及固碳理论比
| 利用方式 | 原料 | 总反应方程式 | 产物 | 固碳理论比 |
| 酯化 | H2 | 3CO2+6H2=DMC+3H2O | 碳酸二甲酯 | 0.49 |
| 催化加氢 | H2 | CO2+4H2=CH4+2H2O | 甲烷 | 2.75 |
| 氨化 | N2、H2 | 6CO2+3N2+9H2=2C3H3N3O3+6H2O | 1,3,5-均三嗪三醇 | 1.02 |
(5)酯化反应的产物碳酸二甲酯(DMC)的化学式为
(6)CO2催化加氢的转化率(消耗的CO2量与投入CO2量的比值)随温度变化如图2所示,该反应的适宜温度为
(7)氨化是CO2资源化利用的最佳方式,根据表1中的信息,分析其原因是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
解题方法
【推荐2】氢能是全球最具发展潜力的清洁能源之一,是国家推进能源革命的重点方向。某实验室提出一种煤制氢技术,其流程如图所示(其流程中得到的 可用于其它工艺):
可用于其它工艺):

资料1:水煤浆是由煤与水混合而成,经过气化器后转化为 和
和 。
。
资料2:在气化器中发生了两个反应: ,
, 。
。
(1)煤在进入气化器之前,需要将其粉碎与水充分混合成水煤浆,粉碎的目的是______ 。
(2)重整器的作用是_______________ 。
(3)煅烧炉中发生反应的化学方程式为_____________ 。
(4)该生产流程中可循环利用的物质______ 。
 可用于其它工艺):
可用于其它工艺):
资料1:水煤浆是由煤与水混合而成,经过气化器后转化为
 和
和 。
。资料2:在气化器中发生了两个反应:
 ,
, 。
。(1)煤在进入气化器之前,需要将其粉碎与水充分混合成水煤浆,粉碎的目的是
(2)重整器的作用是
(3)煅烧炉中发生反应的化学方程式为
(4)该生产流程中可循环利用的物质
您最近一年使用:0次
填空与简答-科普阅读题
|
适中
(0.65)
解题方法
【推荐3】贵州有丰富的溶洞旅游资源,溶洞的形成是二氧化碳循环的结果。在自然界中,溶有二氧化碳的雨水,会使石灰石构成的岩层部分溶解,使碳酸钙转变成可溶性的碳酸氢钙,其发生的变化为 。溶有较多碳酸氢钙的水从溶洞顶滴到洞底时,由于水分蒸发或者压强减小,以及温度变化,水中的碳酸氢钙会分解析出碳酸钙沉淀,其变化为
。溶有较多碳酸氢钙的水从溶洞顶滴到洞底时,由于水分蒸发或者压强减小,以及温度变化,水中的碳酸氢钙会分解析出碳酸钙沉淀,其变化为 。这些沉淀经过千百年的集聚,渐渐形成了钟乳石、石笋等,从而形成千姿百态的奇异景观。请结合文本回答问题:
。这些沉淀经过千百年的集聚,渐渐形成了钟乳石、石笋等,从而形成千姿百态的奇异景观。请结合文本回答问题:
(1)岩层部分溶解时,发生的化学变化的基本类型为_________________ 。
(2)经测定某溶洞中的水为硬水,其原因可能是________________ 。
(3)不能随意进入溶洞的原因是________________ 。
(4)请写出一种自然界中二氧化碳的消耗途径________________ 。
 。溶有较多碳酸氢钙的水从溶洞顶滴到洞底时,由于水分蒸发或者压强减小,以及温度变化,水中的碳酸氢钙会分解析出碳酸钙沉淀,其变化为
。溶有较多碳酸氢钙的水从溶洞顶滴到洞底时,由于水分蒸发或者压强减小,以及温度变化,水中的碳酸氢钙会分解析出碳酸钙沉淀,其变化为 。这些沉淀经过千百年的集聚,渐渐形成了钟乳石、石笋等,从而形成千姿百态的奇异景观。请结合文本回答问题:
。这些沉淀经过千百年的集聚,渐渐形成了钟乳石、石笋等,从而形成千姿百态的奇异景观。请结合文本回答问题:(1)岩层部分溶解时,发生的化学变化的基本类型为
(2)经测定某溶洞中的水为硬水,其原因可能是
(3)不能随意进入溶洞的原因是
(4)请写出一种自然界中二氧化碳的消耗途径
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐1】酸、碱、盐是我们身边重要的化合物。
(1)碱溶液有许多共同性质,是因为不同的碱溶液中都有_____ (填离子符).
(2)常用胃舒平(主要成分是氢氧化铝)治疗胃酸过多,有关反应的化学方程式是_____ .
(3)将一定量的硝酸铜溶液与氢氧化钠溶液混合,充分反应后过滤,得到无色溶液,该无色溶液中一定含有溶质硝酸钠,可能含有溶质_____ .若要验证这可能含有的溶质,不宜使用_____ (填字母)
A 酚酞试液 B pH试纸 C 硫酸铵 D 氯化钠
(1)碱溶液有许多共同性质,是因为不同的碱溶液中都有
(2)常用胃舒平(主要成分是氢氧化铝)治疗胃酸过多,有关反应的化学方程式是
(3)将一定量的硝酸铜溶液与氢氧化钠溶液混合,充分反应后过滤,得到无色溶液,该无色溶液中一定含有溶质硝酸钠,可能含有溶质
A 酚酞试液 B pH试纸 C 硫酸铵 D 氯化钠
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
真题
【推荐2】纯碱工业始于18世纪,我国制碱工业先驱——侯德榜发明的“侯氏制碱法”,其生产过程涉及的主要化学反应有:
①NH3+X+H2O=NH4HCO3
②NH4HCO3+NaCl=NH4Cl+NaHCO3↓
③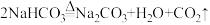
(1)氯化铵中N元素的化合价为________ 。
(2)反应①中X的化学式为________ 。
(3)所制得的“碱”的化学名称为_____ ;写出“碱”与盐酸反应的化学方程式为:__________ 。
①NH3+X+H2O=NH4HCO3
②NH4HCO3+NaCl=NH4Cl+NaHCO3↓
③
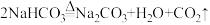
(1)氯化铵中N元素的化合价为
(2)反应①中X的化学式为
(3)所制得的“碱”的化学名称为
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
真题
解题方法
【推荐3】用五个圆表示A(氧化铁)、B(稀盐酸)、C(二氧化碳)、D(碳酸钙)、E(氢氧化钠溶液)五种物质,用两圆相切表示两种物质可以发生反应。请回答下列问题:

(1)将C、D、E三个圆画到图中适当的位置,并标出物质(或溶质)的化学式;______________________________________________________________________ 。
(2)写出A与B反应的现象___________________________ 。
(3)写出有氢氧化钠参加反应的化学方程式________________________________ 。

(1)将C、D、E三个圆画到图中适当的位置,并标出物质(或溶质)的化学式;
(2)写出A与B反应的现象
(3)写出有氢氧化钠参加反应的化学方程式
您最近一年使用:0次



