水是生命之源、万物之基,是人类宝贵的自然资源。
(1)水的净化河水净化的主要步骤如图所示。有关说法错误的是________
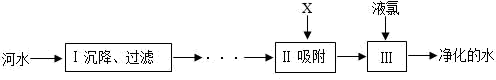
A 步骤Ⅰ可除去难溶性杂质
B X 试剂可以是活性炭
C 步骤Ⅲ可杀菌消毒
D 净化后的水是纯净物
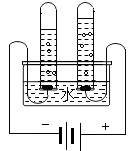
(2)水的组成如图是电解水的实验图,通过电解水的实验得出了水的组成。请写出电解水的化学方程式为________ ,电解时收集到正极、负极气体的质量比为________ 。
(3)水的用途(如图)
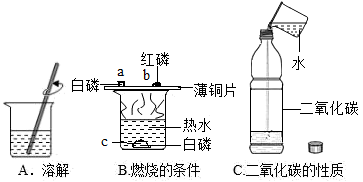
①实验 A 中水作____________ (填“溶剂”或“溶质”)。
②实验 B 中水的作用是提供热量和________ 。
③实验 C 中的水作反应物,与二氧化碳反应生成________ (写名称)。
(4)水的溶液水可以作为溶剂溶解多种物质,如图是甲、乙、丙 三种物质的溶解度曲线。
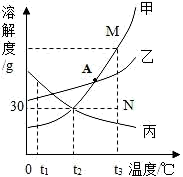
①图中甲和丙的交点的意义是________________ 。
②t1℃时,等质量的甲、乙饱和溶液,其中所含溶质的质量:甲________ 乙(填“大于”、“等于”、“小于”)。
③t2℃时,将 20g 丙溶解于 50g 水中,形成________ g 溶液,溶液的溶质质量分数为 ____________ (保留到 0.1%)。
④分别将 t2℃时甲、乙、丙三种物质的饱和溶液升温至 t3℃,所得 溶液溶质质量分数的大小关系为:____________ (从大到小排列)。
⑤M 点代表 t3℃时甲的____________ 溶液(填“饱和”或“不饱和”),若要将组成在 M 点的甲溶液转变为N 点的甲溶液,可采取____________ 方法。若将甲溶液从状态 A 改变为 N 有多种途径, 试设计并简述一操作最简单、结果最准确的实验途径:先将 A 点的甲的饱和溶液降温到 t2℃,____ ,再将溶液升温至 t3℃。
(1)水的净化河水净化的主要步骤如图所示。有关说法错误的是

A 步骤Ⅰ可除去难溶性杂质
B X 试剂可以是活性炭
C 步骤Ⅲ可杀菌消毒
D 净化后的水是纯净物
(2)水的组成如图是电解水的实验图,通过电解水的实验得出了水的组成。请写出电解水的化学方程式为

(3)水的用途(如图)

①实验 A 中水作
②实验 B 中水的作用是提供热量和
③实验 C 中的水作反应物,与二氧化碳反应生成
(4)水的溶液水可以作为溶剂溶解多种物质,如图是甲、乙、丙 三种物质的溶解度曲线。

①图中甲和丙的交点的意义是
②t1℃时,等质量的甲、乙饱和溶液,其中所含溶质的质量:甲
③t2℃时,将 20g 丙溶解于 50g 水中,形成
④分别将 t2℃时甲、乙、丙三种物质的饱和溶液升温至 t3℃,所得 溶液溶质质量分数的大小关系为:
⑤M 点代表 t3℃时甲的
更新时间:2020-04-16 23:58:49
|
相似题推荐
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,人类的日常生活与工农业生产都离不开水。

(1)电解水的实验装置如图 1所示。通电一段时间后,正极与负极产生的气体体积比为______ ,该反应的化学方程式为______ 。
(2)图 2是用来净化天然水的简易装置,下列分析正确的是______(填标号)。
(3)图 3是自来水厂净水过程的示意图,其中絮凝剂的作用是______ 。
(4)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾受热时发生的反应为 ,则 R的化学式是
,则 R的化学式是______ 。

(1)电解水的实验装置如图 1所示。通电一段时间后,正极与负极产生的气体体积比为
(2)图 2是用来净化天然水的简易装置,下列分析正确的是______(填标号)。
| A.小卵石有过滤作用 | B.能杀菌消毒 |
| C.能把硬水变为软水 | D.净化后的水仍然是混合物 |
(4)高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂。高铁酸钾受热时发生的反应为
 ,则 R的化学式是
,则 R的化学式是
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
【推荐2】水是生命之源,实验小组的同学们想模拟自来水厂的净水过程进行河水净化,最终制取蒸馏水。其实验过程如图所示。请回答以下有关水问题:

(1)A物质的名称是_____ ,操作a的名称是_____ ,若经过操作a后,所得液体C中仍有浑浊,其原因可能是_____ (填写序号)。
①漏斗内的滤纸有破损
②漏斗下端未靠在烧杯内壁
③漏斗内液面高于滤纸的边缘
(2)操作b能除去水中的色素和异味,其操作名称为_____ ,常用到的物质是_____ ,该过程主要是_____ 变化(填“物理”或“化学”)。
(3)小刚取少量液体D与试管中,加入肥皂水,振荡,发现有许多浮渣产生,说明液体是_____ 水。经过操作C以后小刚重复以上实验,他观察到的现象是_____ 。
(4)下列生活中的“水”属于纯净物的是_____ (填字母)。
A 雨水 B 冰水混合物 C 矿泉水 D 地下水
(5)生活中,人们常采用_____ 的方法,既降低水的硬度,又杀菌消毒。

(1)A物质的名称是
①漏斗内的滤纸有破损
②漏斗下端未靠在烧杯内壁
③漏斗内液面高于滤纸的边缘
(2)操作b能除去水中的色素和异味,其操作名称为
(3)小刚取少量液体D与试管中,加入肥皂水,振荡,发现有许多浮渣产生,说明液体是
(4)下列生活中的“水”属于纯净物的是
A 雨水 B 冰水混合物 C 矿泉水 D 地下水
(5)生活中,人们常采用
您最近一年使用:0次
填空与简答-流程题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示,甲、乙是常用的净化水的过程图或装置图。
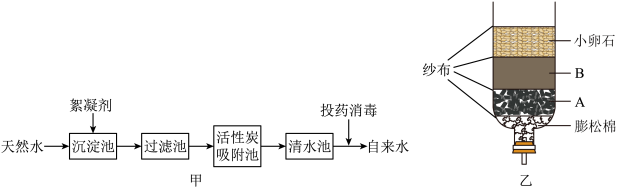
请据图回答:
(1)图甲是自来水的净化过程。
①自来水厂净化水时,没有使用的净水方法有_______ (填字母序号);
A.沉淀 B.过滤 C.吸附 D.蒸馏
②硬水中含有较多的钙离子、镁离子,长期饮用硬水对人体健康不利,生活中可以选用试剂_______ 鉴别硬水和软水。生活中将硬水软化的方法是_______ 。
③消毒剂高铁铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为_______ 。
(2)图乙是一个自制的简易净水器。A B两层需要放置细沙或活性炭,活性炭在净水中的作用是_______ ,根据净化材料特性,A层放置的材料最好是_______ (选“细沙”或“活性炭”)。

请据图回答:
(1)图甲是自来水的净化过程。
①自来水厂净化水时,没有使用的净水方法有
A.沉淀 B.过滤 C.吸附 D.蒸馏
②硬水中含有较多的钙离子、镁离子,长期饮用硬水对人体健康不利,生活中可以选用试剂
③消毒剂高铁铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化。高铁酸钠中铁元素的化合价为
(2)图乙是一个自制的简易净水器。A B两层需要放置细沙或活性炭,活性炭在净水中的作用是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】水是生命之源,无论在生活中还是在化学实验中,水有很大的作用,例如:
①在做硫在氧气中燃烧的实验前,预先要在集气瓶中装少量水,其作用是:______ ;
②在做细铁丝在氧气中燃烧的实验前也预先要在集气瓶中装少量水,其作用是:______ ;
③在测空气组成的实验中更是用到了水,其中预先在集气瓶内装少量水的作用是:______ (只答一个作用即可);烧杯中水的作用是______ ;请你还列出生活中水的作用:______ 。(只答一条)
①在做硫在氧气中燃烧的实验前,预先要在集气瓶中装少量水,其作用是:
②在做细铁丝在氧气中燃烧的实验前也预先要在集气瓶中装少量水,其作用是:
③在测空气组成的实验中更是用到了水,其中预先在集气瓶内装少量水的作用是:
您最近一年使用:0次
填空与简答-推断题
|
适中
(0.65)
解题方法
【推荐2】如图是几种物质之间的转化示意图,其中A、B、C、D均含有同种元素,B是最常用的溶剂,A、C、D中都有人体中含量最高的金属元素。请回答:

(1)C的化学式为___________ 。
(2)A转化为B的反应的化学方程式为___________ 。
(3)B与D的反应属于___________ (填基本反应类型)。

(1)C的化学式为
(2)A转化为B的反应的化学方程式为
(3)B与D的反应属于
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐3】水是宝贵的自然资源,对于人类生活、生产都具有重要意义。
(1)水的组成
有关水的组成和结构的叙述中,正确的是____ (填字母);
A.水中氢、氧元素的质量比为2 :1
B.水是由水分子构成的
C.水分子是由氢分子和氧原子构成的
D.保持水的化学性质的最小微粒是氢原子和氧原子
(2)水的性质
① 少量下列物质加入到水中,充分搅拌后,可以得到溶液的是_______ 。
A.牛奶 B.花生油 C.面粉 D.蔗糖
② 实验室中用5g氯化钠配成溶质质量分数为10%的氯化钠溶液,则需加入蒸馏水______ mL。量取水时,若仰视,则会导致配制溶液的溶质质量分数 ____ (填“大于”、“小于”或“等于”)10%。
③ X、Y、Z三种不含结晶水的固体物质的溶解度曲线如图。

下列说法不正确的是_______ 。
A.Y中含有少量X,用海水晒盐的原理提纯Y
B.t3℃时,X、Y的饱和溶液降温到t2℃,析出晶体较多的是X
C.t3℃时,等质量的X、Y分别配成该温度下的饱和溶液,所得溶液质量X<Y
D.t1℃时,三种物质的饱和溶液升温到t2℃,溶液中溶质质量分数的大小是Y>X>Z
(3)水的用途

①实验A中水作________________ (填“溶剂”或“溶质”)。
②实验B中水的作用是提供热量和____________________ 。
③实验C中的水作______________________ 。
④灭火时将水喷成细雾状的主要原因是_______ (选填编号)。
A.降低着火点
B.增大与可燃物接触面积
C.与空气中气体反应生成CO2
D.隔离氧气
(1)水的组成
有关水的组成和结构的叙述中,正确的是
A.水中氢、氧元素的质量比为2 :1
B.水是由水分子构成的
C.水分子是由氢分子和氧原子构成的
D.保持水的化学性质的最小微粒是氢原子和氧原子
(2)水的性质
① 少量下列物质加入到水中,充分搅拌后,可以得到溶液的是
A.牛奶 B.花生油 C.面粉 D.蔗糖
② 实验室中用5g氯化钠配成溶质质量分数为10%的氯化钠溶液,则需加入蒸馏水
③ X、Y、Z三种不含结晶水的固体物质的溶解度曲线如图。

下列说法不正确的是
A.Y中含有少量X,用海水晒盐的原理提纯Y
B.t3℃时,X、Y的饱和溶液降温到t2℃,析出晶体较多的是X
C.t3℃时,等质量的X、Y分别配成该温度下的饱和溶液,所得溶液质量X<Y
D.t1℃时,三种物质的饱和溶液升温到t2℃,溶液中溶质质量分数的大小是Y>X>Z
(3)水的用途

①实验A中水作
②实验B中水的作用是提供热量和
③实验C中的水作
④灭火时将水喷成细雾状的主要原因是
A.降低着火点
B.增大与可燃物接触面积
C.与空气中气体反应生成CO2
D.隔离氧气
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐1】A、B两种固体物质的溶解度曲线如图1所示;20℃时,将A、B两种固体(A、B两物质均不含结晶水)各50g,分别加入盛有100g水的烧杯中,充分搅拌后的现象如图2所示;升温到50℃时,A、B两种固体在水中的溶解情况如图3所示。请回答下列问题:


(1)从20℃到50℃的变化过程中,一直处于饱和状态的是______ (选填“A”或“B”)的溶液。
(2)50℃时,A溶液的质量为______ 。图1中能表示A物质溶解度随温度变化的曲线是______ (选填“甲”或“乙”)。
(3)甲中含有少量乙,要提纯甲,可采用的方法是______ 。


(1)从20℃到50℃的变化过程中,一直处于饱和状态的是
(2)50℃时,A溶液的质量为
(3)甲中含有少量乙,要提纯甲,可采用的方法是
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
【推荐2】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
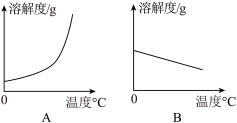
①依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中表示NaOH溶解度曲线的是_____ (填A或B)。
②把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有_____ 。(填一种)
③20℃时,191g饱和NaOH溶液,恒温蒸发10g水后,可析出NaOH晶体_____ g。
④现有60°C时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是_____ 。
⑤20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH_____ (填“偏大”、“偏小”或“不受影响”)。
| 温度/°C | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/(g/100g水) | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
①依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中表示NaOH溶解度曲线的是

②把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有
③20℃时,191g饱和NaOH溶液,恒温蒸发10g水后,可析出NaOH晶体
④现有60°C时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是
⑤20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH
您最近一年使用:0次
填空与简答-填空题
|
适中
(0.65)
解题方法
【推荐3】硝酸钾和氯化钾两种物质的溶解度曲线见图1,这两种物质的溶解度见表。


图1 图2
请回答下列问题:
(1)观察溶解度曲线和溶解度表,判断物质甲是指__________ (填写化学式)。
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用___________ 的方法提纯KNO3固体。
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t℃,析出晶体的质量关系为:KNO3________________ KCl(填写“>”、“=”、“<”或“无法确定”)。
(4)如图2所示,20℃时将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解向烧杯的水中加入某物质后试管内固体能完全溶解。则加入的物质可以是_________ (填序号)。
①冰块②生石灰固体③硝酸铵固体④氢氧化钠固体
(5)在20℃下配制甲物质的溶液,溶质的质量分数最大值为__________ (计算结果保留整数)。


图1 图2
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 |
| 甲溶解度/g | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 |
| 乙溶解度/g | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 |
(1)观察溶解度曲线和溶解度表,判断物质甲是指
(2)60℃时,饱和KNO3溶液中混有少量KCl,应采用
(3)60℃时,分别将等质量的KNO3和KCl两种物质的饱和溶液温度降至t℃,析出晶体的质量关系为:KNO3
(4)如图2所示,20℃时将一定质量的KNO3固体放入盛水的试管中,发现有少量固体未溶解向烧杯的水中加入某物质后试管内固体能完全溶解。则加入的物质可以是
①冰块②生石灰固体③硝酸铵固体④氢氧化钠固体
(5)在20℃下配制甲物质的溶液,溶质的质量分数最大值为
您最近一年使用:0次



