26. 某固体粉末由 Mg、MgO、Mg(OH)
2 中的一种或几种组成。某化学小组为了探究该固体粉末的成分,设计如图所示的装置(固定装置省略)。
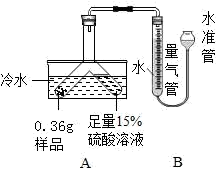
【信息资料】
(1)本实验条件下,氢气密度为 0.09g/L。
(2)Mg,MgO,Mg(OH)
2 均能与硫酸反应,且反应放热MgO + H
2SO
4 ═ MgSO
4 + H
2O;Mg(OH)
2 + H
2SO
4 ═ MgSO
4 + 2H
2O
(3)硫酸镁溶液中滴加氢氧化钠溶液会产生氢氧化镁沉淀MgSO
4 + 2NaOH ═ Na
2SO
4 + Mg(OH)
2↓
【实验过程】
步骤Ⅰ:检查装置气密性,装入药品并连接仪器。
步骤Ⅱ:倾斜 Y 形管,使样品充分反应,测得生成气体的体积 55.6mL(换算成该条件下气体质量约为 0.005g)。
步骤Ⅲ:拆下装置,往 Y 形管内残余液中加入氢氧化钠溶液,至不再生成沉淀。经过滤、洗涤和干燥后,称得沉淀质量为 0.58g。
【回答问题】
(1)该套装置气密性的检验说法正确的是
________。
A 把水准管下移一段距离,如果形成一定的液面差,则说明装置不漏气
B 把水准管下移一段距离,如果两边液面相平,则说明装置不漏气;
(2)用冷水浴的原因是
________。
(3)①使样品与硫酸充分反应的正确操作是
________(填标号)。
A 硫酸溶液转移到样品中
B 样品转移到硫酸溶液中
②判断样品完全反应的现象是
____________。
(4)根据实验结果分析:
①通过步骤Ⅱ推断,样品中一定含有的物质是
____________。通过步骤Ⅲ,经计算,样品中镁元素的总质量为
____________克。
②结论:该样品中的成分是
________。
(5)从该实验中得出制取硫酸镁的三种方法,得出这三个反应(Mg,MgO,Mg(OH)
2 分别与硫酸反应)中消耗等质量等浓度的硫酸,生成的硫酸镁质量
________(相等或不同)。
(6)该化学小组同学经过讨论得出以下结论,正确的是
________(填标号)。
A 利用该实验方案,能计算出样品中各物质的质量
B 实验前可通过样品的质量估算硫酸溶液的质量,确保样品完全反应
C 仅称量步骤Ⅱ中 Y 形管内药品减轻的质量(生成的氢气质量),就能计算出样品中各物质的质量